篇一 :电解水探究实验报告
电解水探究实验报告
一、文献综述:
(一)实验研究的背景和意义:
水是由氢氧两种原子按二比一的比例组合而成,采用熟悉的水做知识载体,通过对水分解产生氢气和氧气的微观过程的描述,认识到分子在化学变化中分子分解成原子,原子再重新组合形成新的分子,从而理解化学反应的实质。
(二)国内外研究现状和发展趋势:
国内外已根据相关原理发明了瓶装电解水、电解水制氧机及电解水制氢等,并将更深入的研究进行优化取得最小成本最大利益的成功。
(三)参考文献:
《2011-2015年中国电解水制氢设备行业市场深度研究分析报告》;专业文献;中学化学教材;贵州教育学院学报。
二、实验目的
1.熟练掌握电解水的实验操作;
2.培养学生“以教师的姿态”做好实验的预备实验以及进行演示的初步能力;
3.学习用正交表的方法寻找电解水实验的最佳反应条件和试验成功的关键;
4.通过本实验进一步培养学生研究化学实验的能力,培养良好的科学态度、品质和实验习惯。
三、实验仪器及药品:
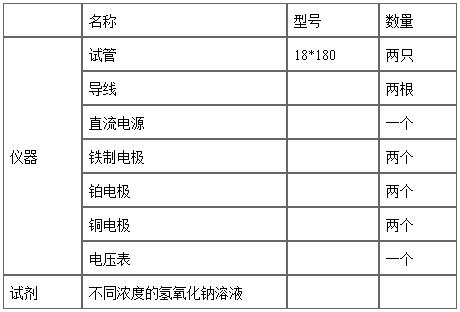
四、实验设计方案
(一)实验原理描述:水在通电的情况下可以发生电解,反应式如下
…… …… 余下全文
篇二 :电解水实验探究报告
电解水实验教学研究
摘要:
电解水实验是初中化学教学中的一个重要的实验,本实验从电极材料、电解液浓度和电压以及电极距进行分析,探索用简易装置在不同的条件下进行“电解水”实验时所产生的H2、O2对电解速度的影响。同时用正交试验法找到使氢、氧气体积比接近2:1的实验条件,找到最佳组合。
1 前言:
电解水实验是中学化学课本中一个非常重要的实验。该实验主要是验证水是由氢、氧两种元素组成的,实验的理论现象为:通电后,电极上出现气泡,一段时间后所收集到的氢、氧气体积比约为2:1。影响该实验的因素有以下几个:电解质种类、电解液浓度、电极材料、电极距、外加电压。通过探究的过程,利用正交实验法探究影响水电解实验的因素以及实验最佳条件。
2 实验原理:
水在通电情况下会发生水解,氢离子向负极移动,氢离子得负极电子而变成氢气,故阴极产物为氢气,而氢氧根离子向正极移动,氢氧根在水的参与下失去电子而得到氢离子和氧气,故阳极产物为氧气。其体积比为2:1,以此可以确定水的组成成分。纯水导电能力不强,电解速度慢,因此为改善这个问题,加快电解速度,可加入适量电解质来增强水的导电能力,本实验采用硫酸作为电解液,对电解液浓度,电压和电极矩三个因素进行分析比较,以便好中选优。
…… …… 余下全文
篇三 :电解水实验报告
电解水实验报告
实验原理:
水溶液中有氢离子和氢氧根离子,在通电的情况下,氢离子向负极移动,得电子形成氢气,氢氧根离子向正极移动,失电子,形成氧气和氢离子,形成的氢离子又往负极移动,这样就形成了一个闭合回路。
纯水导电能力不强,点解速率慢,原因在于氢离子在阴极的电子形成氢气,在阴极附近氢氧根离子浓度减少,导致水本来的电离平衡受到影响,阴极附近溶液带负电,吸引其他的正离子,影响氢离子在阴极被氧化,阳极原理也是如此。
加适量的电解质可以加快点解速率。本实验用的是10%的硫酸,硫酸浓度过大,实验不安全,过小不会对电解速率有多大的改善。
实验装置:


霍夫曼水电解器
简易水电解器不足之处:
1.电极、试管均不固定,不便于气体的收集;
2、试管没有刻度,不易准确地判断气体的体积比,无法进行定量研究;
3、实验时为增强水的导电性,常加入稀硫酸或氢氧化钠,收集气体时手与溶液接触,有腐蚀性;
4、实验无法反复使用;
5、电源装置比较笨重,携带不方便
霍夫曼水电解器不足之处:
…… …… 余下全文
篇四 :水、饱和氯化钠溶液的电解实验报告
水、饱和氯化钠溶液的电解
一、目的与要求
1、掌握演示电解水和电解饱和食盐水实验操作技能;
2、初步掌握这两个实验的讲解方法;
3、探索、设计电解水器的代用装置。
二、实验原理
水的电解
阴极反应:2H++2e→H2↑ 阳极反应:4OH--4e→2H2O+O2↑
总反应:2H2O=2H2↑+O2↑
饱和NaCl溶液的电解
阴极反应:2H++2e→H2↑ 阳极反应:2Cl--2e→Cl2↑
总反应:2NaCl+2H2O=H2↑+Cl2↑+2NaOH
三、主要仪器、材料与药品
仪器和材料:霍夫曼电解水器、直流低压电源、具支U形管、带刻度试管、石墨电极、铁电极、导线、玻璃棒、烧杯
药品:固体NaOH、酚酞试液、淀粉KI试纸、饱和NaCl溶液
四、实验内容
1.水的电解
…… …… 余下全文
篇五 :电解水设计实验方案报告书(打印)
设计实验方案报告书
开课学期 2014至 2015学年第 2学期
实验项目:电解水的实验研究
学生姓名:余庆梅 张怡 周玲玲 崔莹
指导教师: 杨国萍
学 号:12060143026 12060143031
12060143034 12060144001
专 业: 化学教育专业
班 级: 化本3班 化本1班
…… …… 余下全文
篇六 :水、饱和氯化钠溶液的电解实验报告
水、饱和氯化钠溶液的电解
一、 实验目的
1、 掌握演示电解水和电解饱和食盐水实验操作技能;
2、 初步掌握这两个实验的讲解方法;探索、设计电解水器的代用装置。
二、 实验原理
1、 水的电解:
阴极反应:4H++4e- →2H2↑
阳极反应:4OH--4e- →2H2O+O2↑
总反应:2H2O 通电 2H2↑+O2↑
电解水时,加入的电解质并不参与电极反应,主要是为了增加导电性。浓度过低,达不到效果,以5%以上为宜。
2、 饱和NaCl溶液的电解:
i 正接:阴极:Fe;阳极:碳棒。
阴极反应:2H++2e- →H2↑
…… …… 余下全文
篇七 :利用微型实验仪器电解水实验报告.doc
 实验六 微型技术电解水的实验探究
实验六 微型技术电解水的实验探究
【实验目的】
(1)理解在不同电解质溶液环境中电解水的原理规律。
(2)探究微型实验仪器电解水过程中电极变化原因。
【实验设计】
(1)实验原理
水是由氢离子和氢氧根离子结合组成的,氢离子带正电,电解时向负极移动,在负极得电子形成氢气;氢氧根离子带负电向正极移动在正极失电子形成氧气和水。总的电极反应方程式如下:
2H2O 2H2↑+O2↑
2H2↑+O2↑
为了增加水的导电性,一般可以在电导水中加入氢氧化钠、硫酸钠溶液等强酸强碱盐溶液或者是强碱溶液。
(2)实验仪器与药品
多用滴管、井穴板、低压电源(9~20V)、大头针、酒精灯、烧杯、滴管架、肥皂水、去离子水、自来水、KNO3溶液、NaOH溶液
(3)实验装置图


(4)实验步骤
① 配置溶液:
NaOH溶液:用钥匙取适量的NaOH于烧杯,加入适量的水,用玻璃棒搅拌使其溶解,备用;
…… …… 余下全文
篇八 :利用微型实验仪器电解水实验报告.doc
6.1利用微型技术电解水的实验探究
张慧
指导老师:罗秀玲
【实验目的】
①理解在不同电解质溶液环境中电解水的原理规律;
②探究微型实验仪器电解水过程中电极变化原因。
【实验设计】
(1)实验原理
2H2O 2H2↑+O2↑
2H2↑+O2↑
(2)实验仪器与药品
多用滴管、井穴板、低压电源(9~20V)、大头针、50ml烧杯(4个)、
肥皂水、水、H2SO4溶液、Na2SO4溶液、NaOH溶液
(3)实验装置图

(4)实验步骤
1) 配置溶液:
NaOH溶液(固体NaOH溶于水); Na2SO4溶液(固体Na2SO4溶于水) H2SO4溶液(浓硫酸稀释)
…… …… 余下全文