篇一 :MEDDEV 2.7.1 ver.3 临床评价报告样本(中文)
临床评价报告
数字X射线摄影系统: Xxxx 系列
编制:
批准:
1. 器械概述
产品名称:
产品型号:
制造商:
2. 器械及预期用途描述
2.1 预期用途: 数字X射线摄影系统,用于生成人体解剖组织的放射线图像。设计本系统的目的是在所有一般用途的诊断程序中替代放射线胶片/ 屏幕系统。本设备不用于乳腺X 射线成像应用。
2.2 器械描述: 按医用电气设备的安全分类属于Ⅰ类B型间歇加载连续运行固定式设备,诊断患者时人体与摄影床和探测器部分接触。
本X射线摄影系统功能组成有以下几部分构成。
3. 预期诊断适应症
本设备需要在隔离室内对需要诊断人体解剖组织的放射线图像的患者进行拍摄。不适用于乳腺X 射线成像应用。孕妇及儿童应遵守医师的诊断并了解放射拍片的危害。
…… …… 余下全文
篇二 :临床总结报告
SFDA临床试验批准号:2009L00235
儿肤康软膏
治疗小儿湿疮(亚急性湿疹)风热证(Ⅱ期)临床试验总结报告
试验负责单位(盖章):
试验负责单位地址:
试验负责:
试验设计:
试验日期:
试验参加单位:
原始资料保存地点:
联系人姓名:
联系人电话:
申报机构名称(盖章):
药品名称: 资料项目编号:30
临床研究计划与研究方案
试验负责单位(盖章):
试验负责单位地址:
试验负责单位地址:
试验参加单位:
原始资料保存地点:
联系人姓名:
联系人电话:
申报机构名称(盖章):
XX治疗XX病(XX证)临床研究计划
计划做哪几期临床试验
每期的样本量、试验方法
试验单位
试验进度安排
XX治疗XX病(XX证)II(或III)期临床试验方案
…… …… 余下全文
篇三 :临床评价报告
医用骨科牵引床 临床评价报告
目 录
1、产品简介
2、预期用途
3、产品分类
4、临床资料评估
5、临床对比分析
6、临床资料评估结论
7、风险分析
8、相关文件
9、附件
一次性使用内窥镜手术冲吸导管临床评价报告
1、 产品简介
1.1本公司生产的一次性使用内窥镜手术冲吸导管是依据国食药监械【2009】835号《医疗器械生产质量管理规范无菌医疗器械实施细则》及YY 0489-2004 《 一次性使用无菌引流导管及辅助器械》,并结合国内外产品的优点而开发的产品。目前该产品已通过江苏省医疗器械检验所检测。
1.2一次性使用内窥镜手术冲吸导管主要用于主要用于内窥镜手术。
1.3一次性使用内窥镜手术冲吸导管由穿刺头、接头、截流夹、导管、阀体、阀门和不锈钢接管组成
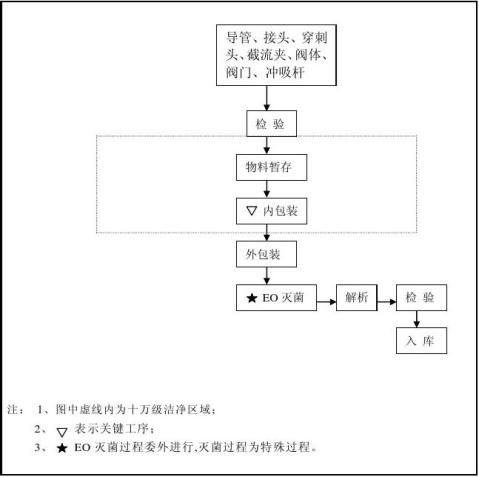
对以上关键过程和特殊过程,公司设置了质量控制点,做好各工序的检验记录进行控制。
1.5 产品在使用前已经灭菌,灭菌有效期为两年。
2、 预期用途
供临床冲洗引流用。
3、 产品分类
根据国家食品药品监督管理局《医疗器械分类管理目录》规定,一次性使用内窥镜手术冲吸导管属Ⅱ类医疗器械。
…… …… 余下全文
篇四 :临床评估报告模板
临床评估报告
(模板适用于设备)
文件编号:xxxxxxxx

编制:xxx
审核:xxx (需要有临床背景)
XXXXXXXXX有限公司
临床评价对象:(设备名称)
1. 临床使用情况的概述:
1.1 预期用途
1.2 基本结构
1.3 与其相配套的设施(如果有,包括连接接口的描述):
1.4 临床原理
3. 临床评价途径
EN ISO14155:2011Clinical investigation of medical devices for human subjects —
…… …… 余下全文
篇五 :临床报告
临床实习报告
转瞬间,紧张而又忙碌一年实习工作结束了。 大五,是不平静的一年。实习,求职,学习,工作,考研,所有的事都在这一年集中爆发了。这一年里经历的事仿佛比我前面四年所有经历的总和还多。在这一年的实习生活里,我认识到临床的实习是对理论学习阶段的巩固与加强,也是对临床技能操作的培养和锻炼,同时也是我们就业岗前的最佳训练。尽管这段时间不长,但对我们每个人都很重要。我们倍加珍惜这段时间,珍惜每一天的锻炼和自我提高的机会,珍惜与老师们这段难得的师徒之情。
因为有考研的打算,我选择了家乡的一家二甲医院—西安航空发动机(集团)有限公司职工医院(简称西航医院),虽然是一家二甲医院,但是科室齐全,病源充足。我暗暗告诉自己,要努力珍惜来之不易的实习机会。
我走进的第一个科室是神经内科。刚进科室,首先是要了解科室内部的运转及医疗文案书写,病史采集,体格检查,开检查单及化验单等这些基本的工作。并没有直接接触病人及具体疾病。我的切身体会是医生除了诊治疾病外,还要处理每天的许多繁文琐事。就拿写病程记录来讲,不得有一丝马虎,一旦写错,前功尽弃,重写。我本来就是一个急躁的人,刚开始总是写错,但经过一段时间,急躁少了些,耐心多了些,犯错少了些。每天总是感觉没干什么事,但每天回家总是很累。看来上班和上学的确是不一样的。
…… …… 余下全文
篇六 :临床试验总结报告结构
临床试验总结报告的结构和体例格式
第一部分 临床试验总结报告的结构
1. 题目封页
2. 试验药物与研究产品的名称
3. 研究药物的适应症
4. 主办者的名录
5. 研究的预期进度与试验安排
6. 试验开始数据(第一位受试者的数据和信息)
7. 末位受试者数据和信息
8. 试验完整数据列表
…… …… 余下全文
篇七 :临床危急值报告制度和流程
临床危急值报告制度和流程
一、为提高科室工作质量,避免医疗事故的发生。使临床能及时掌握病人情况,并提出处理意见,特制订危急值报告制度。 1、医技科室工作人员发现“危急值”情况时,检查(验)者首先要确认仪器、设备和检查过程是否正常,操作是否正确;核查检验标本是否有错,检验项目质控、定标、试剂是否正常,仪器传输是否有误。在确认检查(验)过程各环节无异常的情况下,需立即电话通知临床科室人员“危急值”结果,并在《危急值报告登记本》上逐项做好“危急值”报告登记。
2、临床科室人员在接到“危急值”报告电话后,应在临床科室《危急值报告登记本》上做好记录,同时及时通知主管医生或值班医生。
3、主管医生或值班医生如果认为该结果与患者的临床病情不相符,应进一步对病人进行检查;如认为检验结果不符,应关注标本留取情况。必要时,应重新留取标本送检进行复查。若该结果与临床相符,应在30分钟内结合临床情况采取相应处理措施,同时及时报告上级医师或科主任。
4、主管医生或值班医生需6小时内在病程中记录接收到的“危急值”报告结果和所采取的相关诊疗措施。
三、各临床、医技科室在实际诊疗工作,如发现所拟定“危急值”项目及“危急值”范围需要更改或增减,请及时与医务科联系,以便逐步和规范“危急值”报告制度。
…… …… 余下全文
篇八 :临床报告模板编写依据及数据分析说明
临床报告模板编写依据及数据分析说明
一、临床报告模板的编写依据
临床实验报告的主要按照《体外诊断试剂临床研究技术指导原则》(国食药监械[2007]229号)、《体外诊断试剂注册申报资料形式要求》(国食药监械[2007]609号)和《体外诊断试剂临床研究技术指导原则》(国食药监械[2007]240号)的要求编写,主体框架格式主要参考《体外诊断试剂临床研究技术指导原则》的规定,相关条文摘录如下:
(一)首篇
首篇是每份临床研究报告的第一部分,所有单个的临床研究报告均应包含该部分内容。
1.封面标题
包括进行临床研究产品的通用名、研究开始日期、研究完成日期、主要研究者(签名)、研究单位(盖章)、统计学负责人签名及单位盖章、产品注册申请人(盖章)、注册申请人的联系人及联系方式、报告日期、原始资料保存地点。
2.目录
列出整个临床试验报告的内容目录和对应页码。
3.研究摘要
对临床研究情况进行简单的介绍。
4.试验研究人员
列出临床试验主要研究人员的姓名、单位、在研究中的职责及其简历(列于附件中),主要研究人员包括主要研究者及各单位的主要参加人员、统计学分析的负责人、临床研究报告的撰写人。
…… …… 余下全文