篇一 :化学选修三,人教版知识点总结
选修三知识点
第一章 原子结构与性质
1能级与能层

⑴构造原理:随着核电荷数递增,大多数元素的电中性基态原子的电子按右图顺序填入核外电子运动轨道(能级),叫做构造原理。
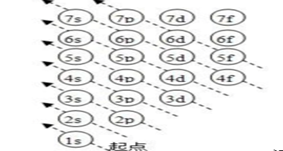
能级交错:由构造原理可知,电子先进入4s轨道,后进入3d轨道,这种现象叫能级交错。 说明:构造原理并不是说4s能级比3d能级能量低(实际上4s能级比3d能级能量高),而是指这样顺序填充电子可以使整个原子的能量最低。
(2)能量最低原理 现代物质结构理论证实,原子的电子排布遵循构造原理能使整个原子的能量处于最低状态,简称能量最低原理。 构造原理和能量最低原理是从整体角度考虑原子的能量高低,而不局限于某个能级。
(3)泡利(不相容)原理:基态多电子原子中,一个轨道里最多只能容纳两个电子,且电旋方向相反(用“↑↓”表示),这个原理称为泡利(Pauli)原理。
(4)洪特规则:当电子排布在同一能级的不同轨道(能量相同)时,总是优先单独占据一个轨道,而且自旋方向相同,这个规则叫洪特(Hund)规则
洪特规则特例:当p、d、f轨道填充的电子数为全空、半充满或全充满时,原子处于较稳定的状态。
…… …… 余下全文
篇二 :【人教版】高中化学选修3知识点总结
第一章原子结构与性质
一.原子结构
1.能级与能层

2.原子轨道

3.原子核外电子排布规律
⑴构造原理:随着核电荷数递增,大多数元素的电中性基 态原子的电子按右图顺序填入核外电子运动轨道(能级),叫做构造原理。
态原子的电子按右图顺序填入核外电子运动轨道(能级),叫做构造原理。
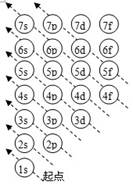
能级交错:由构造原理可知,电子先进入4s轨道,后进入3d轨道,这种现象叫能级交错。
说明:构造原理并不是说4s能级比3d能级能量低(实际上4s能级比3d能级能量高),而是指这样顺序填充电子可以使整个原子的能量最低。 也就是说,整个原子的能量不能机械地看做是各电子所处轨道的能量之和。
也就是说,整个原子的能量不能机械地看做是各电子所处轨道的能量之和。
(2)能量最低原理
现代物质结构理论证实,原子的电子排布遵循构造原理能使整个原子的能量处于最低状态,简称能量最 低原理。
低原理。
构造原理和能量最低原理是从整体角度考虑原子的能量高低,而不局限于某个能级。
(3)泡利(不相容)原理:基态多电子原子中,不可能同时存在4个量子数完全相同的电子。换言之,一个轨道里最多只能容纳两个电子,且电旋方向相反(用“↑↓”表示),这个原理称为泡利(Pauli)原理。
(4)洪特规则:当电子排布在同一能级的不同轨道(能量相同)时,总是优先单独占据一个轨道,而且自旋方向相同,这个规则叫洪特(Hund)规则。比如,p3的轨道式为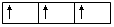
 或
或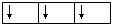
 ,而不是
,而不是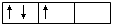
 。
。
…… …… 余下全文
篇三 :化学必修1第三章知识点总结
第三章金属及其化合物知识点总结及方程式
三种金属的比较

氧化钠与过氧化钠的比较

1.金属钠(1)是一种银白色的固体.它的密度比水要小,钠很软,熔沸点低,(2)在自然界中以化合态存在
2.钠放置在空气中先变暗,是因为钠与氧气反应生成的白色的氧化钠,再变潮湿是因为氧化钠与水反应生成的氢氧化钠易吸水.最后形成白色粉末是碳酸钠,
3.过氧化钠是一种强氧化剂,与水和二氧化碳反应都产生氧气。都是放热反应反应,过氧化钠都既做氧化剂又做还原剂,2mol过氧化钠反应时,都转移电子2mol
4.由于钠易与空气中的水或氧气反应,所以通常保存在煤油或石蜡油中.钠失火用干燥沙土盖灭
2、碳酸钠与碳酸氢钠的比较
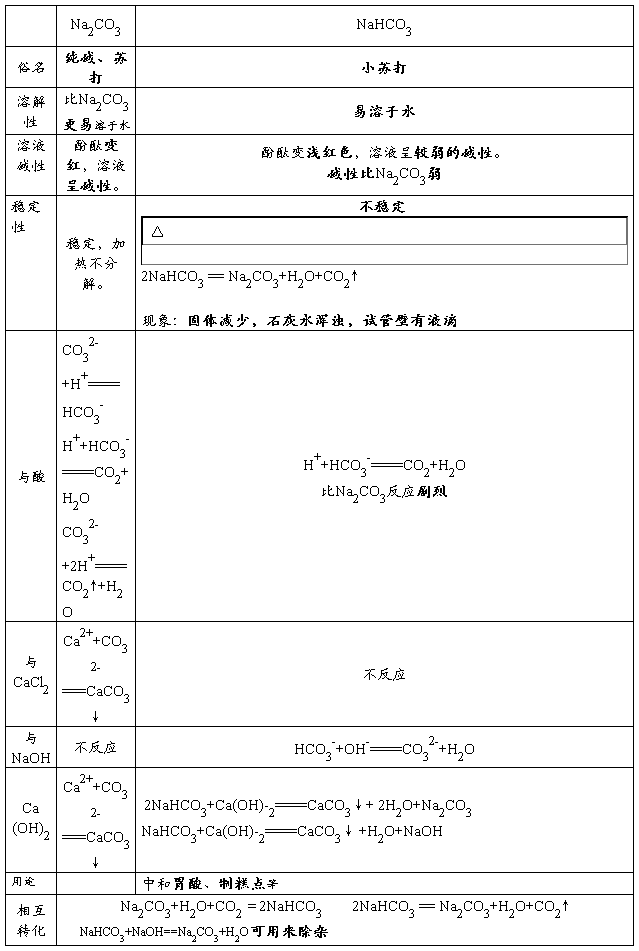
风化是化学变化
区别碳酸钠与碳酸氢钠可用
1. 与CaCl2反应有无沉淀2.与酸反应剧烈程度3碱性强弱4稳定性
2. 碳酸钠与盐酸互滴时现象不同,碳酸钠滴到盐酸中马上有气泡,盐酸滴到碳酸钠
中刚开始无现象,后有气泡
3除杂: Na2CO3固体(NaHCO3)加热; Na2CO3溶液(NaHCO3)适量NaOH
NaHCO3溶液(Na2CO3)足量CO2
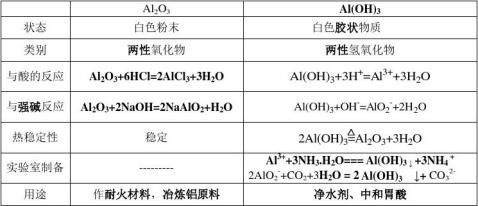
3、铝的氧化物和铝的氢氧化物
…… …… 余下全文
篇四 :高考生物必修3知识点总结(已做最佳处理)
必修3 第一章:人体的内环境与稳态
1、体液:体内含有的大量以水为基础的物体。 细胞内液(2/3) 体液细胞外液(1/3):包括:血浆、淋巴、组织液等
2、体液之间关系:
组织液淋巴
3、内环境:由细胞外液构成的液体环境。内环境作用:是细胞与外界环境进行物质交换的媒介。
4、组织液、淋巴的成分和含量与血浆的相近,但又不完全相同,最主要的差别在于血浆中含有较多的蛋白质,而组织液和淋巴中蛋白质含量较少
5、细胞外液的理化性质:渗透压、酸碱度、温度。
6、血浆中酸碱度:7.35---7.45 调节的试剂: 缓冲溶液: NaHCO3/H2CO3 Na2HPO4/ NaH2PO4
7、人体细胞外液正常的渗透压:770kPa、正常的温度:37度
8、稳态:正常机体通过调节作用,使各个器官、系统协调活动、共同维持内
环境的相对稳定的状态。内环境稳态指的是内环境的成分和理化性质都处于动态平衡中
9、稳态的调节:神经体液免疫共同调节
内环境稳态的意义:内环境稳态是机体进行正常生命活动的必要条件。
第二章;动物和人体生命活动的调节
1、神经调节的基本方式:反射
…… …… 余下全文
篇五 :【人教版】高中化学选修3知识点总结
第一章 原子结构与性质
一.原子结构
3.原子核外电子排布规律 ⑴构造原理:随着核电荷数递增,大多数元素的电中性基态原子的电子按右图顺序填入核外电子运动轨道(能级),叫做构造原理。
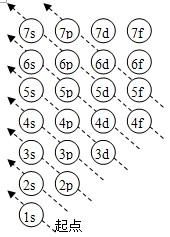
能级交错:由构造原理可知,电子先进入4s轨道,后进入3d轨道,这种现象叫能级交错。
说明:构造原理并不是说4s能级比3d能级能量低(实际上4s能级比3d能级能量高),而是指这样顺序填充电子可以使整个原子的能量最低。也就是说,整个原子的能量不能机械地看做是各电子所处轨道的能量之和。
(2)能量最低原理 现代物质结构理论证实,原子的电子排布遵循构造原理能使整个原子的能量处于最低状态,简称能量最低原理。 构造原理和能量最低原理是从整体角度考虑原子的能量高低,而不局限于某个能级。
(3)泡利(不相容)原理:基态多电子原子中,不可能同时存在4个量子数完全相同的电子。换言之,一个轨道里最多只能容纳两个电子,且电旋方向相反(用“↑↓”表示),这个原理称为泡利(Pauli)原理。
(4)洪特规则:当电子排布在同一能级的不同轨道(能量相同)时,总是优先单独占据一个轨道,而且自旋方向相同,这个规则叫洪特(Hund)规则。比如,p3
…… …… 余下全文
篇六 :化学必修1第三章知识点总结
第三章 金属及其化合物知识点总结及方程式
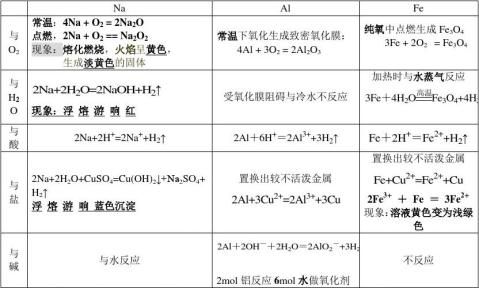
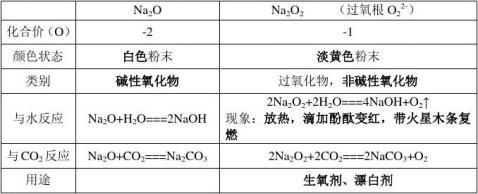

1.金属钠(1)是一种的固体.它的,钠很,,(2)在自然界中以化合态存在
2.钠放置在空气中先,是因为钠与氧气反应生成的,再变是因为氧化3反应,过氧化 4盖
2、碳酸钠与碳酸氢钠的比较
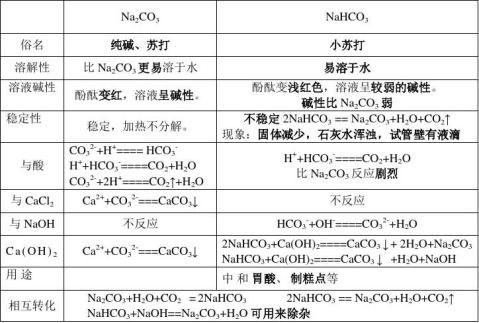
风化是化学变化
区别碳酸钠与碳酸氢钠可用
1. 与CaCl2反应有无沉淀2.与酸反应剧烈程度3碱性强弱4稳定性
2. 碳酸钠与盐酸互滴时中刚开始无现象,后有气泡
3除杂: Na2CO3固体(NaHCO3)加热; Na2CO3溶液(NaHCO3)适量NaOH
NaHCO3溶液(Na2CO3)足量CO2
1.Al3+和OH-互滴现象不同:OH-滴到Al3+中先沉淀后澄清;Al3+到OH-中先澄清后沉淀
Al3++3 OH-=Al(OH)3 ↓ Al(OH)3 + OH- = AlO2- +2 H2O
Al+4OH= AlO2 +2 H2O
2. NaAlO2 和盐酸-互滴现象不同:盐酸滴到NaAlO2中先沉淀后澄清;
NaAlO2 滴到盐酸中先澄清后沉淀
AlO2-+H++H2O=Al(OH)3 ↓ Al(OH)3 + 3H+ = Al3+ + 3H2O .AlO2-+4H+ = Al3+ + 2H2O
…… …… 余下全文
篇七 :高中生物必修三知识点总结
高二生物知识点归纳
必修3
第一章人体的内环境与稳态
一、细胞的生存环境:
1、单细胞直接与外界环境进行物质交换
2、多细胞动物通过内环境作媒介进行物质交换

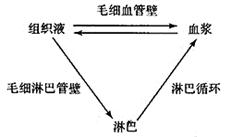
细胞外液主要是血浆、淋巴、组织液,又称内环境(是细胞与外界环境进行物质交换的媒介)
其中血细胞的内环境是血浆
淋巴细胞的内环境是淋巴
毛细血管壁的内环境是血浆、组织液
毛细淋巴管的内环境是淋巴、组织液
3、组织液、淋巴的成分与含量与血浆相近,但又完全不相同,最主要的差别在于血浆中含有较多的蛋白质,而组织液淋巴中蛋白质含量较少。
4、内环境的理化性质:渗透压,酸碱度,温度等相对稳定
①血浆渗透压大小主要与无机盐、蛋白质含量有关;无机盐中Na+、Cl- 占优势
细胞外液渗透压约为770kpa 相当于细胞内液渗透压;
②正常人的血浆近中性,PH为7.35-7.45与HCO3-、HPO42- 等离子有关;
③人的体温维持在370C 左右(一般不超过10C )。
二、内环境稳态的重要性:
1、稳态是指正常机体通过调节作用,使各个器官系统协调活动,共同维持内环境的相对稳定状态。
…… …… 余下全文
篇八 :高中生物必修三知识点总结
第一章:人体的内环境与稳态
1、体液:体内含有的大量以水为基础的物体。
细胞内液(2/3)
体液
细胞内液(1/3):包括:血浆、淋巴、组织液等
2、体液之间关系:
血浆 组织液 细胞内液
淋巴
3、内环境:由细胞外液构成的液体环境。
内环境作用:是细胞与外界环境进行物质交换的媒介。
4、组织液、淋巴的成分和含量与血浆的相近,但又不完全相同,最主要的差
别在于血浆中含有较多的蛋白质,而组织液和淋巴中蛋白质含量较少
5、细胞外液的理化性质:渗透压、酸碱度、温度。
6、血浆中酸碱度:7.35---7.45
调节的试剂: 缓冲溶液: NaHCO3/H2CO3 Na2HPO4/ NaH2PO4
7、人体细胞外液正常的渗透压:770kPa、正常的温度:37度
8、稳态:正常机体通过调节作用,使各个器官、系统协调活动、共同维持内
环境的相对稳定的状态。
内环境稳态指的是内环境的成分和理化性质都处于动态平衡中
9、稳态的调节:神经 体液 免疫共同调节
内环境稳态的意义:内环境稳态是机体进行正常生命活动的必要条件。
…… …… 余下全文