篇一 :有机化学方程式总结
高中有机化学方程式总结
一、烃
1.甲烷
烷烃通式:CnH2n-2
(1)氧化反应
甲烷的燃烧:CH点燃
4+2O2甲烷不可使酸性高锰酸钾溶液及溴水褪色。
2+2H2O
(2)取代反应
一氯甲烷:CH光
4+Cl2二氯甲烷:CHCl+Cl 光
CH3Cl+HCl
32
三氯甲烷:CH 光
CH2Cl2+HCl
2Cl2+Cl2 CHCl3+HCl(CHCl3又叫氯仿)四氯化碳:CHCl 光
3+ClCCl42.乙烯
+HCl
乙烯的制取:CHCH浓硫酸
32OH 170℃H2C=CH2↑+H2O
烯烃通式:C
nH2n
(1)氧化反应
高温
乙烯的燃烧:H2C=CH2+3O22CO2+2H2乙烯可以使酸性高锰酸钾溶液褪色,发生氧化反应。
O
(2)加成反应
与溴水加成:H
2C=CH2+Br与氢气加成:H 催
化剂 CH2Br—CH2Br
2C=CH2+H2CH3CH3
与氯化氢加成:H△
2C=CH2CH3CH2Cl
与水加成:H
2C=CH2+H2CH3CH2OH
(3)聚合反应
乙烯加聚,生成聚乙烯:n H2C=CH 2 - CH 3.乙炔
…… …… 余下全文
篇二 :大学有机化学方程式
1.加硫酸--烯烃的间接水合法制醇:
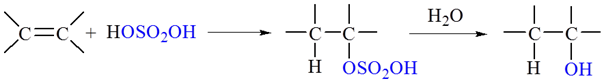
2.加水--烯烃的直接水合法制醇:

3.加卤素:

4.溴鎓离子机理:
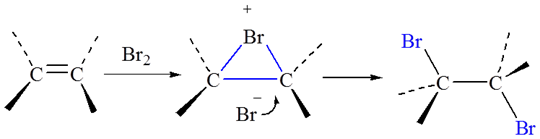
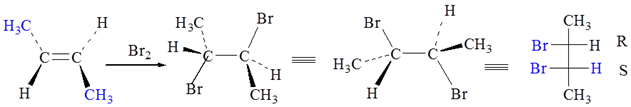
5.加次卤酸(X2/H2O or HXO):
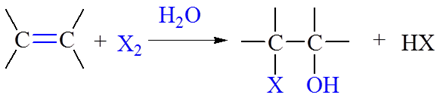
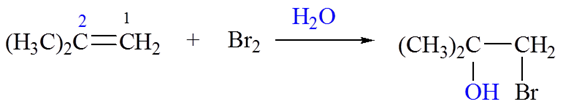
6.自由基加成反应(HBr 特有)
在过氧化物存在下与溴化氢反应得反马氏规则的加成产物:氢加到含氢较少的碳原子上
氯化氢和碘化氢没有过氧化物效应,加成取向仍符合马氏规则。HI吸热不易反应

7.硼氢化反应:
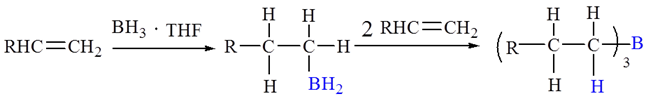
烷基硼烷在碱性条件下用过氧化氢处理转变成醇,反应后氢加在含氢较少的烯碳原子上,用来制备伯醇:
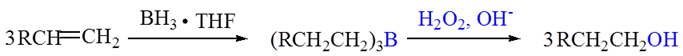
硼氢化反应得顺式加成产物,立体选择性很高,是一个立体专一性的反应。
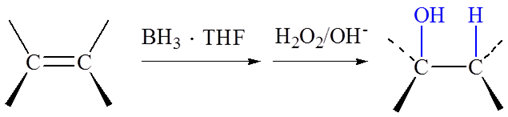
8.高锰酸钾氧化 :
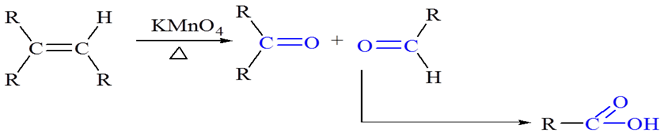
9.臭氧化还原反应 :

若无锌粉的存在该条件下醛会被继续还原成羧酸
10.环氧化反应:
烯烃被过氧酸氧化生成环氧化合物,该反应立体化学上是顺式反应
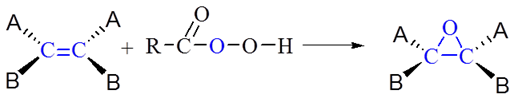
11.α-氢的反应
在高温或光照下,α-氢易被卤素取代,发生自由基取代反应
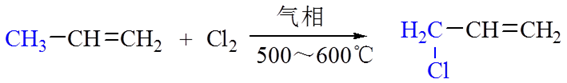
12.NBS:N-溴代丁二酰亚胺 ,常见的烯丙位溴代试剂。
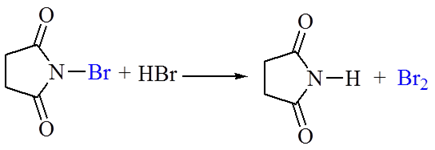
…… …… 余下全文
篇三 :有机化学基础方程式总结
一、脂肪烃
1.烷烃
化学性质:不与强酸、强碱、强氧化剂和强还原剂反应,不能使溴的四氯化碳溶液或酸性高锰酸钾溶液褪色。
(1)取代反应
CH3CH3 + Cl2 → CH3CH2Cl + HCl (光照条件)
(2)氧化反应—可燃性
CnH2n+2 + (3n+1)/2O2 → nCO2 + (n+1)H2O (点燃)
(3)分解反应
烷烃在隔绝空气的条件下加热或加催化剂可发生裂化或裂解。
C8H18 → C4H10 + C4H8 , C4H10 → CH4 + C3H6
2.烯烃
(1)烯烃通入酸性高锰酸钾溶液中会使溶液褪色
(2)催化氧化
2CH2=CH2 + O2 → 2CH3CHO (催化剂,加热)
(3)可燃性
烯烃燃烧火焰明亮,伴有黑烟
CnH2n + 3n/2O2 → nCO2 + nH2O (点燃)
(4)烯烃与H2,X2,HX,H2O发生加成反应
1溴水,卤素单质(X2) ○
CH2==CH2 + Br2 → CH2Br—CH2Br 常温下使溴水褪色
2氢气(H2) ○
CH2==CH2 + H2 → CH3—CH3 (催化剂,加热)
…… …… 余下全文
篇四 :大学有机化学期末复习总结
有机化学复习资料 公共基础学院一楼文印室提供 价格实惠 欢迎您光临!
有机化学复习总结
一、有机化合物的命名
命名是学习有机化学的“语言”,因此,要求学习者必须掌握。有机合物的命名包括俗名、习惯命名、系统命名等方法,要求能对常见有机化合物写出正确的名称或根据名称写出结构式或构型式。
1、 俗名及缩写 : 要求掌握一些常用俗名所代表的化合物的结构式,如:木醇、甘醇、 甘油、石炭酸、蚁酸、水杨醛、水杨酸、氯仿、草酸、苦味酸、肉桂酸、苯酐、甘氨酸、丙氨酸、谷氨酸、巴豆醛、葡萄糖、果糖等。还应熟悉一些常见的缩写及商品名称所代表的化合物,如:RNA、DNA2、习惯命名法
3、系统命名法:4、次序规则: (1优先次序为: (2次类推。常见 (3次序为: -C≡ 次序规则 烷烃的系则”一次列出 按照次序规则,>甲基。(1) :烯烃几何异构体的命名包括顺、反和Z、E两种方法。 Z、E表示。用顺反表示时,相同的原子或基团在反之为反式。如果双键碳原子上所连四个基团都不相同时,不能用顺反表示,只能用Z、E表示。按照“次序规则”比较两对基团的优先顺序,较优基团在双键碳原子同侧的为Z型,反之为E型。必须注意,顺、反和Z、E是两种不同的表示方法,不存在必然的内在联系。有的化合物可以用顺反表示,也可以用Z、E表示,顺式的不一定是Z型,反式的不一定是E型。例如:
…… …… 余下全文
篇五 :有机化学基础方程式总结
一、脂肪烃
1.烷烃
化学性质:不与强酸、强碱、强氧化剂和强还原剂反应,不能使溴的四氯化碳溶液或酸性高锰酸钾溶水:HC≡CH + H2O → CH3CHO (催化剂,加热)
卤素:HC≡CH + 2Br2 → CHBr2—CHBr2 (1,1,2,2 – 四溴乙烷) (5)加聚反应
液褪色。
(1)取代反应
CH3CH3 + Cl2 → CH3CH2Cl + HCl (光照条件) (2)氧化反应—可燃性
CnH2n+2 + (3n+1)/2O2 → nCO2 + (n+1)H2O (点燃) (3)分解反应
烷烃在隔绝空气的条件下加热或加催化剂可发生裂化或裂解。 C8H18 → C4H10 + C4H8 , C4H10 → CH4 + C3H6 2.烯烃
(1)烯烃通入酸性高锰酸钾溶液中会使溶液褪色 (2)催化氧化
2CH2=CH2 + O2 → 2CH3CHO (催化剂,加热) (3)可燃性
烯烃燃烧火焰明亮,伴有黑烟
CnH2n + 3n/2O2 → nCO2 + nH2O (点燃) (4)烯烃与H2,X2,HX,H2O发生加成反应 ○
…… …… 余下全文
篇六 :大学有机化学期末复习总结
有机化学期末复习总结
一、有机化合物的命名
命名是学习有机化学的“语言”,因此,要求学习者必须掌握。有机合物的命名包括俗名、习惯命名、系统命名等方法,要求能对常见有机化合物写出正确的名称或根据名称写出结构式或构型式。
1、 俗名及缩写 : 要求掌握一些常用俗名所代表的化合物的结构式,如:木醇、甘醇、
甘油、石炭酸、蚁酸、水杨醛、水杨酸、氯仿、草酸、苦味酸、肉桂酸、苯酐、甘氨酸、丙氨酸、谷氨酸、巴豆醛、葡萄糖、果糖等。还应熟悉一些常见的缩写及商品名称所代表的化合物,如:RNA、DNA、阿司匹林、福尔马林、尼古丁等。
2、习惯命名法:要求掌握“正、异、新”、“伯、仲、叔、季”等字头的含义及用法,
掌握常见烃基的结构,如:烯丙基、丙烯基、正丙基、异丙基、异丁基、叔丁基、苄基等。
3、系统命名法:系统命名法是有机化合物命名的重点,必须熟练掌握各类化合物的命名原则。其中烃类的命名是基础,几何异构体、光学异构体和多官能团化合物的命名是难点,应引起重视。要牢记命名中所遵循的“次序规则”。
4、次序规则:次序规则是各种取代基按照优先顺序排列的规则
(1)原子:原子序数大的排在前面,同位素质量数大的优先。几种常见原子的优先次序为:I>Br>Cl>S>P>O>N>C>H
…… …… 余下全文
篇七 :大学有机化学性质总结
有机化学复习资料—化学性质
烷烃及环烷烃的化学性质:
1. 烷烃卤代反应
2.环烷烃加成反应(加氢,加卤素,加卤化氢)
烯烃的化学性质:
1.加成反应(加氢,加水,加卤素,加次卤酸反式加成,自由基加成ROOR )
马氏规则的应用(形成稳定的正碳离子);个别化合物,要考虑甲基、氢的重排。 在过氧化物存在下,与HBr的自由基加成,反马氏规则。
烯烃的硼氢化-氧化反应条件:BH3或B2H6 →H2O2/OH-→H2O
反马氏规则, 顺型加成,产物是醇。
2.氧化反应
1.KMnO4溶液(碱性或中性) 产物邻二醇,顺式;
KMnO4溶液(酸性) 产物双键发生断裂。
(烯烃C=C 氧化为C=O; C=C 上的氢被氧化成羟基(-OH)。)
2.臭氧化反应:反应条件:O3→Zn/H2O 产物是醛、酮
炔烃的化学性质:
1.酸性(炔化银和炔化亚酮的生成与复原)
2.加成反应(加卤素,加卤化氢,加水H2O, HgSO4-H2SO4<互变异构> )
炔键在中间,生成反式加成产物。
在过氧化物存在下,与HBr的自由基加成,反马氏规则。
3. 氧化反应(KMnO4溶液(酸性),臭氧化反应)
…… …… 余下全文
篇八 :大学有机化学期末复习总结
有机化学期末复习总结
本课程的学习即将结束,现将全书的重点内容按命名、结构理论、基本反应、化合物转化及合成方法、鉴别等几个专题进行总结归纳,供同学们复习时参考。
一、有机化合物的命名
命名是学习有机化学的“语言”,因此,要求学习者必须掌握。有机合物的命名包括俗名、习惯命名、系统命名等方法,要求能对常见有机化合物写出正确的名称或根据名称写出结构式或构型式。
1、 俗名及缩写 要求掌握一些常用俗名所代表的化合物的结构式,如:木醇、甘醇、
甘油、石炭酸、蚁酸、水杨醛、水杨酸、氯仿、草酸、苦味酸、肉桂酸、苯酐、甘氨酸、丙氨酸、谷氨酸、巴豆醛、葡萄糖、果糖等。还应熟悉一些常见的缩写及商品名称所代表的化合物,如:RNA、DNA、阿司匹林、煤酚皂(来苏儿)、福尔马林、扑热息痛、尼古丁等。
2、习惯命名法 要求掌握“正、异、新”、“伯、仲、叔、季”等字头的含义及用法,
掌握常见烃基的结构,如:烯丙基、丙烯基、正丙基、异丙基、异丁基、叔丁基、苄基等。
3、系统命名法 系统命名法是有机化合物命名的重点,必须熟练掌握各类化合物的命名原则。其中烃类的命名是基础,几何异构体、光学异构体和多官能团化合物的命名是难点,应引起重视。要牢记命名中所遵循的“次序规则”。
…… …… 余下全文