篇一 :九年级下册化学知识点总结大全
20##年中考化学必记知识上策(下册)
学习化学要重点记忆的知识:物质的物理性质、物质的化学性质、化学反应方程式、化学反应现象、物质的用途等。
上册(1-7单元)化学方程式总汇
三大气体实验室制取:
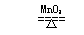 实验室制取氧气:(1-3)
实验室制取氧气:(1-3)
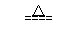 1、实验室用加热氯酸钾和二氧化锰制取氧气(二氧化锰作催化剂):2KClO3 2KCl + 3O2↑
1、实验室用加热氯酸钾和二氧化锰制取氧气(二氧化锰作催化剂):2KClO3 2KCl + 3O2↑
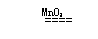 2、实验室用加热高锰酸钾制取氧气:2KMnO4 K2MnO4 + MnO2 + O2 ↑
2、实验室用加热高锰酸钾制取氧气:2KMnO4 K2MnO4 + MnO2 + O2 ↑
3、实验室用过氧化氢(又叫双氧水)与二氧化锰制取氧气(二氧化锰作催化剂):2H2O2 2H2O+ O2 ↑
实验室制取二氧化碳:(唯一个)
4、实验室用石灰石(或大理石,主要成分是碳酸钙)与稀盐酸制取二氧化碳:CaCO3+2HCl=CaCl2 + H2O + CO2↑
…… …… 余下全文
篇二 :九年级下册化学知识点总结大全
20##年中考化学必记知识上策(下册)
学习化学要重点记忆的知识:物质的物理性质、物质的化学性质、化学反应方程式、化学反应现象、物质的用途等。
上册(1-7单元)化学方程式总汇
三大气体实验室制取:
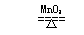 实验室制取氧气:(1-3)
实验室制取氧气:(1-3)
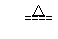 1、实验室用加热氯酸钾和二氧化锰制取氧气(二氧化锰作催化剂):2KClO3 2KCl + 3O2↑
1、实验室用加热氯酸钾和二氧化锰制取氧气(二氧化锰作催化剂):2KClO3 2KCl + 3O2↑
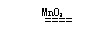 2、实验室用加热高锰酸钾制取氧气:2KMnO4 K2MnO4 + MnO2 + O2 ↑
2、实验室用加热高锰酸钾制取氧气:2KMnO4 K2MnO4 + MnO2 + O2 ↑
3、实验室用过氧化氢(又叫双氧水)与二氧化锰制取氧气(二氧化锰作催化剂):2H2O2 2H2O+ O2 ↑
实验室制取二氧化碳:(唯一个)
4、实验室用石灰石(或大理石,主要成分是碳酸钙)与稀盐酸制取二氧化碳:CaCO3+2HCl=CaCl2 + H2O + CO2↑
…… …… 余下全文
篇三 :初三化学(下册)重点知识点总结
第8单元 金属和金属材料
课题1 金属材料
一、金属和合金
1、金属的物理性质:常温下都是固体(汞除外),大多数为银白色,有金属光泽、优良的导电导热性、有延展性,密度、硬度较大,熔点较高。
2、性质与用途的关系:性质决定用途,但这不是唯一的决定因素,还要考虑价格、资源、美观、便利、回收以及对环境的影响。
3、合金
(1)合金是金属和其他金属(或非金属)熔合形成的具有金属特性物质。(合金属于混合物。)
(2)合金的性能与纯金属不同,硬度和强度一般比纯金属更高,抗腐性也更强。 (3)生铁和钢是两种常见的铁合金。
它们的根本区别是含碳量不同。
课题2 金属的化学性质
一、金属的化学性质
1、与氧气反应(很多金属在常温或高温下能和氧气反应,但剧烈和难易程度不同) ① 2Mg + O2 == 2 MgO
②4Al + 3O2 ==2 Al2O3 (氧化铝是致密的保护膜,能阻止铝被进一步氧化,所以铝具有很好的抗腐蚀性能)
③2Cu + O2 == 2CuO
2、活泼金属与稀酸反应(指稀盐酸和稀硫酸),能转换出酸中的氢。
①Fe +2 HCl == FeCl2 + H2 ↑
…… …… 余下全文
篇四 :九年级下册化学知识点总结大全
第八单元金属和金属材料
课题1 金属材料
1、人类从石器时代进入青铜器时代继而进入铁器时代,铝的利用要晚得多。
2、金属材料:金属材料包括纯金属和合金。合金(一定是混合物):由一种金属跟其他一种或几种金属(或金属与非金属)一起熔合而成的具有金属特性的物质。合金的特点:合金与组成它的纯金属对比:合金硬度变大、熔点变低、耐腐蚀性更好。因此,合金具有更广泛的用途。
3、一些金属的特性:大多数金属都呈银白色,但铜却呈紫红色,金呈黄色;在常温下,铁、铜、铝等大多数金属是固体,但体温计中的汞却是液体;
4、金属材料共同的物理性质:金属都具有金属光泽、导电性、导热性、延展性(能展成薄片、能拉成丝)等共同的物理性质。
5、决定物质用途的主要是物质的性质 ,但不是唯一的因素。还要考虑价格、资源、是否美观、使用是否便利、以及废料是否易于回收、对环境的影响。
5、金属之最:
(1)铝:地壳中含量最多的金属元素 (2)钙:人体中含量最多的金属元素
…… …… 余下全文
篇五 :九年级下册化学知识点总结大全
20##年中考化学必记知识上策(下册)
学习化学要重点记忆的知识:物质的物理性质、物质的化学性质、化学反应方程式、化学反应现象、物质的用途等。
上册(1-7单元)化学方程式总汇
三大气体实验室制取:
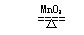 实验室制取氧气:(1-3)
实验室制取氧气:(1-3)
 1、实验室用加热氯酸钾和二氧化锰制取氧气(二氧化锰作催化剂):2KClO3 2KCl + 3O2↑
1、实验室用加热氯酸钾和二氧化锰制取氧气(二氧化锰作催化剂):2KClO3 2KCl + 3O2↑
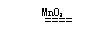 2、实验室用加热高锰酸钾制取氧气:2KMnO4 K2MnO4 + MnO2 + O2 ↑
2、实验室用加热高锰酸钾制取氧气:2KMnO4 K2MnO4 + MnO2 + O2 ↑
3、实验室用过氧化氢(又叫双氧水)与二氧化锰制取氧气(二氧化锰作催化剂):2H2O2 2H2O+ O2 ↑
实验室制取二氧化碳:(唯一个)
4、实验室用石灰石(或大理石,主要成分是碳酸钙)与稀盐酸制取二氧化碳:CaCO3+2HCl=CaCl2 + H2O + CO2↑
…… …… 余下全文
篇六 :化学九年级下册知识点归纳
金属的化学性质
2Mg+O2===2MgO 4Al+3O2===2Al2O3 3F+2O2=====Fe3O4 Cu+O2====2CuO
2、金属能和酸反应:金属(H前)+酸==盐+氢气 (置换反应)
Mg+2HCl==MgCl2+H2 Mg+H2SO4==MgSO4+H2 2Al+6HCl==2AlCl3+3H2 Zn+2HCl==ZnCl2+H2 Fe+2HCl==FeCl2+H2 Fe+H2SO4=FeSO4+H2 金属(前)+盐==金属(后)+盐 (置换反应)
Fe+CuSO4==Cu+FeSO4 (湿法炼铜的原理) Cu+2AgNO3==2Ag+Cu(NO3)2
酸的化学性质
紫色石蕊遇酸变红,无色酚酞遇酸不变色。
金属(H前)+酸==盐+氢气 (置换反应)
Mg+2HCl==MgCl2+H2 Mg+H2SO4==MgSO4+H2
3、酸能和金属氧化物反应:金属氧化物+酸==盐+水 (复分解反应)
Fe2O3+6HCl==2FeCl3+3H2O Fe2O3+3H2SO4==F2(SO4)3+3H2O CuO+H2SO4==CuSO4+H2O
…… …… 余下全文
篇七 :20xx年九年级下册化学知识点总结及排版
三十一中九年级化学下册知识点总结:
第八单元金属和金属材料 课题1 金属材料
1、人类从石器时代进入青铜器时代继而进入铁器时代,铝的利用要晚得多。
2、金属材料:金属材料包括纯金属和合金。合金(一定是混合物):由一种金属跟其他一种或几种金属(或金属与非金属)一起熔合而成的具有金属特性的物质。合金的特点:合金与组成它的纯金属对比:合金硬度变大、熔点变低、耐腐蚀性更好。因此,合金具有更广泛的用途。
3、一些金属的特性:大多数金属都呈银白色,但铜却呈紫红色,金呈黄色;在常温下,铁、铜、铝等大多数金属是固体,但体温计中的汞却是液体;
4、金属材料共同的物理性质:金属都具有金属光泽、导电性、导热性、延展性(能展成薄片、能拉成丝)等共同的物理性质。
5、决定物质用途的主要是物质的性质 ,但不是唯一的因素。还要考虑价格、资源、是否美观、使用是否便利、以及废料是否易于回收、对环境的影响。
5、金属之最:(1)铝:地壳中含量最多的金属元素 (2)钙:人体中含量最多的金属元素
…… …… 余下全文
篇八 :九年级化学(下册)知识点汇总
九年级化学(下册)知识点汇总
九年级化学(下册)知识点汇总
第八单元 金属和金属材料
?
? 第一节 金属材料 金属材料:金属材料包括纯金属以及它们的合金。 金属的物理性质
? 在常温下一般为固态(汞为液态),有金属光泽(大多数金属呈银白色,铜呈紫红色,金呈黄色); ? 导电性、导热性、熔点较高、有延展性、能够弯曲、硬度较大、密度较大。
金属之最
? 地壳中含量最多的金属元素——铝
? 人体中含量最多的金属元素——钙
? 目前世界年产量最多的金属——铁(铁>铝>铜)
?
? 熔点最高的金属——钨
? 熔点最低的金属——汞
? 硬度最大的金属——铬
? 密度最大的金属——锇
? 密度最小的金属——锂
金属的分类
黑色金属:通常指铁、锰、铬及它们的合金。
重金属:如铜、锌、铅等
轻金属:如钠、镁、铝等 ? ?
? 金属的应用
物质的性质在很大程度上决定了物质的用途,但这不是唯一的决定因素。在考虑物质的用途时,还需要考虑价格、资源、是否美观、使用是否便利,以及废料是否易于回收和对环境的影响等多种因素。 ? ————
? ? 铬——电镀——硬度大
?
…… …… 余下全文