篇一 :有机化学反应总结
有机化学反应总结
1、取代反应
(1).能发生取代反应的官能团有:醇羟基(-OH)、卤原子(-X)、羧基
(-COOH)、 酯基(-COO-)、肽键(-CONH-)等。
(2).能发生取代反应的有机物种类如下图所示:
2、加成反应
1.能发生加成反应的官能团:双键、三键、苯环、羰基(醛、酮)等。
2.加成反应有两个特点:
①反应发生在不饱和的键上,不饱和键中不稳定的共价键断裂,然后不饱和原
子与其 它原子或原子团以共价键结合。
②加成反应后生成物只有一种(不同于取代反应)。
说明:
1.羧基和酯基中的碳氧双键不能发生加成反应。
2.醛、酮的羰基只能与H2发生加成反应。
3.共轭二烯有两种不同的加成形式。
3、消去反应
(1).能发生消去反应的物质:醇、卤代烃;能发生消去反应的官能团有:醇
羟基、 卤素原子。
(2).反应机理:相邻消去 ,发生消去反应,必须是与羟基或卤素原子直接
相连的碳原子的邻位碳上必须有氢原子,否则不能发生消去反应。如CH3OH,没
…… …… 余下全文
篇二 :有机化学方程式总结
高中有机化学方程式总结
一、烃
1.甲烷
烷烃通式:CnH2n-2
(1)氧化反应
甲烷的燃烧:CH点燃
4+2O2甲烷不可使酸性高锰酸钾溶液及溴水褪色。
2+2H2O
(2)取代反应
一氯甲烷:CH光
4+Cl2二氯甲烷:CHCl+Cl 光
CH3Cl+HCl
32
三氯甲烷:CH 光
CH2Cl2+HCl
2Cl2+Cl2 CHCl3+HCl(CHCl3又叫氯仿)四氯化碳:CHCl 光
3+ClCCl42.乙烯
+HCl
乙烯的制取:CHCH浓硫酸
32OH 170℃H2C=CH2↑+H2O
烯烃通式:C
nH2n
(1)氧化反应
高温
乙烯的燃烧:H2C=CH2+3O22CO2+2H2乙烯可以使酸性高锰酸钾溶液褪色,发生氧化反应。
O
(2)加成反应
与溴水加成:H
2C=CH2+Br与氢气加成:H 催
化剂 CH2Br—CH2Br
2C=CH2+H2CH3CH3
与氯化氢加成:H△
2C=CH2CH3CH2Cl
与水加成:H
2C=CH2+H2CH3CH2OH
(3)聚合反应
乙烯加聚,生成聚乙烯:n H2C=CH 2 - CH 3.乙炔
…… …… 余下全文
篇三 :高中有机化学反应类型归纳总结
高中有机化学反应类型归纳总结
本文由 梦魇狂朝 整理后由张德莉老师批阅整理完成
(注:上中苯环全用“苯”字代替,箭头后的括号内容为反应条件) ★取代反应
烷:CH4+Cl2→(光)CH3Cl+HCl 苯:苯+Br2→(Fe)苯-Br+HBr(液溴)
苯+HO-NO2→(浓H2SO4;△)苯-NO2+H2O(硝化反应)
甲苯:苯-CH3+3HO-NO2→(浓H2SO4;△)三硝基甲苯(TNT)+3H2O 苯-CH3+Cl2→(光)苯-CH2Cl+HCl 醇:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
卤代烃:CH3CH2Br+NaOH→(△)CH3CH2OH+NaBr(水解反应) 另有酯化,硫化,水解等
★加成反应
烯:CH2=CH2+Br2→CH2BrCH2Br CH2=CH2+H2O→(催化剂;△)CH3CH2OH CH2=CH2+H2→(Ni)CH3CH3 炔:CH≡CH+2Br2→CHBr2CHBr2 苯:苯+3H2→(Ni)C6H6(环已烷) 苯+3Cl2→C6H6Cl6(六六六)
醛:CH3CHO+H2→(Ni;△)CH3CH2OH(加氢还原) 另有加聚
…… …… 余下全文
篇四 :有机化学总结全部
一烃的衍生物性质对比 1.脂肪醇、芳香醇、酚的比较
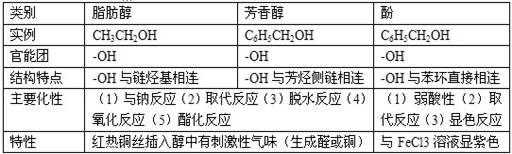
2.苯、甲苯、苯酚的分子结构及典型性质比较
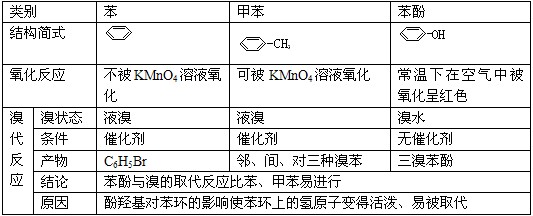
3.醛、羰酸、酯(油脂)的综合比较
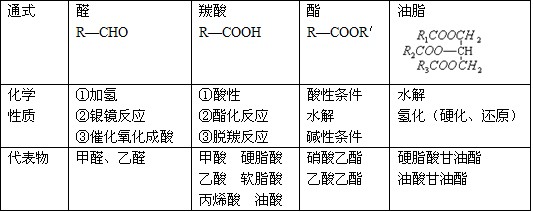
4.烃的羟基衍生物性质比较
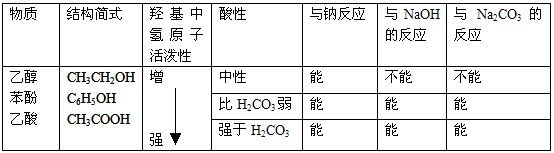
5.烃的羰基衍生物性质比较
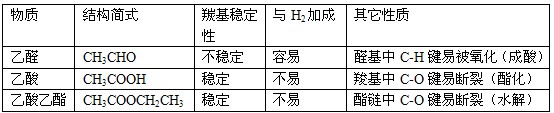
6.酯化反应与中和反应的比较

7.烃的衍生物的比较
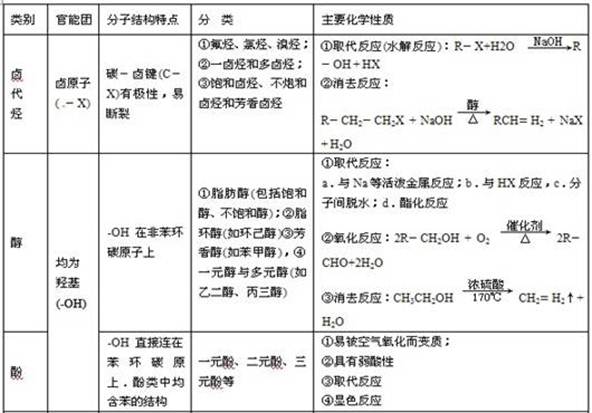

二、有机反应的主要类型
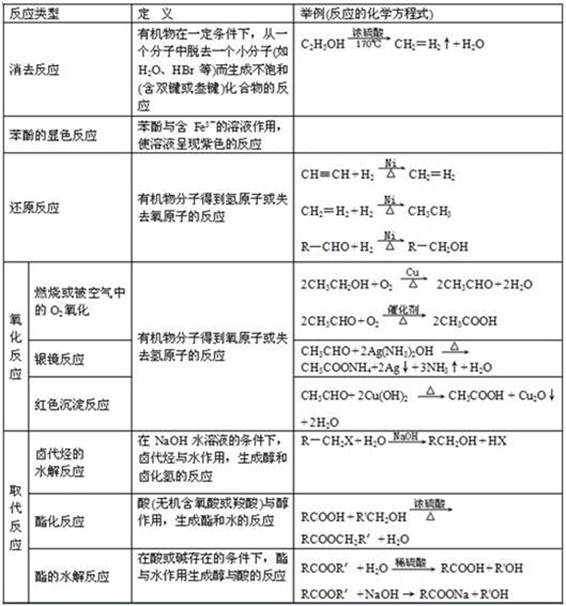
三、烃及其重要衍生物之间的相互转化关系
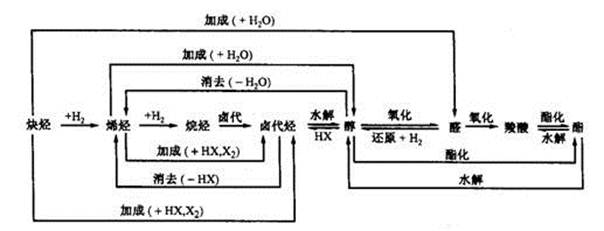
要点精讲
一、有机化合物的分类
…… …… 余下全文
篇五 :有机化学反应机理总结
引言
反应机理是对一个反应过程的详细描述,在表述反应机理时,必须指出电子的流向,并规定用箭头表示一对电子的转移。
摘要:反应机理是根据很多实验事实总结后提出的,它有一定的适用范围,能解释很多实验事实,并能预测反应的发生。如果发现新的实验事实无法用原有的反应机理来解释,就要提出新的反应机理。反应机理已成为有机结构理论的一部分。
关键词: 反应 反应机理 自由基反应
有机化合物分子中的某个原子或基团被其它原子或基团所置换的反应称为取代反应。若取代反应是按共价键均裂的方式进行的,即是由于分子经过均裂产生自由基而引发的,则称其为自由基型取代反应。
自由基反应包括链引发、链转移、链终止三个阶段。链引发阶段是产生自由基的阶段。由于键的均裂需要能量,所以链引发阶段需要加热或光照。链转移阶段是由一个自由基转变成另一个自由基的阶段,犹如接力赛一样,自由基不断地传递下去,像一环接一环的链,所以称之为链反应。链终止阶段是消失自由基的阶段。自由基两两结合成键。所有的自由基都消失了,自由基反应也就终止了。
分子中的原子或基团被卤原子取代的反应称为卤化反应。若卤原子为氯原子,则该卤化反应称为氯化反应。
…… …… 余下全文
篇六 :高中有机化学各物质特征反应总结
高中有机化学各物质特点总结
有机物的物理性质
1、状态:
固态:饱和高级脂肪酸、脂肪、葡萄糖、果糖、蔗糖、麦芽糖、淀粉、维
生素、醋酸(16.6℃以下);
气态:C4以下的烷、烯、炔烃、甲醛、一氯甲烷、新戊烷;
液态: 油状:乙酸乙酯、油酸;
粘稠状:石油、乙二醇、丙三醇。
2、气味:
无味:甲烷、乙炔(常因混有PH3、H2S和AsH3而带有臭味);
稍有气味:乙烯;
特殊气味:甲醛、乙醛、甲酸和乙酸;
香味:乙醇、低级酯;
3、颜色:
白色:葡萄糖、多糖
黑色或深棕色:石油
4、密度:
比水轻:苯、液态烃、一氯代烃、乙醇、乙醛、低级酯、汽油;
比水重:溴苯、乙二醇、丙三醇、CCl4。
5、挥发性:
乙醇、乙醛、乙酸。
6、水溶性:
不溶:高级脂肪酸、酯、溴苯、甲烷、乙烯、苯及同系物、石油、CCl4;
易溶:甲醛、乙酸、乙二醇;
能与溴水发生化学反应而使溴水褪色或变色的物质
1、有机物:
⑴ 不饱和烃(烯烃、炔烃、二烯烃等)
⑵ 不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等)
⑶ 石油产品(裂化气、裂解气、裂化汽油等)
…… …… 余下全文
篇七 :高中有机化学各物质特征反应总结
高中有机化学各物质特点总结
有机物的物理性质
1、状态:
固态:饱和高级脂肪酸、脂肪、葡萄糖、果糖、蔗糖、麦芽糖、淀粉、维生素、醋酸(16.6℃以下);
气态:C4以下的烷、烯、炔烃、甲醛、一氯甲烷、新戊烷;
液态:
 油状:乙酸乙酯、油酸;
油状:乙酸乙酯、油酸;
粘稠状:石油、乙二醇、丙三醇。
2、气味:
无味:甲烷、乙炔(常因混有PH3、H2S和AsH3而带有臭味);
稍有气味:乙烯;
特殊气味:甲醛、乙醛、甲酸和乙酸;
香味:乙醇、低级酯;
3、颜色:
白色:葡萄糖、多糖
黑色或深棕色:石油
4、密度:
比水轻:苯、液态烃、一氯代烃、乙醇、乙醛、低级酯、汽油;
比水重:溴苯、乙二醇、丙三醇、CCl4。
5、挥发性:
乙醇、乙醛、乙酸。
6、水溶性:
不溶:高级脂肪酸、酯、溴苯、甲烷、乙烯、苯及同系物、石油、CCl4;
易溶:甲醛、乙酸、乙二醇;
能与溴水发生化学反应而使溴水褪色或变色的物质
1、有机物:
⑴ 不饱和烃(烯烃、炔烃、二烯烃等)
⑵ 不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等)
⑶ 石油产品(裂化气、裂解气、裂化汽油等)
⑷ 含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等)
…… …… 余下全文
篇八 :高中有机化学常用反应方程式和相关知识点总结)
高中有機化學方程式匯總
 一:烷烃
一:烷烃
 1. CH4 + Cl2 CH3Cl + HCl
1. CH4 + Cl2 CH3Cl + HCl
 2. CH3Cl + Cl2 CH2Cl2 + HCl
2. CH3Cl + Cl2 CH2Cl2 + HCl
 4. CHCl3 + Cl2 CCl4+ HCl
4. CHCl3 + Cl2 CCl4+ HCl
 5. CH4 C +2H2
5. CH4 C +2H2
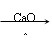 6. C16H34 C8H18 + C8H16
6. C16H34 C8H18 + C8H16
7. CH3COONa + NaOH CH4↑+ Na2CO3
…… …… 余下全文