篇一 :物理化学总结
物理化学总结
一、简史
随着化学与物理学两个学科的发展,二者之间相互结合渗透并吸收其他学科(如计算机、数学等)的科研成果逐步形成比较成熟的现代的物理化学。热力学第一定律和第二定律被广泛地应用于化学系统 。1840年,盖斯(Hess)建立了热化学定律。1876年,美国的化学家吉布斯(Gibbs),对化学热力学贡献最大,引出了吉布斯自由能,定义了化学势,形成一套完整的处理方法,对相平衡、化学平衡等进行了严密地数学处理。1884年范特荷夫(Van't Hoff),创立了稀溶液理论,推导出化学平衡的等温方程式。1886~1893年间F.M.拉乌尔发表了关于系列物质蒸气压与溶液浓度、溶液凝固点与温度方面论文提出了拉乌尔定律和非挥发溶质溶剂凝固点降低规律。J.W.吉布斯对多相系统平衡的研究并建立了相律,奠定了化学热力学重要理论基础。1886年,阿仑尼乌斯(S.Anhencus)建立电离理论,揭了电解质水溶液的本性。在化学动力学上作出很大贡献。提出了阿仑尼乌斯方程式。1906年能斯特(W.Nernst)发现了热定律,建立了热力学第三定律,他还对电化学作出很大的贡献,提出了能斯特方程。。化学热力学基本理论已经臻于成熟。
…… …… 余下全文
篇二 :物理化学各章节总结
物理化学每章总结
第1章热力学第一定律及应用
1.系统、环境及性质
热力学中把研究的对象(物质和空间)称为系统,与系统密切相关的其余物质和空间称为环境。根据系统与环境之间是否有能量交换和物质交换系统分为三类:孤立系统、封闭系统和敞开系统。


2.热力学平衡态
系统的各种宏观性质不随时间而变化,则称该系统处于热力学平衡态。必须同时包括四个平衡:力平衡、热平衡、相平衡、化学平衡。
3.热与功
(1) 热与功的定义
热的定义:由于系统与环境间温度差的存在而引起的能量传递形式。以Q表示,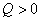 表示环境向系统传热。
表示环境向系统传热。
功的定义:由于系统与环境之间压力差的存在或其它机、电的存在引起的能量传递形式。以W表示。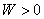 表示环境对系统做功。
表示环境对系统做功。
(2) 体积功与非体积功
功有多种形式,通常涉及到是体积功,是系统体积变化时的功,其定义为: 
…… …… 余下全文
篇三 :物理化学重点超强总结
第一章 热力学第一定律 1、热力学三大系统:
(1)敞开系统:有物质和能量交换; (2)密闭系统:无物质交换,有能量交换; (3) 隔绝系统(孤立系统):无物质和能量交换。 2、状态性质(状态函数):
(1)容量性质(广度性质):如体积,质量,热容量。 数值与物质的量成正比;具有加和性。 (2)强度性质:如压力,温度,粘度,密度。
数值与物质的量无关;不具有加和性,整个系统的强度性质的数值与各部分的相同。
特征:往往两个容量性质之比成为系统的强度性质。 3、热力学四大平衡:
(1)热平衡:没有热隔壁,系统各部分没有温度差。
(2)机械平衡:没有刚壁,系统各部分没有不平衡的力存在,即压力相同 (3)化学平衡:没有化学变化的阻力因素存在,系统组成不随时间而变化。 (4)相平衡:在系统中各个相(包括气、液、固)的数量和组成不随时间而变化。 4、热力学第一定律的数学表达式:
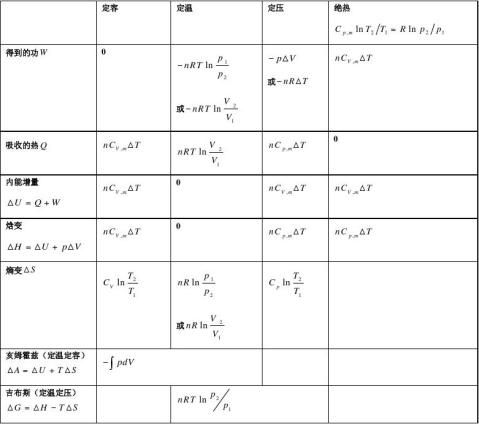
1
12、在通常温度下,对理想气体来说,定容摩尔热容为:
单原子分子系统 CV,m=
32
R
5262
双原子分子(或线型分子)系统 CV,m=多原子分子(非线型)系统 CV,m?定压摩尔热容:
…… …… 余下全文
篇四 :物理化学(下)总结
《物理化学》(下) (南京大学第五版)总结
第八章 电解质溶液
一、基本概念与定义
1. 离子迁移数t
电解质溶液导电时,溶液中的i离子运载的电流Ii与总电流之比(即i离子所承担的导电任务的分数)。

2. 离子电迁移率(离子淌度)ui:单位电位梯度时离子的运动速率。
3. 电导与电导率
电导G(W-1):电阻R的倒数。a
电导率k(W-1·m-1):电阻率r的倒数。
电导池常数Kcell:Kcell = L/A
L: 电极之间的距离;A:电极的面积
4. 摩尔电导率Lm(S·m2·mol-1)
含1mol电解质的溶液置于相距单位距离的2个平行电极之间的电导池所具有的电导。
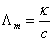
5.电解质的平均活度和平均活度因子
对于任意价型的强电解质Mn+Bn-
平均活度因子 g± =[ (g+)n+ (g-)n-]1/(n+ +n-)
a± = m±g±
m± =[ (m+)n+ (m-)n-]1/(n+ +n-)
m+ = n+m;m- = n-m
…… …… 余下全文
篇五 :物理化学学习小结
物理化学学习小结
本学期,我们学习了物理化学这门课程,在这近半年的物理化学学习历程中,对于物理化学这门课程,我自己内心有了属于自己的深深地体会,在刚刚开始学习物理化学这门课程是,由于自己认识的不到位,准备的不充分以及对于老师更替的较长时间的适应,导致自己在学习这门课程上走了不少弯路。
总体来看,首先就是对于即将学习的这门课程的认识认识和把握不充分,由于认为这门课程可能就是大学物理和化学的杂合体,自恃大学物理和化学掌握的还不错的我能一开始并没有给予这门课程有足够的认识,等到了学习一段时间之后,才慢慢觉得这门课程的晦涩与难懂。其次,从最开始,对于这门课程就没有一个宏观的把握,只知道跟随老师的不发而缺乏对于整体的认识,缺乏将知识点彼此串联起来的能力。然后就是在准备方面,从小学时,老师就教导我们,课前要预习,课后要认真复习,可是就玉溪这一方面,自己做的远远不够,也因此有时候上课听不懂老师所讲的内容,从而严重打击了自己的学习物理化学的积极性。对于物理化学课程自己也产生了排斥的情绪。最后就是在学习物理化学的态度方面的问题,曾近有老师哦和我们说,大学里课堂上知识听不完全懂是很正常的现象,但是你还要认真听,课后要针对你所不懂的地方进行复习,但是自己可能只听到发哦了前半句话,而对于后半句话可能并没有留心,虽然物化课堂上自己一直坐在前排听课,但是在课堂上有时候依旧没有认真地听课,课后也没有针对自己所不懂得地方做好复习的工作,等到现阶段真正复习的阶段了,才发现,往往一小块知识点也需要自己花很长一段时间去搞明白,自此才真正觉得得不偿失,上课的时候应该认真听老师讲课,做好课堂知识点的归纳,做好课堂笔记。
…… …… 余下全文
篇六 :物理化学总结
第一章 热力学第一定律
一、基本概念
系统与环境,状态与状态函数,广度性质与强度性质,过程与途径,热与功,内能与焓。
二、基本定律
热力学第一定律:ΔU=Q+W。
焦耳实验:ΔU=f(T) ; ΔH=f(T)
三、基本关系式
1、体积功的计算 δW= -pedV
恒外压过程:W= -peΔV
可逆过程: W=nRT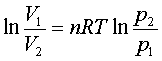
2、热效应、焓
等容热:QV =ΔU(封闭系统不作其他功)
等压热:Qp =ΔH(封闭系统不作其他功)
焓的定义:H=U+pV ; dH=dU+d(pV)
焓与温度的关系:ΔH=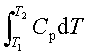
3、等压热容与等容热容
热容定义: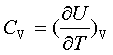 ;
;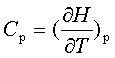
定压热容与定容热容的关系:
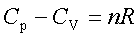
热容与温度的关系:Cp=a+bT+c’T2
四、第一定律的应用
1、理想气体状态变化
等温过程:ΔU=0 ; ΔH=0 ; W=-Q=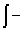 pedV
pedV
等容过程:W=0 ; Q=ΔU= ; ΔH=
; ΔH=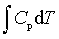
…… …… 余下全文
篇七 :物理化学复习归纳
第一章热力学第一定律
1.基本概念
1.1体系和环境
系统(System)-被划定的研究对象称为系统。
环境(surroundings)- 与系统密切相关、有相互作用或影响所能及的部分称为环境。
1.2状态函数
*状态函数——由系统的状态确定的系统的各种热力学性质称为系统的状态函数。
*它具有以下特点:
(1)状态函数是状态的单一函数。
(2)系统的状态发生变化,状态函数的变化值取决于系统始、终态。与所经历的途径无关。
(3)状态函数的微小变化,在数学上是全微分。
(4)不同状态函数的集合(和、差、积、商)也是状态函数。
1.3体积功
功(work)--系统与环境之间传递的除热以外的其它能量都称为功,用符号W表示。体积功就是体积膨胀或缩小所做的功。
系统对环境作功,W<0 环境对体系作功,W>0
…… …… 余下全文
篇八 :物理化学总结
第二章 热力学第一定律
一、基本概念
系统与环境,状态与状态函数,广度性质与强度性质,过程与途径,热与功,内能与焓。
二、基本定律
热力学第一定律:ΔU=Q+W。
焦耳实验:ΔU=f(T) ; ΔH=f(T)
三、基本关系式
1、体积功的计算 δW= -pedV
恒外压过程:W= -peΔV
可逆过程: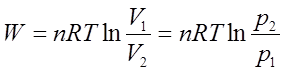
2、热效应、焓
等容热:QV =ΔU(封闭系统不作其他功)
等压热:Qp =ΔH(封闭系统不作其他功)
焓的定义:H=U+pV ; dH=dU+d(pV)
焓与温度的关系:ΔH=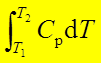
3、等压热容与等容热容
热容定义: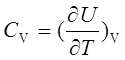 ;
;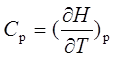
定压热容与定容热容的关系:
热容与温度的关系:Cp=a+bT+c’T2
四、第一定律的应用
1、理想气体状态变化
等温过程:ΔU=0 ; ΔH=0 ; W=-Q= pedV
pedV
等容过程:W=0 ; Q=ΔU=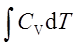 ; ΔH=
; ΔH=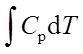
等压过程:W=-peΔV ; Q=ΔH=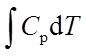 ; ΔU=
; ΔU=
可逆绝热过程:Q=0 ; 利用p1V1γ=p2V2γ求出T2,
W=ΔU=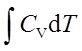 ;ΔH=
;ΔH=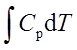
不可逆绝热过程:
…… …… 余下全文