篇一 :高中化学有机物知识总结
高中化学有机物知识总结
一、有机代表物质的物理性质
1. 状态
固态:饱和高级脂肪酸、脂肪、TNT、萘、苯酚、葡萄糖、果糖、麦芽糖、淀粉、纤维素、醋(16.6℃
以下)
气态:C4以下的烷烃、烯烃、炔烃、甲醛、一氯甲烷
液态:油 状:硝基苯、溴乙烷、乙酸乙酯、油酸
粘稠状:石油、乙二醇、丙三醇
2. 气味
无味:甲烷、乙炔(常因混有PH3、H2S和AsH3而带有臭味))
稍有气味:乙烯 特殊气味:苯及苯的同系物、萘、石油、苯酚
刺激性:甲醛、甲酸、乙酸、乙醛
甜味:乙二醇(甘醇)、丙三醇(甘油)、蔗糖、葡萄糖
香味:乙醇、低级酯 苦杏仁味:硝基苯
3. 颜色
白色:葡萄糖、多糖 淡黄色:TNT、不纯的硝基苯 黑色或深棕色:石油
4. 密度
比水轻的:苯及苯的同系物、一氯代烃、乙醇、低级酯、汽油
比水重的:硝基苯、溴苯、乙二醇、丙三醇、CCl4、氯仿、溴代烃、碘代烃
5. 挥发性:乙醇、乙醛、乙酸
6. 升华性:萘、蒽
7. 水溶性: 不溶:高级脂肪酸、酯、硝基苯、溴苯、烷烃、烯烃、炔烃、苯及苯的同系物、萘、蒽、石油、卤代烃、TNT、氯仿、CCl4 能溶:苯酚(0℃时是微溶) 微溶:乙炔、苯甲酸 易溶:甲醛、乙酸、乙二醇、苯磺酸 与水混溶:乙醇、苯酚(65℃以上)、乙醛、甲酸、丙三醇
…… …… 余下全文
篇二 :高中化学有机物总结
高中有机化学总结
1.能与Na反应的有机物: 醇、酚、羧酸等——凡含羟基的化合物。
2、能与NaOH溶液发生反应的有机物:1.羧酸,如:CH3COOH+NaOH--->CH3COONa+H2O(中和反应)
说明:氨基酸也有类似反应
2.酯,如:CH3COOC2H5+NaOH--->CH3COONa+C2H5OH(水解反应)
说明:油脂也有类似反应
3.酚,如:C6H5OH+NAOH--->C6H5ONa+H2O(类似于酸碱中和反应)
说明:上面方程中的C6H5表示苯基
4.卤代烃,如:
CH3Cl+NaOH--->CH3OH+NaCl(碱性水解,反应条件:与NaOH水溶液共热)
CH3CH2Cl+NaOH--->CH2=CH2+NaCl+H2O(消去反应,反应条件:与NaOH醇溶液共热)
说明:另外,某些醛也可以跟NaOH发生歧化反应,但中学不学习。
…… …… 余下全文
篇三 :高中化学有机物总结
一、 物理性质
甲烷:无色无味难溶
乙烯:无色稍有气味难溶
乙炔:无色无味微溶
(电石生成:含H2S、PH3 特殊难闻的臭味)
苯:无色有特殊气味液体难溶有毒
乙醇:无色有特殊香味混溶易挥发
乙酸:无色刺激性气味易溶能挥发
二、 实验室制法
①:甲烷:CH3COONa + NaOH →(CaO,加热) → CH4↑+Na2CO3
注:无水醋酸钠:碱石灰=1:3
固固加热(同O2、NH3)
无水(不能用NaAc晶体)
CaO:吸水、稀释NaOH、不是催化剂
②:乙烯:C2H5OH →(浓H2SO4,170℃)→ CH2=CH2↑+H2O
注:V酒精:V浓硫酸=1:3(被脱水,混合液呈棕色)
排水收集(同Cl2、HCl)控温170℃(140℃:乙醚)
碱石灰除杂SO2、CO2
碎瓷片:防止暴沸
③:乙炔:CaC2 + 2H2O → C2H2↑ + Ca(OH)2
注:排水收集无除杂
不能用启普发生器
饱和NaCl:降低反应速率
导管口放棉花:防止微溶的Ca(OH)2泡沫堵塞导管
④:乙醇:CH2=CH2 + H2O →(催化剂,加热,加压)→CH3CH2OH
…… …… 余下全文
篇四 :高中化学有机物知识总结
高中化学有机物知识总结
一、有机代表物质的物理性质
1. 状态
固态:饱和高级脂肪酸、脂肪、TNT、萘、苯酚、葡萄糖、果糖、麦芽糖、淀粉、纤维素、醋(16.6℃
以下)
气态:C4以下的烷烃、烯烃、炔烃、甲醛、一氯甲烷
液态:油 状:硝基苯、溴乙烷、乙酸乙酯、油酸
粘稠状:石油、乙二醇、丙三醇
2. 气味
无味:甲烷、乙炔(常因混有PH3、H2S和AsH3而带有臭味))
稍有气味:乙烯 特殊气味:苯及苯的同系物、萘、石油、苯酚
刺激性:甲醛、甲酸、乙酸、乙醛
甜味:乙二醇(甘醇)、丙三醇(甘油)、蔗糖、葡萄糖
香味:乙醇、低级酯 苦杏仁味:硝基苯
3. 颜色
白色:葡萄糖、多糖 淡黄色:TNT、不纯的硝基苯 黑色或深棕色:石油
4. 密度
比水轻的:苯及苯的同系物、一氯代烃、乙醇、低级酯、汽油
比水重的:硝基苯、溴苯、乙二醇、丙三醇、CCl4、氯仿、溴代烃、碘代烃
5. 挥发性:乙醇、乙醛、乙酸
6. 升华性:萘、蒽
7. 水溶性: 不溶:高级脂肪酸、酯、硝基苯、溴苯、烷烃、烯烃、炔烃、苯及苯的同系物、萘、蒽、石油、卤代烃、TNT、氯仿、CCl4 能溶:苯酚(0℃时是微溶) 微溶:乙炔、苯甲酸 易溶:甲醛、乙酸、乙二醇、苯磺酸 与水混溶:乙醇、苯酚(65℃以上)、乙醛、甲酸、丙三醇
…… …… 余下全文
篇五 :高中化学有机物部分 总结
高二化学重要知识点总结
第三章烃的含氧衍生物
课标要求
1.了解醇、酚、醛、羧酸、酯的典型代表物的组成和结构特点以及它们的相互联系。
2.能列举事实说明有机分子中基团之间的相互影响。
3.结合实际了解某些有机物对环境和健康可能产生的影响,关注有机化合物的安全使用问题。
要点精讲
一、烃的衍生物性质对比
1.脂肪醇、芳香醇、酚的比较
![AC6]3HJ8YC04HQ}1K$1KA3J](https://upload2.fanwen118.com/wk001/2442353/2442353_img_001.jpg)
2.苯、甲苯、苯酚的分子结构及典型性质比较
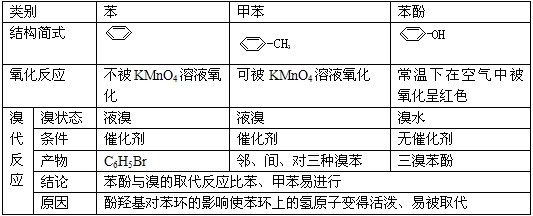
3.醛、羰酸、酯(油脂)的综合比较
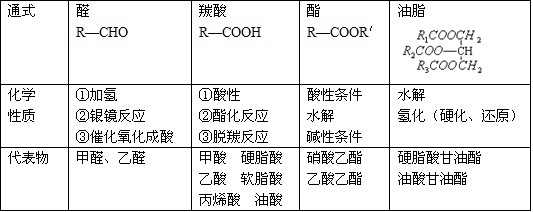
4.烃的羟基衍生物性质比较
![3BY)K`2`PC5TH8I459[NL]F](https://upload2.fanwen118.com/wk001/2442353/2442353_img_004.jpg)
5.烃的羰基衍生物性质比较
![(J)(95ZD%3`_NED]WSLE(1R](https://upload2.fanwen118.com/wk001/2442353/2442353_img_005.jpg)
6.酯化反应与中和反应的比较

7.烃的衍生物的比较
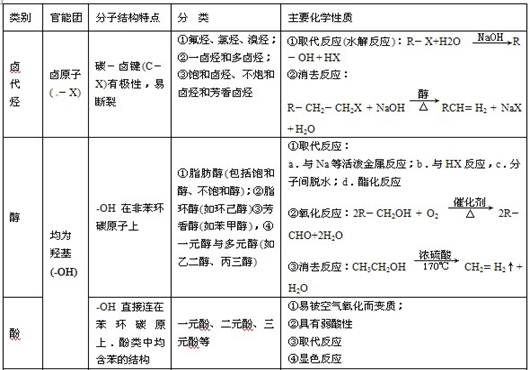
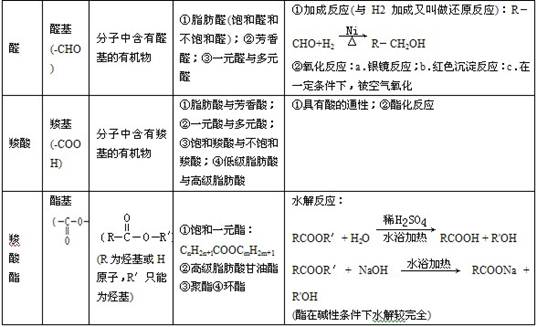
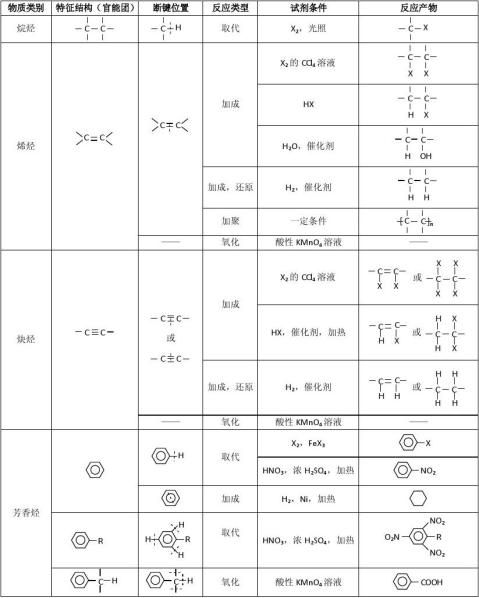
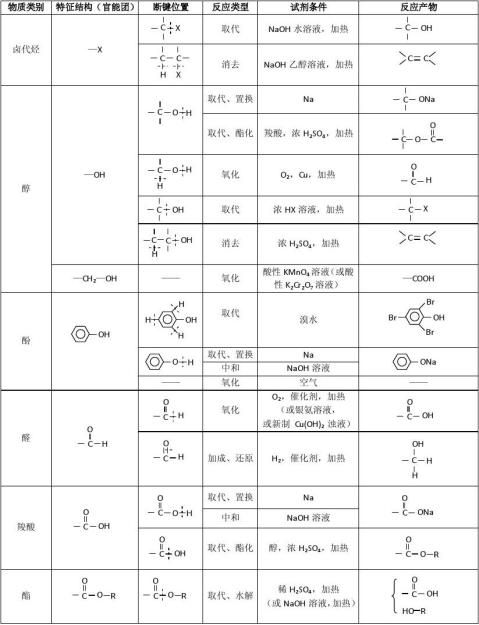
二、有机反应的主要类型
![6(X3EN)UNMH`BTZ)E@6]]CG](https://upload2.fanwen118.com/wk001/2442353/2442353_img_009.jpg)
三、烃及其重要衍生物之间的相互转化关系
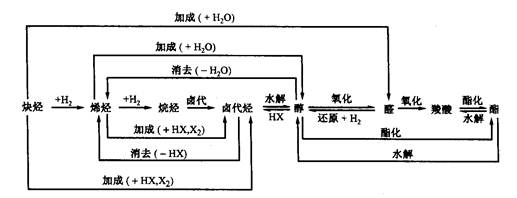
第四章生命中的基础有机物
课表要求
1.了解糖类的组成和性质特点,能举例说明糖类在食品加工和生物能源开发上的应用。
2.了解氨基酸的组成、结构特点和主要性质。了解氨基酸和人体健康的关系。
3.了解蛋白质的组成、结构和性质。
4.了解化学科学在生命科学发展中所起的重 要作用。
要作用。
要点精讲
一、糖类
1.糖类的结构:分子中含有多个羟基、醛基的多羟基醛,以及水解后能生成多羟基醛的由C、H、O组成的有机物。糖类根据其能否水解以及水解产物的多少,可分为单糖、二糖和多糖等。
…… …… 余下全文
篇六 :高中有机化学各物质特征反应总结
高中有机化学各物质特点总结
有机物的物理性质
1、状态:
固态:饱和高级脂肪酸、脂肪、葡萄糖、果糖、蔗糖、麦芽糖、淀粉、维
生素、醋酸(16.6℃以下);
气态:C4以下的烷、烯、炔烃、甲醛、一氯甲烷、新戊烷;
液态: 油状:乙酸乙酯、油酸;
粘稠状:石油、乙二醇、丙三醇。
2、气味:
无味:甲烷、乙炔(常因混有PH3、H2S和AsH3而带有臭味);
稍有气味:乙烯;
特殊气味:甲醛、乙醛、甲酸和乙酸;
香味:乙醇、低级酯;
3、颜色:
白色:葡萄糖、多糖
黑色或深棕色:石油
4、密度:
比水轻:苯、液态烃、一氯代烃、乙醇、乙醛、低级酯、汽油;
比水重:溴苯、乙二醇、丙三醇、CCl4。
5、挥发性:
乙醇、乙醛、乙酸。
6、水溶性:
不溶:高级脂肪酸、酯、溴苯、甲烷、乙烯、苯及同系物、石油、CCl4;
易溶:甲醛、乙酸、乙二醇;
能与溴水发生化学反应而使溴水褪色或变色的物质
1、有机物:
⑴ 不饱和烃(烯烃、炔烃、二烯烃等)
⑵ 不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等)
⑶ 石油产品(裂化气、裂解气、裂化汽油等)
…… …… 余下全文
篇八 :高中化学有机物知识总结
高中化学有机物知识总结
一、有机代表物质的物理性质
1. 状态
固态:饱和高级脂肪酸、脂肪、TNT、萘、苯酚、葡萄糖、果糖、麦芽糖、淀粉、
纤维素、醋(16.6℃以下)
气态:C4以下的烷烃、烯烃、炔烃、甲醛、一氯甲烷
液态:油 状:硝基苯、溴乙烷、乙酸乙酯、油酸
粘稠状:石油、乙二醇、丙三醇
2. 气味
无味:甲烷、乙炔(常因混有PH3、H2S和AsH3而带有臭味))
稍有气味:乙烯 特殊气味:苯及苯的同系物、萘、石油、苯酚 刺激性:甲醛、甲酸、乙酸、乙醛
甜味:乙二醇(甘醇)、丙三醇(甘油)、蔗糖、葡萄糖
香味:乙醇、低级酯 苦杏仁味:硝基苯
3. 颜色
白色:葡萄糖、多糖 淡黄色:TNT、不纯的硝基苯 黑色或深棕色:石油
4. 密度
比水轻的:苯及苯的同系物、一氯代烃、乙醇、低级酯、汽油
比水重的:硝基苯、溴苯、乙二醇、丙三醇、CCl4、氯仿、溴代烃、碘代烃
5. 挥发性:乙醇、乙醛、乙酸
6. 升华性:萘、蒽
7. 水溶性: 不溶:高级脂肪酸、酯、硝基苯、溴苯、烷烃、烯烃、炔烃、苯及苯的同系物、萘、蒽、石油、卤代烃、TNT、氯仿、CCl4 能溶:苯酚(0℃时是微溶) 微溶:乙炔、苯甲酸 易溶:甲醛、乙酸、乙二醇、苯磺酸 与水混溶:乙醇、苯酚(65℃以上)、乙醛、甲酸、丙三醇
…… …… 余下全文