篇一 :化学实验报告-氯化钠提纯
化学实验报告-氯化钠提纯
实验目的
1.通过沉淀反应,了解提纯氯化钠的方法;
2.练习台称和煤气灯的使用以及过滤、蒸发、结晶、干燥等基本操作。
实验原理
粗食盐中含有不溶性杂质(如泥沙)和可溶性杂质(主要是Ca2+、Mg2+、K+和SO42-)。
不溶性杂质,可用溶解和过滤的方法除去。
可溶性杂质可用下列方法除去:在粗食盐溶液中加入稍微过量的BaCl2溶液时,即可将SO42-转化为难溶解的BaSO4沉淀而除去:
Ba2++SO42- = BaSO4
将溶液过滤,除去BaSO4沉淀,再加入NaOH和Na2CO3溶液,由于发生下列反应:
Mg2++2OH- = Mg(OH)2
Ca2++CO32- = CaCO3
Ba2++ CO32- = BaCO3
食盐溶液中的杂质Mg2+、Ca2+以及沉淀SO42-时加入的过量Ba2+转化为难溶的Mg(OH)2,CaCO3,BaCO3沉淀,并通过过滤的方法除去。过量的NaOH和Na2CO3可以用纯盐酸中和除去。少量可溶性的杂质(如KCl)由于含量很少,在蒸发浓缩和结晶过程中仍留在溶液中,不会和NaCl同时结晶出来。
过程步骤
一、粗食盐的提纯
1.在台秤上,称取8g粗食盐,放入小烧杯中,加30ml蒸馏水,用玻璃棒搅动,并加热使其溶解。至溶液沸腾时,在搅动下一滴一滴加入1mol·dm-3BaCl2溶液至沉淀完全(约2ml),继续加热,使BaSO4颗粒长大易于沉淀和过滤。为了试验沉淀是否完全,可将烧杯从石棉网上取下,待沉淀沉降后,在上层清液中加入1-2滴BaCl2溶液,观察澄清液中是否还有混浊现象,如果无混浊现象,说明SO42-已完全沉淀。如果仍有混浊现象,则需继续滴加BaCl2溶液,直到上层清液在加入一滴BaCl2后,不再产生混浊现象为止。沉淀完全后,继续加热五分钟,以使沉淀颗粒长大而易于沉降,用普通漏斗过滤。
2.在滤液中加入1ml2mol·dm-3NaOH和3ml 1mol·dm-3Na2CO3溶液加热至沸。待沉淀沉降后,在上层清液中滴加1mol·dm-3Na2CO3溶液至不再产生沉淀为止,用普通漏斗过滤。
3.在滤液中还滴加入2mol·dm-3HCl,并用玻璃棒沾取滤液在pH试纸上试验,直到溶液呈微酸性为止(pH≈6)。
4.将溶液倒入蒸发皿中,用小火加热蒸发,浓缩至稀粥状的稠液为止,但切不可将溶液蒸发至干。
5.冷却后,用布氏漏斗过滤,尽量将结晶抽干。将结晶移入蒸发皿中,在石棉网上用小火加热干燥。
6.称出产品的质量,并计算产量百分率。
二、产品纯度的检验:取少量(约1g)提纯前和提纯后的食盐。分别用5ml蒸馏水溶解,然后各盛于三支试管中,组成三组,对照检验它们的纯度。
1.SO42-的检验:在第一组溶液中,分别加入2滴1mol·dm-3BaCl2溶液,比较沉淀产生的情况,在提纯的食盐溶液中应该无沉淀产生。
2.Ca2+的检验:在第二组溶液中,各加入2滴0.5mol·dm-3草酸铵(NH4)2C2O4溶液,在提纯的食盐溶液中应无白色难溶的草酸钙CaC2O4沉淀产生。
3.Mg2+的检验:在第三组溶液中,各加入2-3滴1mol·dm-3NaOH溶液,使溶液呈碱性(用pH试纸试验)再各加入2-3滴“镁试剂”,在提纯的食盐溶液中应无天蓝色沉淀产生。
镁试剂是一种有机染料,它在酸性溶液中呈黄色,在碱性溶液中呈红色或紫色,但被Mg(OH)2沉淀吸附后,则呈天蓝色,因此可以用来检验Mg2+的存在。
…… …… 余下全文
篇二 :无机化学实验八 氯化钠的提纯
实验八 氯化钠的提纯
一、实验目的
1.学会用化学方法提纯粗食盐,同时为进一步精制成试剂级纯度的氯化钠提供原料;
2.练习台秤的使用以及加热、溶解、常压过滤、减压过滤、蒸发浓缩、结晶、干燥等基本操作;
3.学习食盐中Ca2+、Mg2+、SO42-的定性检验方法。
二、实验原理
1.在粗盐中滴加BaCl2除去SO42-
Ba2++ SO42-= BaSO4↓
2.在滤液中滴加NaOH、Na2CO3除去Mg2+、Ca2+、Ba2+、Fe3+
Mg2++2OH-= Mg(OH)2↓ Ca2++CO32-= CaCO3↓
Ba2++CO32-= BaCO3↓ Fe3+ + 3OH - = Fe(OH)3↓
3.用HCl中和滤液中过量的OH-、CO32-
H+ + OH - = H2O
CO32- + 2H+ = CO2↑ + H2O
[教学重点]
常压过滤、减压过滤、蒸发(浓缩)、结晶等操作
[教学难点]
常压过滤、减压过滤、蒸发(浓缩)、结晶等操作
[实验用品]
仪器:烧杯、量筒、长颈漏斗、吸滤瓶、布氏漏斗、石棉网、泥三角、蒸发皿、
台秤、循环水真空泵
药品:1 mol?L-1Na2CO3、2 mol?L-1NaOH、2 mol?L-1HCl、1 mol?L-1BaCl2、
…… …… 余下全文
篇三 :氯化钠的提纯实验报告
山东师范大学化学化工与材料科学学院
实 验 报 告
实验题目 氯化钠的提纯 实验时间 指导教师 成绩
年级__ _专业 班 姓名 学号
[目的要求]
[实验原理]
[主要仪器设备]
[实验步骤]












…… …… 余下全文
篇四 :实验一 氯化钠的提纯
实验一 氯化钠的提纯
一、目的要求
1 、掌握提纯氯化钠的原理和方法。
2 、练习溶解、沉淀、减压过滤、蒸发浓缩、结晶和烘干等基本操作。
4 、了解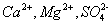 等离子的定性鉴定。
等离子的定性鉴定。
二、实验原理
化学试剂或医药用的氯化钠都是以粗食盐为原料提纯的。粗盐中含有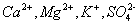 等可溶性杂质和泥沙等不溶杂质。选择适当的试剂可使
等可溶性杂质和泥沙等不溶杂质。选择适当的试剂可使 等离子生成沉淀而除去。一般是先在食盐溶液中加入
等离子生成沉淀而除去。一般是先在食盐溶液中加入 溶液,除去
溶液,除去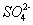 :
:
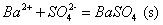
然后在溶液中加入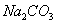 溶液,除去
溶液,除去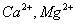 和过量的
和过量的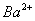
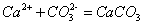


过量的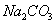 溶液用盐酸中和。粗食盐中的
溶液用盐酸中和。粗食盐中的 与这些沉淀剂不作用,仍留在溶液中。由于
与这些沉淀剂不作用,仍留在溶液中。由于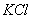 的溶解度比
的溶解度比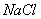 的大,而且在粗食盐中的含量较少,所以在蒸浓食盐溶液时,
的大,而且在粗食盐中的含量较少,所以在蒸浓食盐溶液时,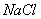 结晶出来,
结晶出来,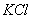 仍留在母液中。
仍留在母液中。
三、仪器与试剂
仪器:台称,普通漏斗,布氏漏斗,吸滤瓶,蒸发皿,烧杯(2只,100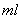 ),酒精灯,滤纸,玻璃棒,石棉网,火柴,循环水真空泵,
),酒精灯,滤纸,玻璃棒,石棉网,火柴,循环水真空泵,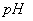 试纸坩埚钳,泥三角,小试管(多只)等
试纸坩埚钳,泥三角,小试管(多只)等
试剂: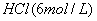 ,
,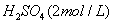 ,
, 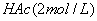 ,
,  ,
,  ,
,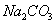 (饱和),
(饱和),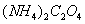 (饱和),镁试剂和粗食盐等。
(饱和),镁试剂和粗食盐等。
四、基本操作(补充内容)
1.固体溶解
2.固液分离
(1)倾析法
(2)过滤法
A常压过滤:滤纸的选择、漏斗、滤纸的折叠、过滤和转移、洗涤
B减压过滤
C热过滤
…… …… 余下全文
篇五 :粗盐制备分析纯氯化钠实验报告
粗盐制备分析纯氯化钠
一、实验题目:粗盐制备分析纯氯化钠
二、实验目的:1.巩固减压过滤,蒸发、浓缩等基本操作;
2.了解沉淀溶解平衡原理的应用;
3.学习在分离提纯物质过程中,定性检验Ca2+、Mg2+、SO42-等离子是否除尽。
三、实验原理:粗盐中,除含一些不溶性杂志,还含有Ca2+、Mg2+、SO42-和Fe3+等可溶性杂质,不溶性杂质可用过滤法出去,可溶性杂质中Ca2+、Mg2+、SO42-和Fe3+通过过滤的方法除去,然后蒸发水分得到较纯净的精盐。
1.BaCl2—NaOH,Na2CO3法
(1)除SO42-,加入BaCl2溶液
Ba2++SO42-=BaSO4
(2)除Ca2+、Mg2+、和Fe3+和过量的Ba2+,加入NaOH—Na2CO3
Ca2++CO32-=CaCO3 Ba2++CO32-=BaCO3 4Mg2++4CO32-+H2O=Mg(OH)2·3MgCO3
…… …… 余下全文
篇六 :普通化学实验--氯化钠的提纯 - 副本
普通化学实验要求:
实验前必须进行预习:
① 认真阅读实验教材、参考教材、资料中的有关内容。
② 明确本实验的目的和内容提要。
③ 掌握本实验的预备知识和实验关键。
④ 了解本实验的内容、步骤、操作和注意事项。
⑤ 写好简明扼要的预习报告后,方能进行实验,若发现预习不够充分,应停止实验,要求熟悉实验内容后再进行实验。
⑥ 预习报告必须书写在专用的的实验记录本上,内容包括:
一、实验目的
二、实验原理
三、实验关键
四、实验步骤(采用流程示意图简单明了地表示)
五、实验数据记录和数据处理(采用表格形式表示,在表格的左下端注明计算公式以及 采用的其他数据)。
六、思考题(必须做出解答)
2. 对实验的要求
① 认真操作,细心观察,如实记录,不得抄袭他人数据。实验中测量的原始数据必须记录在实验记录本上(附在预习报告后面),不得将数据记录在纸片上或其他地方,不得伪造和涂改原始数据。
② 认真阅读“实验室规则”和“实验室学生须知”,要遵守实验制度,养成良好的科学实验习惯,实验中保持肃静,遵守规则,注意安全,整洁节约。
③ 实验过程中应勤于思考,仔细分析,力争自己解决问题,遇到难以解决疑难问题时,可请教师指点。
…… …… 余下全文
篇八 :粗盐的提纯与溶液配制实验报告
《粗盐的提纯》实验报告
班级 姓名
实验目的:1。掌握溶解、过滤、蒸发等实验的操作技能
2.理解过滤法分离混合物的化学原理
3.体会过滤的原理在生活生等社会实际中的应用
实验操作:
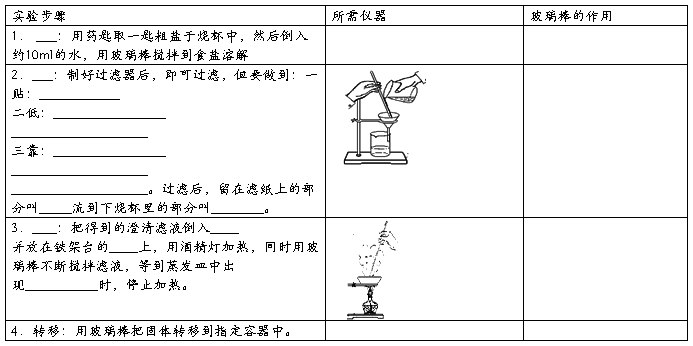
总结:该实验所需全部仪器有 。
二:交流与讨论:
…… …… 余下全文
