篇一 :实验二 溶液偏摩尔体积的测定实验报告 思考题 绘图
实验二 溶液偏摩尔体积的测定
一、实验目的
偏摩尔量是溶液中一个重要参数,有许多性质都与偏摩尔数量有关。本实验是测定溶液的偏摩尔体积。
1. 掌握用比重瓶测定溶液密度的方法;
2. 运用密度法测定指定组成的乙醇—水溶液中各组分的偏摩尔体积;
3. 学会恒温槽的使用。
4. 理解偏摩尔量的物理意义。
二、预习要求
1.复习课堂讲授内容,真正理解偏摩尔量的物理意义。
2.理解摩尔体积—摩尔分数图与比容—质量百分数图之间的关系。
三、实验原理
在多组分体系中,某组分i的偏摩尔体积定义为
??V?Vi,m?? (1) ???ni?T,p,nj(i?j)
若是二组分体系,则有
??V?V1,m?? (2) ??n?1?T,p,n2
??V?V2,m?? (3) ???n2?T,p,n1
体系总体积
V=n1V1,m+n2V2。m (4)
将(4)式两边同除以溶液质量W
…… …… 余下全文
篇二 :偏摩尔体积的测定

北京理工大学
物理化学实验报告
偏摩尔体积的测定
班级:09111101
实验日期:20##-4-23
一、 实验目的及要求
1) 配制不同浓度的NaCl水溶液,用密度瓶测定各溶液的密度。
2) 计算溶液中各组分的偏摩尔体积。
二、原理
设体系有二组分A,B,体系的总体积V是nA, nB、温度、压力的函数,即
V=f(nA ,nB,T,P)
组分A、B的偏摩尔体积定义为


吉布斯-杜亥姆(Gibbs-Duhem)方程如下:
nAdVA+nBdVB =0
…… …… 余下全文
篇三 :A偏摩尔体积的测定
偏摩尔体积测定实验报告
一、实验目的
1) 配制不同浓度的NaCl水溶液,测定各溶液的密度。
2) 计算溶液中各组分的偏摩尔体积。
3) 学习用比重管测定液体的密度。
二、实验原理
根据热力学概念,体系的体积V为广度性质,其偏摩尔量则为强度性质。设体系有二组分A,B,体系的总体积V是nA, nB、温度、压力的函数,即
V=f(nA ,nB,T,P) (C9.1)
组分A、B的偏摩尔体积定义为
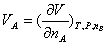
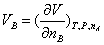 (C9.2)
(C9.2)
在恒定温度和压力下
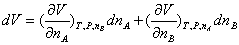 (C9.3)
(C9.3)
dV=VAdnA + VBdnB (C9.4)
…… …… 余下全文
篇四 :溶液偏摩尔体积测定实验报告思考题
1、使用比重瓶应注意哪些问题?
答:(1)拿比重瓶时应手持其颈部;
(2)比重瓶加满溶液后,瓶内及塞子上的毛细管要不能有气泡产生;
(3)称量前必须用滤纸把比重瓶的外表面擦干净,然后再放到天平上称量。
2、如何使用比重瓶测量颗粒状固体物的密度?
答:(1)将比重瓶洗净干燥,装入一定量的研细的待测固体(装入量视瓶大小而定),称量记为m1。(2)再向瓶中注入部分已知密度为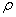 的液体,将瓶敞口放入真空干燥器内,用真空泵抽气约10min,将吸附在固体表面的空气全部除去。然后向瓶中注满液体,塞上塞子。恒温(t℃)10min后,取出比重瓶擦干外壁,并用滤纸吸去塞帽毛细管口溢出的液体,称重为m1’。(3)增加加入待测固体的量,重复步骤(1)(2),并记装入固体后称重为m2,装满液体恒温后称重为m2’。(4)根据下述公式计算待测固体的密度ρs。
的液体,将瓶敞口放入真空干燥器内,用真空泵抽气约10min,将吸附在固体表面的空气全部除去。然后向瓶中注满液体,塞上塞子。恒温(t℃)10min后,取出比重瓶擦干外壁,并用滤纸吸去塞帽毛细管口溢出的液体,称重为m1’。(3)增加加入待测固体的量,重复步骤(1)(2),并记装入固体后称重为m2,装满液体恒温后称重为m2’。(4)根据下述公式计算待测固体的密度ρs。

3、为提高溶液密度测量精度,可作哪些改进?
答:(1)准确称量以计算溶液的质量分数;
(2)多次测量同一组成溶液的质量,结果取其平均值;
(3)每次称量瓶都要烘干;
(4)动作要敏捷,以减少挥发引起的误差。
…… …… 余下全文
篇五 :刘志超__溶液偏摩尔体积的测定实验报告
实验二 溶液偏摩尔体积的测定
一、实验目的
偏摩尔量是溶液中一个重要参数,有许多性质都与偏摩尔数量有关。本实验是测定溶液的偏摩尔体积。
1. 运用密度法测定指定组成的乙醇—水溶液中各组分的偏摩尔体积;
2. 掌握用比重瓶测定溶液密度的方法;
二、实验原理
在多组分体系中,某组分i的偏摩尔体积定义为
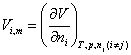 (1)
(1)
若是二组分体系,则有
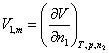 (2)
(2)
…… …… 余下全文
篇六 :溶液偏摩尔体积的测定
物理化学实验报告
实验名称:溶液偏摩尔体积的测定
实验日期:
院 系:机械工程学院
专 业:冶金工程(有色金属方向)
学 号:
姓 名:
一、实验目的
1. 掌握用比重瓶测定溶液密度的方法;
2. 运用密度法测定指定组成的乙醇—水溶液中各组分的偏摩尔体积;
3. 学会恒温槽的使用;
4. 理解偏摩尔量的物理意义。
二、实验原理
在多组分体系中,某组分i的偏摩尔体积定义为
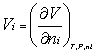 (1)
(1)
…… …… 余下全文
篇七 :无机化学实验第四版置换法测定镁的摩尔质量实验报告
实验名称:置换法测定镁的摩尔质量
实验日期: 温度: 气压:
一、实验目的
1.了解置换法测定镁的相对原子质量的原理和方法
2.掌握气态方程和分压定律的有关的计算
3.练习使用量气管和气压计
二、实验原理
1.在一定的温度T和压力P下,一定质量m的镁与足量的稀硫酸反应,可置换出一定体积y的氢气(含水蒸汽) Mg+H2SO4===MgSO4+H2
常压下的氢气可近似看作理想气体,根据气体状态方程和化学方程式,则有:
PH2V=nH2RT=(m/M)RT R为常数 R=8.314 R的单位Pa*m3/mol*K T=(t+273)K
根据分压定律:PH2=P-PH2O,(我们所需的是氢气的压力,但是我们不能直接得到,所以我们通过大气的压力减去水蒸汽的压力便是我们想得到的氢气压力)
整理后可得:M=mRT/[(P-PH2O)]V
三、实验内容
1.用砂纸将镁条打光,清除掉表面氧化物膜,截取一段,在电子天平上准确称其质量。
2.装配好仪器,由漏斗注水至近于量气管刻度“0”的位置,上下移动漏斗以驱赶量气管与橡皮管内的气泡。
3.检查装置是否漏气,将各连接处的橡皮塞塞紧,把漏斗下移适当的距离固定,如果连气管内的液面只在开始时稍有下降,以后维持恒定,经3至5分钟不变,可判断装置不漏气。
…… …… 余下全文
篇八 :测定气体摩尔体积实验误差的原因分析
资源信息表

10.1 测定1mol气体的体积(共3+1课时)
第4课时 测定1mol气体体积实验误差的原因分析
[设计思想]
任何定量测定的方法,得到的数据都有一定的精确范围,或者说存在一定的误差。定量实验必须尽可能减小实验误差,提高实验精确度。本节课的教学围绕实验中如何实现这一要求?展开教学讨论,让学生认识实验误差的来源:一是仪器装置精密度和药品试剂的品质;二是操作的失误。围绕着误差的来源,结合自己的实验,分析产生各种误差的原因,获得减小实验误差的方法。在讨论减小实验误差,提高实验精确度的方法、措施时,从以下几个方面展开:(1)根据实验要求和条件精选精度比较高的计量仪器(如量体积时,尽可能用滴定管或移液管);(2)进行重复测量。计算时取两次(或多次)可测量值之间的平均值;(3)准确规范操作。如读数液体体积时,视线应该与管中的凹液面最低处相切等。最后让学生归纳出:定量实验存在误差是一定的、允许的,重要的是误差要控制在合理的范围内,本实验误差值在-2—+2%。
一.教学目标
1.知识与技能
(1)实验误差分析(B)。
(2)实验报告的书写(B)。
2.过程与方法
…… …… 余下全文