篇一 :化学反应热效应的测定
化学反应热效应的测定
一、实验目的
1.学会测定化学反应热效应的一般原理和方法,测定锌与硫酸铜反应的热效应。
2.学习准确浓度溶液的配制方法。
3.掌握利用外推法校正温度改变值的作图方法。
二、实验原理
对一化学反应,当生成物的温度与反应物的温度相同,且在反应过程中除膨胀功以外不做其它功时,该化学反应所吸收或放出的热量,称为化学反应热效应。若反应是在恒压条件下进行的,则反应的热效应称为恒压热效应Qp,且此热效应全部增加体系的焓(ΔH),所以有
ΔH = Qp
式中ΔH为该反应的焓变。对于放热反应ΔrHm为负值,对于吸热反应ΔrHm为正值。
例如,在恒压条件下,1mol锌置换硫酸铜溶液中的铜离子时,放出216.8 kJ的热量,即
Zn + CuSO4 = ZnSO4 + Cu ΔrHm=–216.8 kJ·mol-1
测定化学反应热效应的基本原理是能量守恒定律,即反应所放出的热量促使反应体系温度的升高。因此,对上面的反应,其热效应与溶液的质量(m)、溶液的比热(c)和反应前后体系温度的变化(ΔT )有如下关系
…… …… 余下全文
篇二 :化学反应热效应的测定实验
化学反应热效应的测定实验
一、实验要求
⒈学会测定化学反应热效应的一般原理和方法,测定锌与硫酸铜反应的热效应。
⒉学习准确浓度溶液的配制方法。
⒊掌握利用外推法校正温度改变值的作图方法。
二、实验原理
对一化学反应,当生成物的温度与反应物的温度相同,且在反应过程中除膨胀功以外不做其它功时,该化学反应所吸收或放出的热量,称为化学反应热效应。若反应是在恒压条件下进行的,则反应的热效应称为恒压热效应Qp,且此热效应全部增加体系的焓(ΔH),所以有
ΔH = Qp
式中ΔH为该反应的焓变。对于放热反应ΔrHm为负值,对于吸热反应ΔrHm为正值。
例如,在恒压条件下,1mol锌置换硫酸铜溶液中的铜离子时,放出216.8 kJ的热量,即
Zn + CuSO4 = ZnSO4 + Cu ΔrHm=–216.8 kJ·mol-1
测定化学反应热效应的基本原理是能量守恒定律,即反应所放出的热量促使反应体系温度的升高。因此,对上面的反应,其热效应与溶液的质量(m)、溶液的比热(c)和反应前后体系温度的变化(ΔT )有如下关系
…… …… 余下全文
篇三 :化学反应焓变的测定实验报告正文
化学反应焓变的测定
摘要:化学反应都伴随着能量的转移,而焓变就是能量转移的重要表现形式。因此,化学反应焓变的测定就成为我们学习化学知识、掌握化学反应原理、控制反应进行程度的重要手段。本次实验利用常见的保温杯等装置简易测定了Zn与CuSO4的化学反应焓变。结果表明:该实验测量效果好,操作简洁,易于观察实验现象
关键词:焓变;测定;Zn;CuSO4;保温杯;温度计
化学反应焓变的测定
化学反应过程中,除了发生物质的变化外,常伴有能量的变化,这种能量变化表现为反应热效率,而恒压条件下的反应热效应叫做等压热效应。在标准状态下的焓变成为化学反应的标准焓变。本实验采用普通保温杯和精密温度计作为简易量热计来测量。
在298.15K和标准条件下,1mol锌置换硫酸铜中的铜离子,放出218.7J的热量。
Zn+CuSO4=ZnSO4+Cu △rHm=-218.7KJ/mol
有溶液反应前后的温度变化,可求得上述反应的焓变。
考虑到热量计的热容,则反应放出的热量Qp等于系统中溶液吸收的热量与热量计吸收的热量之和:Qp=(c.m+Cp) △T
c--------溶液的比热容(取4.18)
m--------溶液的质量(近似等于溶剂的质量)
…… …… 余下全文
篇四 :实验七化学反应热效应的测定
实验七 化学反应热效应的测定
一、实验目的:
1、学会测定化学反应热效应的一般原理和方法,测定锌与硫酸铜反应的热效应。
2、学习准确浓度溶液的配制方法。
3、掌握利用外推法校正温度改变值的作图方法。
二、实验原理
对一化学反应,当生成物的温度与反应物的温度相同,且在反应过程中除膨胀功以外不做其它功时,该化学反应所吸收或放出的热量,称为化学反应热效应。若反应是在恒压条件下进行的,则反应的热效应称为恒压热效应Qp,且此热效应
全部增加体系的焓(ΔH),所以有
ΔH = Qp
式中ΔH为该反应的焓变。对于放热反应ΔrHm为负值,对于吸热反应ΔrHm为正值。
例如,在恒压条件下,1mol锌置换硫酸铜溶液中的铜离子时,放出216.8 kJ的热量,即
Zn + CuSO4 = ZnSO4 + Cu ΔrHm=–216.8 kJ·mol-1 测定化学反应热效应的基本原理是能量守恒定律,即反应所放出的热量促使反应体系温度的升高。因此,对上面的反应,其热效应与溶液的质量(m)、溶液的比热(c)和反应前后体系温度的变化(ΔT )有如下关系
Qp = - (cmΔT+KΔT)
式中K为热量计的热容量,即热量计本身每升温1度所吸收的热量。 由溶液的密度(d)和体积(V)可得溶液的质量,即
…… …… 余下全文
篇五 :中和反应反应热的测定实验报告
中和反应反应热的测定
定义:在稀溶液中,酸和碱发生中和反应,生成1mol水时的反应热,叫中和热。
一、实验目的
测定强酸与强碱反应的反应热。(热效应)
二、实验用品
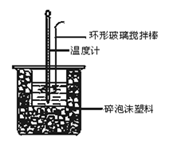
大烧杯(500 mL)、小烧杯(100 mL)、温度计、量筒(50mL)两个、泡沫塑料或纸条、泡沫塑料板或纸条、泡沫塑料板或硬纸板(中心有两个小孔)、环形玻璃搅拌棒。
0.50 mol/L 盐酸、0.55 mol/L NaOH溶液。
 三、实验步骤
三、实验步骤
1.在大烧杯底垫泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平。然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过,以达到保温、隔热、减少实验过程中热量损失的目的,如图所示。该实验也可在保温杯中进行。
2.用一个量筒量取50mL0.50mol/L盐酸,倒入小烧杯中,并用温度计测量盐酸的温度,记入下表。然后把温度计上的酸用水冲洗干净。
3.用另一个量筒量取50mL 0.55 mol/L NaOH溶液,并用温度计测量NaOH溶液的温度,记入下表。
…… …… 余下全文
篇六 :化学反应速率与活化能的测定实验报告
化学反应速率与活化能的测定
(实验报告及数据处理)
实验目的
1.了解浓度、温度及催化剂对化学反应速率的影响。
2.测定(NH4)2S2O8与KI反应的速率、反应级数、速率系数和反应的活化能。
实验原理
(NH4)2S2O8和KI在水溶液中发生如下反应:
S2O82-(aq)+ 3I-(aq) = 2SO42- (aq)+ I3-(aq) (1)
这个反应的平均反应速率为
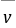 = -
= - 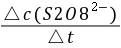 =
= 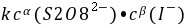 式中:
式中: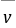 ── 反应的平均反应速率;
── 反应的平均反应速率;
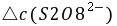 ──
── 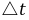 时间内
时间内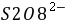 的浓度变化;
的浓度变化;
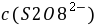 ,
,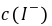 ──
── 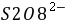 ,
,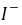 的起始浓度;
的起始浓度;
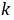 ── 该反应的速率系数;
── 该反应的速率系数;
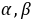 ──反应物
──反应物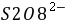 ,
,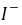 的反应级数,
的反应级数,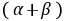 为该反应的总级数。
为该反应的总级数。
为了测出在一定时间(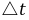 )内S2O82-的浓度变化,在混合(NH4)2S2O8和KI溶液的同时,加入一定体积的已知浓度的Na2S2O3溶液和淀粉,这样在反应(1)进行的同时,还有以下反应发生:
)内S2O82-的浓度变化,在混合(NH4)2S2O8和KI溶液的同时,加入一定体积的已知浓度的Na2S2O3溶液和淀粉,这样在反应(1)进行的同时,还有以下反应发生:
2S2O32- (aq) + I3-(aq) ══ S4O62-(aq) + 3I-(aq) (2)
由于反应(2)的速率比反应(1)的大得多,由反应(1)生成的I3-会立即与S2O32-反应生成无色的S4O62-和I-。这就是说,在反应开始的一段时间内,溶液呈无色,但当Na2S2O3一旦耗尽,由反应(1)生成的微量I3-就会立即与淀粉作用,使溶液呈蓝色。
…… …… 余下全文
篇八 :化学反应速率与活化能的测定实验报告
化学反应速率与活化能的测定实验报告
姓名 班级 试验时间
第 室 号位 指导教师
实验目的
1. 了解浓度、温度及催化剂对化学反应速率的影响。
2. 测定(NH4)2S2O8与KI反应的速率、反应级数、速率系数和反应的活化能。
实验原理
(NH4)2S2O8和KI在水溶液中发生如下反应:
S2O82-(aq)+ 3I-(aq) = 2SO42- (aq)+ I3-(aq) (1)
这个反应的平均反应速率为
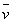 = -
= - 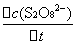 =
= 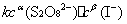
式中: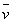 ── 反应的平均反应速率;
── 反应的平均反应速率;
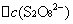 ──
── 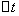 时间内
时间内 的浓度变化;
的浓度变化;
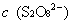 ,
,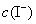 ──
──  ,
,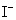 的起始浓度;
的起始浓度;
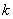 ── 该反应的速率系数;
── 该反应的速率系数;
…… …… 余下全文
