篇一 :对硝基苯甲酸的制备
对硝基苯甲酸的制备(预习报告)
一、实验目的
1、掌握利用对硝基甲苯制备对硝基苯甲酸的原理及方法。
2、掌握电动搅拌装置的安装及使用。
3、练习并掌握固体酸性产品的纯化方法。
二、实验原理
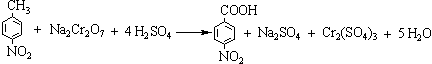
该反应为两相反应,还要不断滴加浓硫酸,为了增加两相的接触面,为了尽可能使其迅速均匀地混合,以避免因局部过浓、过热而导致其它副反应的发生或有机物的分解,本实验采用电动搅拌装置。这样不但可以较好地控制反应温度,同时也能缩短反应时间和提高产率。
生成的粗产品为酸性固体物质,可通过加碱溶解、再酸化的办法来纯化。纯化的产品用蒸汽浴干燥。
三、实验药品用量及物理常数
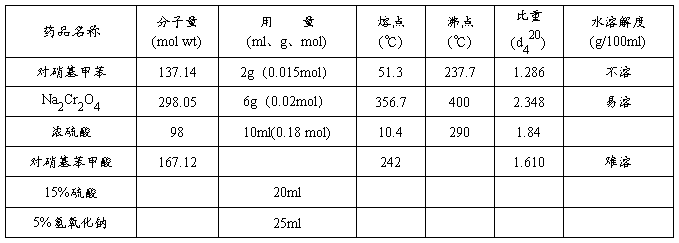
四、实验装置图
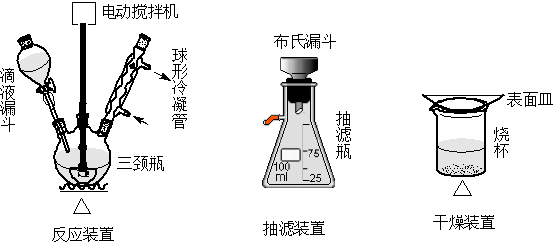
五、实验流程及步骤
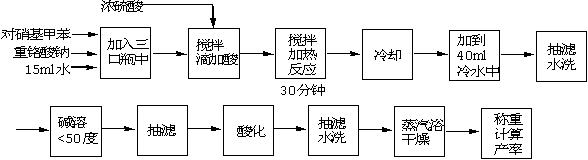
1. 安装带搅拌、回流、滴液的装置如图
2. 在250ml的三颈瓶中依次加入6g对硝基甲苯,18g重铬酸钾粉末及40ml水。
3. 在搅拌下自滴液漏斗滴入25ml浓硫酸。(注意用冷水冷却,以免对硝基甲苯因温度过高挥发而凝结在冷凝管上)。
4. 硫酸滴完后,加热回流0.5h,反应液呈黑色。(此过程中,冷凝管可能会有白色的对硝基甲苯析出,可适当关小冷凝水,使其熔融滴下)。
…… …… 余下全文
篇二 :苯佐卡因实验报告二:对硝基苯甲酸乙酯的制备(酯化)
苯佐卡因实验报告二:对硝基苯甲酸乙酯的制备(酯化)
对硝基苯甲酸乙酯的制备
一、实验目的
1. 掌握利用对硝基苯甲酸制备对硝基苯甲酸乙酯的原理及方法。
2. 熟练掌握回流、抽滤、重结晶、干燥等过程的操作。
3. 练习并掌握酯的纯化方法。
 二、实验原理
二、实验原理
M 167.12 195.17
m.p.(℃) 147~148 57
…… …… 余下全文
篇三 :苯甲酸乙酯的制备实验报告
苯甲酸乙酯的制备
班级: 姓名: 学号:
摘要:
苯甲酸乙酯(C9H10O2)为无色透明液体,其能与乙醇、乙醚、环己烷混溶,不溶于水,用于配制香水香精和人造精油等。本实验将用苯甲酸酯化制取苯甲酸乙酯,再取适量样品做鉴定实验。
关键词:
苯甲酸乙酯的制备 酯化反应 样品鉴定
前言:
苯甲酸乙酯(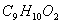 )稍有水果气味,密度1.068g/ml,用于配制香水香精和人造精油;也大量用于食品中,也可用作有机合成中间体、溶剂如纤维素酯、纤维素醚、树脂等。本实验利用酯化反应法制备,直接从苯甲酸→苯甲酸乙酯。实验原理:直接酸催化酯化反应是经典的制备酯的方法,但反应是可逆反应,反应物间建立如下平衡:既然反应可逆,为提高酯的转化率,使用过量乙醇或将反应生成的水从反应混合物中除去,都可以使平衡向生成酯的方向移动。另外,使用大大过量的强酸催化剂,水转化成它的共轭酸H3O+, 没有亲核性,也可抑制逆反应的发生。
)稍有水果气味,密度1.068g/ml,用于配制香水香精和人造精油;也大量用于食品中,也可用作有机合成中间体、溶剂如纤维素酯、纤维素醚、树脂等。本实验利用酯化反应法制备,直接从苯甲酸→苯甲酸乙酯。实验原理:直接酸催化酯化反应是经典的制备酯的方法,但反应是可逆反应,反应物间建立如下平衡:既然反应可逆,为提高酯的转化率,使用过量乙醇或将反应生成的水从反应混合物中除去,都可以使平衡向生成酯的方向移动。另外,使用大大过量的强酸催化剂,水转化成它的共轭酸H3O+, 没有亲核性,也可抑制逆反应的发生。

实验部分:
1、实验仪器及试剂:
仪器:分水回流装置、烧杯、加热套、玻璃棒、分液漏斗、圆底烧瓶、冷凝管、蒸馏装置一套
药品:苯甲酸4.0g 无水乙醇10.00ml 2.00ml浓硫酸 Na2CO3固体 无水硫酸镁 环己烷7.50ml 石油醚
…… …… 余下全文
篇四 :对硝基苯甲酸的还原实验设计报告2
实验设计报告
一.实验目的
1. 通过对硝基苯甲酸的还原,了解有机合成的基本过程;
2. 掌握还原反应的原理及基本操作;
3. 由对硝基苯甲酸制备对氨基苯甲酸。
二.实验原理
金属还原法,尤其铁粉还原法适用面广、操作简单、还原效率高、选择性好、产品质量好,尤其对品质有特殊要求的芳胺的制备,仍有优越性。适宜于采用铁粉还原法生产的胺类有:①容易被水蒸气蒸出的芳胺;②易溶于水,并且可以通过蒸馏分离的芳胺;③能溶于热水的芳胺;④含磺酸基或羧酸基等水溶性基团的芳胺。
COOHCOONH4
NO2NH2
三.实验试剂
对硝基苯甲酸,锡粉,浓盐酸,氨水,冰醋酸
四.实验仪器
三口烧瓶(250ml),电子天平,四口烧瓶(1000ml),球形冷凝管,器械搅拌装置,
油浴加热装置,布氏漏斗,抽滤瓶,水泵,玻璃棒,烧杯
五.实验方案
在100ml单颈烧瓶中加入4g对硝基苯甲酸,8g锡粉,20ml浓盐酸,用加热搅拌装置和温度控制装置回流加热回流。大约半小时后,对硝基苯甲酸和大部分锡粉都反应掉,溶液基本上呈透明状。稍冷后,把反应液倒入烧杯中,慢慢滴加浓氨水,直至PH=8。这时有氢氧化锡沉淀产生,抽滤,沉淀用少量蒸馏水洗涤。在得到的滤液中慢慢滴加冰醋酸,直至PH到6,这时有白色晶体产生。用冰醋酸进行冷却,抽滤,即得白色的对氨基苯甲酸晶体,量大约在2.5g左右,产率约为76%。
…… …… 余下全文
篇五 :对硝基苯甲酸的还原实验操作报告
实验操作报告 (对硝基苯甲酸制对氨基苯甲酸)
一.实验目的
1. 通过对硝基苯甲酸的还原,了解有机合成的基本过程;
2. 掌握还原反应的原理及基本操作;
3. 由对硝基苯甲酸制备对氨基苯甲酸;
4. 熟悉有机合成中的重结晶,抽滤,熔点测定等操作。
二.实验仪器
三口烧瓶(250ml),电子天平,四口烧瓶(1000ml),球形冷凝管,器械搅拌装置,油浴加热装置,布氏漏斗,抽滤瓶,水泵,玻璃棒,烧杯
三.实验试剂
对硝基苯甲酸,锡粉,浓盐酸,氨水,冰醋酸
第一次实验
1.实验过程
在操作台上搭制油浴加热装置,电动搅拌装置,回流加热装置
①在250ml三口烧瓶中加入4g对硝基苯甲酸,8g锡粉和20ml浓盐酸。
②盖上活塞,打开电动搅拌装置、油浴加热装置的电源,通冷凝水。开始搅拌加热,设定回流温度95℃.
③大约半小时后,反应液变澄清。
④停止反应,稍冷,把反应液倒入烧杯中,慢慢滴加浓氨水。开始时有悬浮状沉淀产生,到PH接近8时呈白色均匀沉淀,停止滴加。抽滤,沉淀用少量蒸馏水洗涤。
⑤在得到的滤液中慢慢滴加冰醋酸至PH=5,有白色晶体产生,用冰水浴冷却,抽滤,即得白色的对氨基苯甲酸晶体。用电子天平称量产物质量,m=0.4g。用熔点仪测定产物熔点,为184℃.
…… …… 余下全文
篇六 :对硝基苯甲酸的制备
八、对硝基苯甲酸的制备
一、实验目的
1. 进一步了解苯环侧链氧化反应的原理和方法
2. 了解机械搅拌的用途,并学习其安装和使用方法
3. 熟练掌握回流,抽滤、重结晶等过程的操作
二、反应式
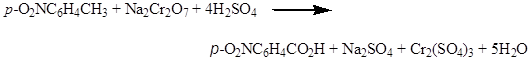
三、主要物料物理常数

四、主要试剂用量及规格
对硝基甲苯6g(0.04mol),重铬酸钾18g(0.06mol);
浓硫酸,15%硫酸溶液,5%氢氧化钠溶液
五、操作步骤
1. 安装带搅拌、回流、滴液的装置如图P16图1.9
2. 在250ml的三颈瓶中依次加入6g对硝基甲苯,18g重铬酸钾粉末及40ml水。
3. 在搅拌下自滴液漏斗滴入25ml浓硫酸。(注意用冷水冷却,以免对硝基甲苯因温度过高挥发而凝结在冷凝管上)。
4. 硫酸滴完后,加热回流0.5h,反应液呈黑色。(此过程中,冷凝管可能会有白色的对硝基甲苯析出,可适当关小冷凝水,使其熔融滴下)。
5. 待反应物冷却后,搅拌下加入80ml冰水,有沉淀析出,抽滤并用50ml水分两次洗涤。
6. 将洗涤后的对硝基苯甲酸的黑色固体放入盛有30ml 5%硫酸中,沸水浴上加热10min,冷却后抽滤。(目的是为了除去未反应完的铬盐)
…… …… 余下全文
篇七 :对硝基苯甲酸的制备
对硝基苯甲酸的制备
一、实验目的:
1. 掌握利用对硝基甲苯制备对硝基苯甲酸的原理及方法。
2. 熟练掌握回流、抽滤、重结晶等过程的操作。
3. 练习并掌握固体酸性产品的纯化方法。
二、实验原理:
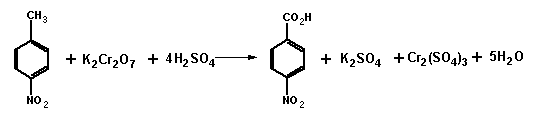
M 137.14 167.12
b.p.(℃) 238.3
m.p.(℃) 54.5 147~148
…… …… 余下全文
篇八 :对硝基苯甲酸的制备
对硝基苯甲酸的制备
一、实验目的
1、掌握利用对硝基甲苯制备对硝基苯甲酸的原理及方法。 2、掌握电动搅拌装置的安装及使用。 3、练习并掌握固体酸性产品的纯化方法。
二、实验原理
3
+
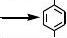
Na2Cr2O7+4H2SO42
2+Na2SO4+Cr2(SO4)3+5H2O
该反应为两相反应,还要不断滴加浓硫酸,为了增加两相的接触面,为了尽可能使其迅速均匀地混合,以避免因局部过浓、过热而导致其它副反应的发生或有机物的分解,本实验采用电动搅拌装置。这样不但可以较好地控制反应温度,同时也能缩短反应时间和提高产率。 生成的粗产品为酸性固体物质,可通过加碱溶解、再酸化的办法来纯化。纯化的产品用蒸汽浴干燥。
三、实验药品用量及物理常数
四、实验装置图

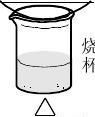
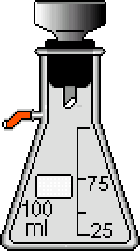
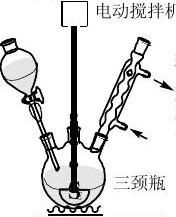
布氏漏斗
抽滤瓶
反应装置
抽滤装置
干燥装置
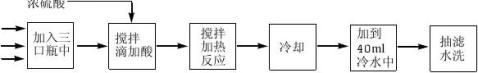
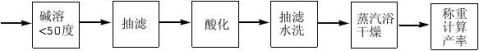
五、实验流程图
重铬酸钠15ml
六、实验注意事项
1、安装仪器前,要先检查电动搅拌装置转动是否正常,搅拌棒要垂直安装,安装好仪器后,再检查转动是否正常。
2、从滴加浓硫酸开始,整个反应过程中,一致保持搅拌。
3、滴加浓硫酸时,只搅拌,不加热;加浓硫酸的速度不能太快,否则会引起剧烈反应。 4、转入到40ml冷水中后,可用少量(约10ml)冷水再洗涤烧瓶。
…… …… 余下全文