篇一 :电导的测定及其应用实验报告wqf
宁 波 工 程 学 院
物理化学实验报告
专业班级 姓名 序号 同组姓名 指导老师 实验日期 3月31号
实验名称 实验五 电导的测定及其应用
一、实验目的
1、测量KCl水溶液的电导率,求算它的无限稀释摩尔电导率。
2、用电导法测量醋酸在水溶液中的解离平衡常数。
…… …… 余下全文
篇二 :电导率实验报告20xx
受控编号:ZHJC/GL021 No:
实验报告
监 测 项 目: 电导率
监测分析方法: 便携式电导率仪法
郑州市环境保护监测中心站
20##年 2 月 1 日
监测科室:现场监测室
实验人员:
审核人员:
电导率的测定
本方法采用便携式电导率仪法(B)《水和废水监测分析方法》国家环境保护总局 20##年 第四版。
…… …… 余下全文
篇三 :电导的测定及应用实验报告
实验名称 电导的测定及其应用
一、实验目的
1.测量KCl水溶液的电导率,求算它的无限稀释摩尔电导率;
2.用电导法测量醋酸在水溶液中的解离平衡常数;
3.掌握恒温水槽及电导率仪的使用方法。
二、实验原理
 1、电导G:对于电解质溶液,常用电导表示其导电能力的大小。电导G是电阻R的倒数,即 G=1/R。电导的单位是西门子,常用S表示。1S=1Ω-1
1、电导G:对于电解质溶液,常用电导表示其导电能力的大小。电导G是电阻R的倒数,即 G=1/R。电导的单位是西门子,常用S表示。1S=1Ω-1
2、电导率或比电导:κ=Gl/A (2.5.1)
其意义是电极面积为及1m2、电极间距为lm的立方体导体的电导,单位为S·m-1。
…… …… 余下全文
篇四 :电导的测定及其应用实验报告
电导的测定及其应用
一、实验目的
1、测量KCl水溶液的电导率,求算它的无限稀释摩尔电导率。
2、用电导法测量醋酸在水溶液中的解离平衡常数。
3、掌握恒温水槽及电导率仪的使用方法。
二、实验原理
1、电导G可表示为: 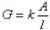 (1)
(1)
式中,k为电导率,电极间距离为l,电极面积为A,l/A为电导池常数Kcell,单位为m-1。
本实验是用一种已知电导率值的溶液先求出Kcell,然后把欲测溶液放入该电导池测出其电导值G,根据(1)式求出电导率k。
摩尔电导率与电导率的关系: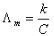 (2)
(2)
…… …… 余下全文
篇五 :电导的测定及其应用实验报告
电导的测定及其应用
一、实验目的
1、测量KCl水溶液的电导率,求算它的无限稀释摩尔电导率。
2、用电导法测量醋酸在水溶液中的解离平衡常数。
3、掌握恒温水槽及电导率仪的使用方法。
二、实验原理
1、电导G可表示为:  (1)
(1)
式中,k为电导率,电极间距离为l,电极面积为A,l/A为电导池常数Kcell,单位为m-1。
本实验是用一种已知电导率值的溶液先求出Kcell,然后把欲测溶液放入该电导池测出其电导值G,根据(1)式求出电导率k。
摩尔电导率与电导率的关系: (2)
(2)
…… …… 余下全文
篇六 :电导的测定及其应用实验报告
根据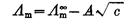 ,截距即为
,截距即为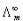 ,得
,得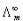 =154*10-4 S·m2·mol-1
=154*10-4 S·m2·mol-1
k = k’- kH2O
uS.cm-1=10-4S·m-1
CHAc=0.1127 mol·dm-3=112.7 mol·m-3
kH2O =7*10-4S·m-1
k(HAc测量)=560*10-4 S·m-1 k(HAc)= k(HAc测量)- kH2O=553*10-4 S·m-1
Λm=553*10-4/112.7=4.91*10-4 S·m2·mol-1
Λm -1=2.04*103 S-1·m-2·mol C =k=553*10-4 S·m-1
=k=553*10-4 S·m-1
α=4.91*10-4/3.907*10-2=0.0126
…… …… 余下全文
篇七 :电导的测定及应用实验报告
气温:24.3℃ 气压:70.28Kpa




以KCl溶液的Λm对 作图得一直线,其截距即为KCl的Λ∞m=
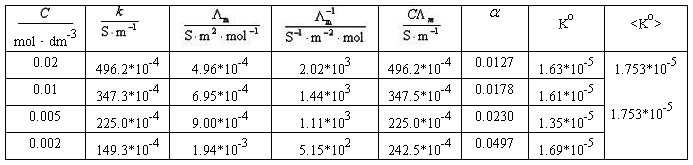
HAc溶液的各组数据

α=Λm/ Λ∞m Kθ=(CΛ∞m2)/ Λ∞mCθ(Λ∞m-Λm)
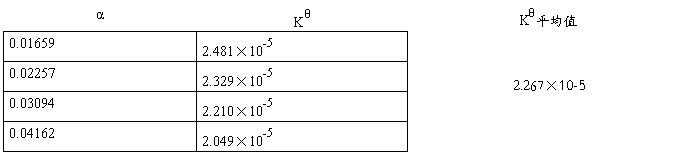
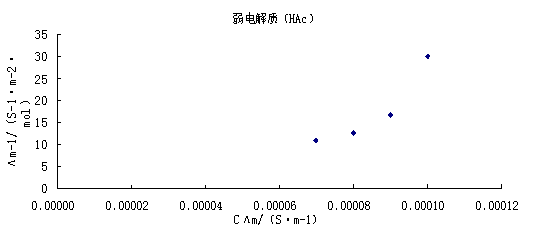
以CΛm对1/Λm作图
由图可知此直线的斜率为4.44727×10-5,所以(Λ∞m)2 KθCθ=4.44727×10-5,
又因为Λ∞m=3.907×10-2(S·m2·mol-1),Cθ=1mol/L;
所以Kθ=4.1963×10-5/((3.907×10-2)2×1×1000)=2.749×10-5
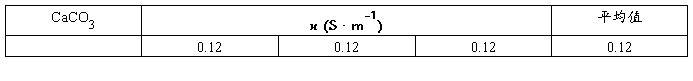
KCaCO3=0.12-0.093=0.027
Λm(1/2CaCO3)≈Λ∞m(1/2CaCO3) Λm(1/2CaCO3)=139.3×10-4
…… …… 余下全文
篇八 :电解质电导测定实验报告
实验三:电解质溶液的电导测定实验

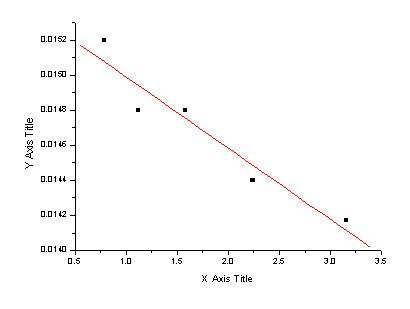
在浓度极稀的时候,额强电解质的Am与√C几乎成线性关系。
由于Kcl溶液是强电解质溶液,可以用外推法作当C ---- 0时,与纵坐标的交点即是溶液在无限稀释时的摩尔电导率Am

图一 :Kcl溶液的摩尔电导Am对√C作图
…… …… 余下全文