篇三 :熔点的测定实验报告
熔点的测定
一 实验目的
1, 了解熔点测定的基本原理及应用。
2, 掌握熔点的测定方法。
二实验原理
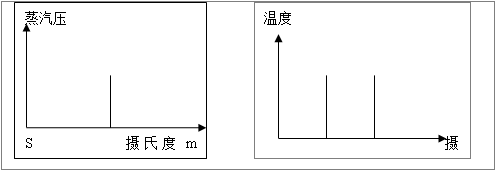
固液两相蒸汽压一致,固液两相平衡共存,这时的温度摄氏度m即为该物质的熔点。初熔至全熔范围称为熔程。温度不超过0.5-1摄氏度。当含有非挥发性杂质时,液体的蒸汽压降低,熔点降低,熔程变长。
三,熔点测定方法
(1) 粗测:快速加热5℃/min,测定大概熔点温度(适用未知物的熔点测定)
(2) 精测:缓慢加热5℃/min,距熔点10时,减慢加热速度为1—2s。当毛细管仲样品开始塌落和有温润现象时,出现下滴液体时,表明样品已经开始融化,为初熔,记下温度,继续加热,至透明胶体,记下温度为全熔
四,实验内容
1, 测定尿素的熔点。(mp 132.7摄氏度)
2, 测定肉桂酸的熔点(mp 133摄氏度)
主要装置:


…… …… 余下全文
篇四 :熔点的测定预习实验报告
河北北方学院20xx级工业分析与检验一班 邢妍萍
熔点的测定预习实验报告
一、实验目的及要求
1.了解熔点测定的意义和应用。
2.掌握熔点测定的操作方法。
3.了解温度计校正的方法。
二、实验原理
晶体化合物的固液两态在大气压力下成平衡时的温度称为该化合物的熔
点。利用测定熔点,可以估计出有机化合物的纯度。 如果在一定的温度和压力下,将某物质的固液两相置于同一容器中,将可能发生三种情况:固相迅速转化为液相;液相迅速转化为固相;固相液相同时并存,它所对应的温度TM即为该物质的熔点。
三、实验装置
温度计、b形管(Thiele管)、熔点毛细管、酒精灯、开口橡皮塞、乳胶管、玻璃棒、烧杯、表面皿
四、实验步骤
1.制备熔点管 内径为1mm、长为60~70mm、一端封闭的毛细管作为熔点管
2.样品的填装 取干燥、研细的待测物样品放在表面皿上,将毛细管开口一端插入样品中,即有少量样品挤入熔点管中。然后取一支长玻璃管,垂直于桌面上,由玻璃管上口将毛细管开口向上放入玻璃管中,使其自由落下,将管中样品夯实。重复操作使所装样品约有 2~3mm 高时为止。
3、仪器安装 向 B 管中加入浓硫酸作为加热介质,直到支管上沿。在温度计上
…… …… 余下全文
篇五 :熔点.沸点的测定实验报告
有 机 化 学 实 验 报 告

实 验 学 专 班 姓 指 导日 名 称: 院: 业: 级: 名:教 师: 期:
熔点的测定、沸点的测定 化学工程与工艺 化工10-1班 郭了了 学 号 10402010114 房椒华、沈梁钧 20xx年10月13日
一、 实验目的
1、 了解熔点和沸点的意义和应用
2、 掌握熔点沸点测定的操作方法
二、 实验原理
1.每一个晶体有机物都是具有一定的熔点,利用测定熔点,可以估计出有机化合物的纯度;
2.纯净有机物都有一定沸点,利用沸点可以估计出有机物的纯度;
三、 主要试剂及物理性质
尿素、苯甲酸、未知溶液;丙酮、乙醇、未知溶液;
几个概念:1.始熔:样品开始融化
2.熔距:开始熔化至完全熔化的温度范围,也叫熔点范围,熔距:一般不超过0.5℃
3.全熔固体样品消失成为透明液体时
四、 仪器装置
…… …… 余下全文
篇六 :传热膜系数测定实验报告加思考题
目录
一.摘要............................................... 1
二.实验目的........................................... 1
三.实验基本原理及内容................................. 1
四.实验装置说明及流程图............................... 3
五.实验步骤.......................................... 4
六.实验注意事项...................................... 4
七.实验数据处理...................................... 5
八.结果与讨论........................................ 8
九.误差分析.......................................... 9
十.思考题............................................ 9
…… …… 余下全文
篇七 :有机化学实验部分思考题答案
测定熔点时,遇到下列情况将产生什么结果?
(1) 熔点管壁太厚;(2) 熔点管不洁净;(3) 试料研的不细或装得不实;(4)加热太快;(5) 第一次熔点测定后,热浴液不冷却立即做第二次;(6)温度计歪斜或熔点管与温度计不附贴。
答:(1) 熔点管壁太厚,影响传热,其结果是测得的初熔温度偏高。
(2) 熔点管不洁净,相当于在试料中掺入杂质,其结果将导致测得的熔点偏低。
(3) 试料研得不细或装得不实,这样试料颗粒之间空隙较大,其空隙之间为空气所占据,而空气导热系数较小,结果导致熔距加大,测得的熔点数值偏高。
(4) 加热太快,则热浴体温度大于热量转移到待测样品中的转移能力,而导致测得的熔点偏高,熔距加大。
(5) 若连续测几次时,当第一次完成后需将溶液冷却至原熔点温度的二分之一以下,才可测第二次,不冷却马上做第二次测量,测得的熔点偏高。
…… …… 余下全文
篇八 :实验三熔点的测定
实验三 熔点的测定
实验目的:
1.了解熔点测定的意义。
2.掌握测定熔点的操作。
实验原理:
每一个晶体有机化合物都具有一定的熔点,熔点就是化合物熔化时固液两态在大气压下成平衡的温度。一个纯化合物从始熔到全熔的温度范围称为熔距(熔点范围或熔程),一般为0.5~1℃。若含有杂质则熔点下降,熔距增大。大多数有机化合物的熔点都在300℃以下,较易测定。
实验器材和药品:
b形管、酒精灯、温度计、液体石蜡、苯甲酸、乙酰苯胺
实验内容与方法:
1.熔点管拉熔制
用内径为1mm,长约60~70mm一端封闭的毛细管作为熔点管。
2.样品的填装
取0.1~0.2g样品,放在干净的表面皿上,用玻棒研成粉末,集成一堆,将毛细管的开口端插入样品堆中,使样品挤入管内,把开口一端向上竖立,轻敲毛细管使样品落在管底;至高度2~3mm。
注:①样品研得很细;②装样品要迅速;③样品结实均匀无空隙
3.测定熔点的装置
测定熔点的装置是利用Thiele管(又叫b形管也叫熔点测定管)。
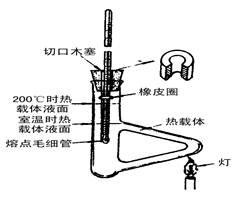
4.熔点测定方法
熔点测定的关键操作之一就是控制加热速度,使热能透过毛细管,样品受热熔化,令熔化温度与温度计所示温度一致,一般方法是先在快速加热下,粗测化合物的熔点,再作第二次测定, 测定前,先待热浴温度降至熔点约30℃以下,换一根样品管,慢慢加热,一开始5℃/min,当达到熔点下约15℃时,以1~2℃/min升温,接近熔点时,以0.2~0.3℃/min升温,当毛细管中样品开始塌落和有湿润现象,出现下滴液体时,表明样品已开始熔化,为始熔,记下温度,继续微热,至成透明液体,记下温度为全熔。
…… …… 余下全文