篇二 :配制一定物质的量浓度的溶液实验报告设计
实验报告
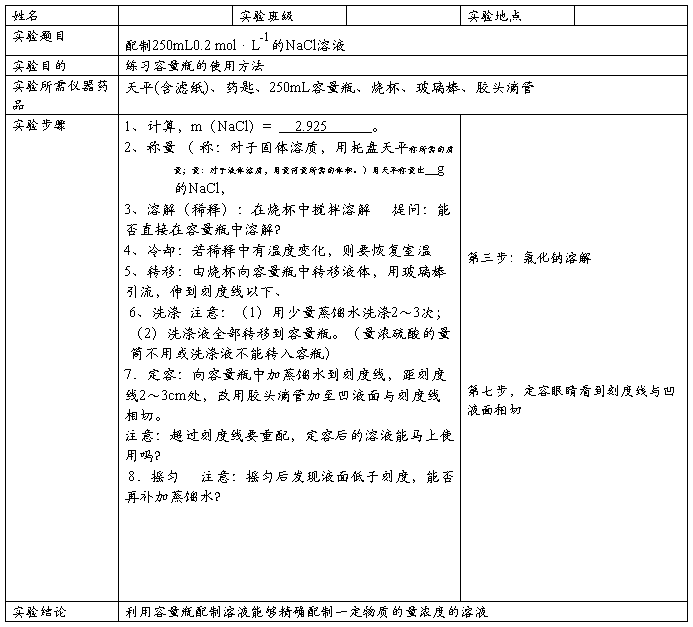
【实验一】配制一定物质的量浓度的溶液
一、 实验目的:1、掌握配制一定物质的量浓度的溶液的操作过程和方法。
2、加深对物质的量浓度概念的理解。
3、学会容量瓶、胶头滴管、托盘天平等的使用方法。
4、培养严谨、求实的科学作风。
三、实验用品:烧杯、玻璃棒、药匙、滤纸、托盘天平、 容量瓶 、胶头滴管 氯化钠固体、蒸馏水
四、实验内容:
五、实验注意点:
(1)容量瓶属于精密仪器,主要用于配制一定浓度的溶液,不允许加热。
…… …… 余下全文
篇四 :配制一定物质的量浓度的溶液实验报告
配制一定物质的量浓度的溶液实验报告
实验目的
1、练习配制一定物质的量浓度的溶液。
2、加深对物质的量浓度概念的理解。
3、练习容量瓶、胶头滴管的使用方法。
实验原理
n=C V,配制标准浓度的溶液
实验用品
烧杯、容量瓶(100mL)、胶头滴管、量筒、玻璃棒、药匙、滤纸、托盘天平、NaCl(s)、蒸馏水。
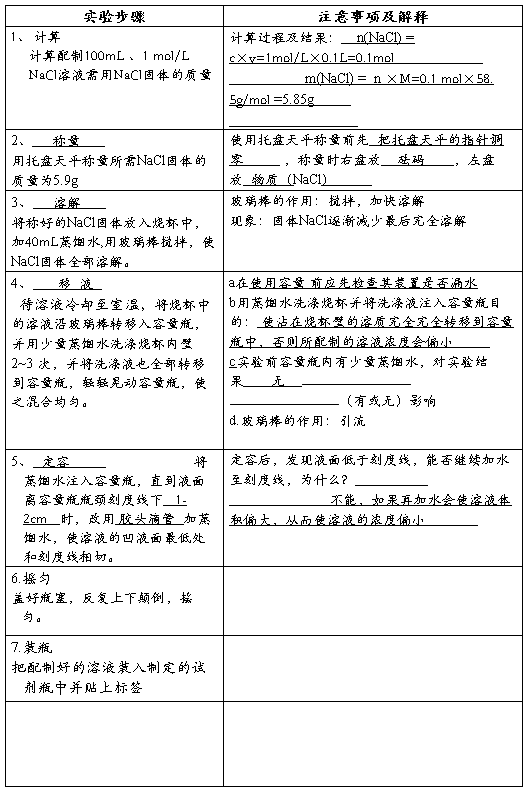
实验步骤
(1)计算所需溶质的量
(2)称量:固体用托盘天平,液体用量筒(或滴定管/移液管)移取。
(3)溶解或稀释(用玻璃棒搅拌)
(4)移液:把烧杯液体引流入容量瓶(用玻璃棒引流)。
(5)洗涤:洗涤烧杯和玻璃棒2~3次,洗涤液一并移入容量瓶,振荡摇匀。
(6)定容:向容量瓶中注入蒸馏水至距离刻度线2~3 cm处改用胶头滴管滴蒸馏水至溶液凹液面与刻度线正好相切。(要求平视)
(7)盖好瓶塞,反复上下颠倒,摇匀。
实验结果
计算出溶质的质量
实验结论
(1)配制一定物质的量浓度的溶液是将一定质量或体积的溶质按所配溶液的体积在选定的容量瓶中定容,因而不需要计算水的用量。
…… …… 余下全文
篇五 :一定物质量浓度溶液的配制实验报告
配制一定物质的量浓度的溶液
考试内容:配制100ml0.1mol/LNa2CO3溶液
实验名称:配制100ml0.1mol/LNa2CO3溶液
实验目的:练习配制一定物质的量浓度的溶液;加深对物质的量浓度概念的理解;练习容量瓶的使用方法。
实验原理:溶液稀释前后溶质的物质的量不变。
实验用品:托盘天平、小烧杯、药匙、容量瓶(100ml)、胶头滴管、玻璃棒、量筒、蒸馏水、Na2CO3固体粉末
实验步骤与装置图:
1.计算 所需 Na2CO3固体粉末的质量为:
m(Na2CO3)=100×10-3×0.1mol/L×106g·mol-1=1.06g 因为托盘天平的精确度只能达到0.1,所以应称量1.1g 。
2.称量 称量固体一般应在托盘天平两端各垫一张大小相同的纸。
3.溶解 先将固体置于烧杯中,加入约所配溶液体积一半的水溶解,搅拌并冷却到室温。
4.转移液体 将冷却后的溶液沿玻璃棒转移到容量瓶中。
5.洗涤 用少量蒸馏水洗涤烧杯2~3次,并将洗涤液也全部转移到容量瓶中。轻轻摇动容量瓶,使溶液混合均匀。
6.定容 向容量瓶中加水至离刻度1~2cm处,改用胶头滴管加水至刻度线。定容时,溶液凹液面恰好与刻度线相切。
…… …… 余下全文
篇六 :配制一定物质的量浓度的溶液实验报告
配制一定物质的量浓度的溶液实验报告
实验目的
1、练习配制一定物质的量浓度的溶液。
2、加深对物质的量浓度概念的理解。
3、练习容量瓶、胶头滴管的使用方法。
实验重点
1、配制一定物质的量浓度的溶液的操作过程和方法。
2、容量瓶、胶头滴管、托盘天平等的使用方法。
实验用品
烧杯、容量瓶(100mL)、胶头滴管、量筒、玻璃棒、药匙、滤纸、托盘天平、NaCl(s)、蒸馏水。
实验过程
物质的量是化学上的重要物理量,是把宏观物质与微观粒子数联系起来的桥梁。学习配制一定物质的量浓度的溶液,对于学习化学和今后的工作,都有非常重要的意义。
1、 计算 2、称量 3、溶解(稀释) 4、移液 5、洗涤 6、定容 7、摇匀
即:
(1)计算所需溶质的量
(2)称量:固体用托盘天平,液体用量筒(或滴定管/移液管)移取。
(3)溶解或稀释(用玻璃棒搅拌)
(4)移液:把烧杯液体引流入容量瓶(用玻璃棒引流)。
(5)洗涤:洗涤烧杯和玻璃棒2~3次,洗涤液一并移入容量瓶,振荡摇匀。
(6)定容:向容量瓶中注入蒸馏水至距离刻度线2~3 cm处改用胶头滴管滴蒸馏水至溶液凹液面与刻度线正好相切。(要求平视)
…… …… 余下全文
篇七 :配制一定浓度的溶液实验报告
实验题目:配制一定浓度的溶液
班级 姓名 同组人
实验目的:
掌握配制某A%溶液的方法
实验器材:
天平、药匙、烧杯、量筒(50ml)、细口瓶、食盐
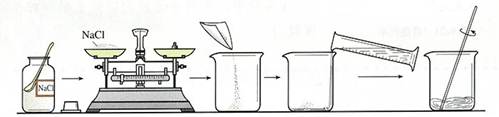
实验步骤:
1、计算:算出配制50g,6%的NaCl深液中NaCl和H2O的质量。
m(NaCl)= g
m(水)= g
V(水)= ml
…… …… 余下全文
篇八 :氯化钠溶液的配置实验报告
实验4:配制100mL1.00 mol/L的NaCl溶液
班级: 姓名:
【实验目的】
1、练习配制一定物质的量浓度的溶液;
2、加深对物质的量浓度概念的理解;
3、练习容量瓶的使用方法
【实验仪器药品】
托盘天平、小烧杯、药匙、100ml容量瓶、胶头滴管、玻璃棒、量筒
【实验药品】
NaCl固体、蒸馏水
【实验步骤】
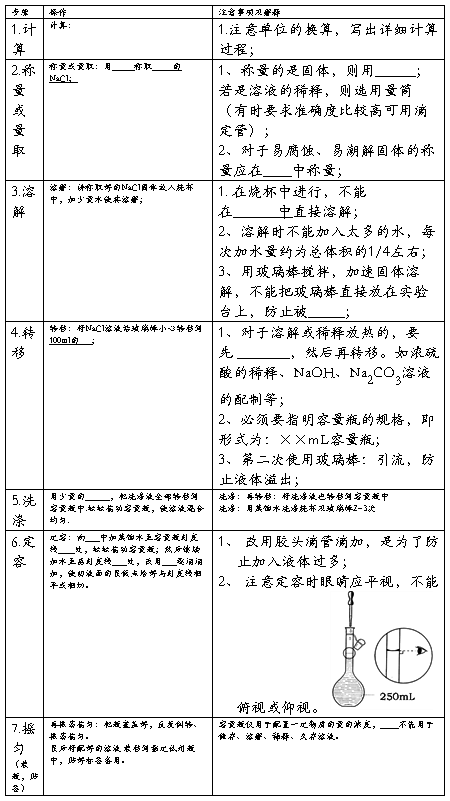
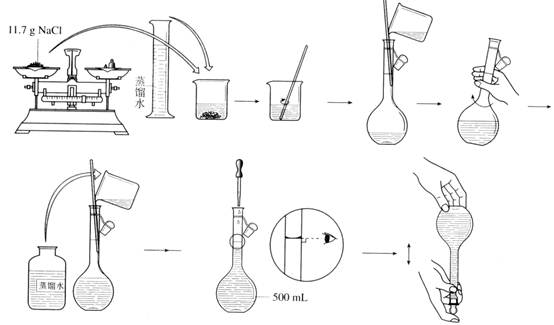
【交流与思考】
1、 容量瓶使用时应注意的事项:
2、 为什么要用蒸馏水来配置溶液而不能用自来水配置呢?
3、 为什么要洗涤玻璃棒和烧杯?如何洗涤?
4、 能否将溶解的NaCl溶液立即注入容量瓶中?为什么?
5、 为什么要将配好的溶液,从容量瓶里倒入试剂瓶?
6、 定容时不慎滴加液体超过刻度线,则该怎么做?
7、 下列实验操作会使所配制的溶液浓度偏高,偏低,还是不变?为什么?
①把溶液向容量瓶中转移,有少量溶液溅出;( ) 原因: ;
…… …… 余下全文