篇一 :物化各种公式概念总结
第一章热力学第一定律
一、基本概念
系统与环境,状态与状态函数,广度性质与强度性质,过程与途径,热与功,内能与焓。
二、基本定律 热力学第一定律:ΔU=Q+W。
三、基本关系式1、体积功的计算 δW= -p外dV
恒外压过程:W= -p外ΔV
定温可逆过程(理想气体):W=nRT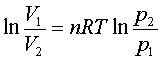
2、热效应、焓:等容热:QV =ΔU(封闭系统不作其他功)
等压热:Qp =ΔH(封闭系统不作其他功)
焓的定义:H=U+pV ; ΔH=ΔU+Δ(pV)
焓与温度的关系:ΔH=
3、等压热容与等容热容:热容定义: ;
;
定压热容与定容热容的关系: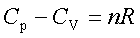
热容与温度的关系:Cp,m=a+bT+cT2
四、第一定律的应用
1、理想气体状态变化
等温过程:ΔU=0 ; ΔH=0 ; W=-Q=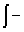 p外dV
p外dV
等容过程:W=0 ; Q=ΔU= ; ΔH=
; ΔH=
等压过程:W=-peΔV ; Q=ΔH=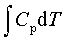 ; ΔU=
; ΔU=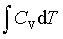
可逆绝热过程:Q=0 ; 利用p1V1γ=p2V2γ求出T2,
W=ΔU= ;ΔH=
;ΔH=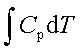
CV(㏑T2-㏑T1)=nR(㏑V1-㏑V2)(T与V的关系)
…… …… 余下全文
篇二 :物化公式总结

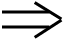
 1.
1.
Ω是热力学概率,K是玻尔兹曼常数,k=R/N=1.3807×10^(-23)J/K
 2.在温度趋近于热力学温度0 K时的等温过程中,体系的熵值不变。即:
2.在温度趋近于热力学温度0 K时的等温过程中,体系的熵值不变。即:
3.在0 K时,任何完整晶体的熵等于零。
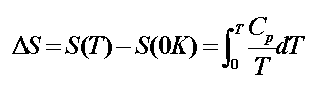
4.规定熵
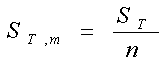 4.摩尔熵
4.摩尔熵
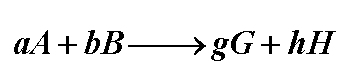
5.化学反应熵变

任意温度下(无相变)
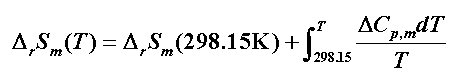
 6.亥姆霍兹能
6.亥姆霍兹能
-dFT³-d W
 吉布斯能
吉布斯能
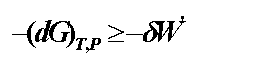
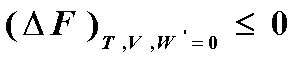 当封闭系统在等温、等容、非体积功 W¢= 0 的条件下
当封闭系统在等温、等容、非体积功 W¢= 0 的条件下
封闭系统在等温、等压、W’=0 条件下
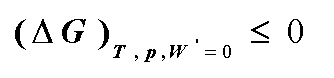
上式中的W为总功,为体积功(-PedV)与非体积功W¢之和。
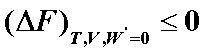 7.当封闭系统在等温、等容、非体积功 W¢= 0 的条件下:
7.当封闭系统在等温、等容、非体积功 W¢= 0 的条件下:
 自发过程
自发过程
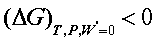
…… …… 余下全文
篇三 :高一物理公式总结
一、匀变速直线运动
1.平均速度: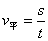 2.有用推论:
2.有用推论: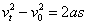
3.中间时刻速度: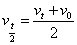 4.末速度:
4.末速度:
5.中间位置速度: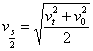 6.位移:
6.位移:
7.实验用推论: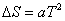 ;
;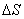 为相邻连续相等时间
为相邻连续相等时间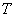 内位移之差
内位移之差
8. 1m/s=3.6Km/h
注:
1.平均速度是矢量。
2.物体速度大,加速度不一定大。
3.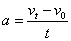 只是量度式,不是决定式。
只是量度式,不是决定式。
二、自由落体运动
1.初速度: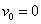 2.末速度:
2.末速度: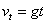
3.下落高度: 4.推论:
4.推论: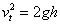
…… …… 余下全文
篇四 :初中物理公式总结
物理公式
1、比热公式:Q = cm△t
吸热:Q吸=Cm(t-t0)=CmΔt
Q ——热量(J);c ——物质的比热容(J/kg·℃);△t ——温度差(℃)
2、热值公式:Q = m·q Q =  ·q
·q
Q ——燃料放出的热量(J); q ——燃料的热值(J/kg);V——气体的体积(J/ m
m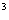 )
)
3、串联电路:? I=I =I
=I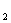 =…=I
=…=I ? U=U
? U=U +U
+U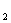 +…+U
+…+U ? R=R
? R=R +R
+R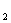 +…+R
+…+R
④ =
=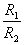
并联电路: ①I=I1+I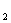 +…+I
+…+I ②U=U1=U
②U=U1=U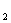 =…=U
=…=U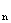 ③
③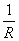 =
=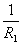 +
+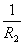 +…+
+…+
4、欧姆定律:I = 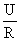 I——电流(A);U——电压(V);R——电阻(Ω)
I——电流(A);U——电压(V);R——电阻(Ω)
…… …… 余下全文
篇六 :物化公式
第一章 气体的pVT关系
主要公式及使用条件
1. 理想气体状态方程式
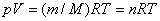
或 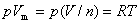
式中p,V,T及n单位分别为Pa,m3,K及mol。 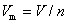 称为气体的摩尔体积,其单位为m3 · mol-1。 R=8.314510 J · mol-1 · K-1,称为摩尔气体常数。
称为气体的摩尔体积,其单位为m3 · mol-1。 R=8.314510 J · mol-1 · K-1,称为摩尔气体常数。
此式适用于理想气体,近似地适用于低压的真实气体。
2. 气体混合物
(1) 组成
摩尔分数 yB (或xB) = 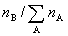
体积分数 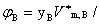
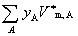
式中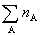 为混合气体总的物质的量。
为混合气体总的物质的量。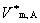 表示在一定T,p下纯气体A的摩尔体积。
表示在一定T,p下纯气体A的摩尔体积。 为在一定T,p下混合之前各纯组分体积的总和。
为在一定T,p下混合之前各纯组分体积的总和。
(2) 摩尔质量
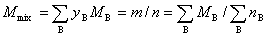
式中 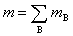 为混合气体的总质量,
为混合气体的总质量,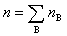 为混合气体总的物质的量。上述各式适用于任意的气体混合物。
为混合气体总的物质的量。上述各式适用于任意的气体混合物。
…… …… 余下全文
篇七 :初二物理下册公式总结
初二下册公式总结
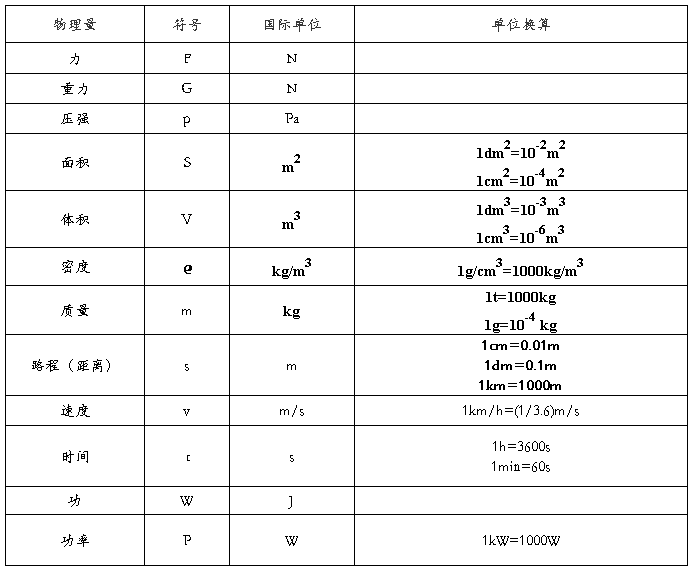
公式:
重力:G=mg(g=9.8N/kg) 变形:m=G/g=ρV ρ=m/V V=m/ρ
压强:(1)固体:p=FS 变形:F=p/S S=p/F
(2)液体:p=ρgh(ρ是液体的密度,h是液体的竖直深度,从液面到所研究的点的数值距离) 变形:ρ=p/gh h=p/ρh
浮力:(1)称重法 F浮=G-F示(G是物体的重力即物体在空气中弹簧测力计的示数,F示表示将物体完全浸没在液体中弹簧测力计的示数)
(2)压力差法F浮=F向上-F向下(F向上是指液体对物体向上的压力,F向下是指液体对物体向下的压力)
(3)阿基米德原理F浮=ρ液V排g(ρ液是液体的密度,V排是排出液体的体积,如果物体完全浸没在液体中则V排=V物,如果物体时漂浮在液面上的,则V排≠V物,V排只等于物体浸入液体中的那部分体积)变形:ρ液=F浮/V排g,V排=F浮/ρ液g
(4)漂浮、悬浮时F浮=G物
功:W=Fs=Pt 变形:F=W/s=P/v s=W/F=vt
…… …… 余下全文
篇八 :物态变化知识点总结
物态变化知识点总结
一、温度:
温度:温度是用来表示物体冷热程度的物理量;
注:热的物体我们说它的温度高,冷的物体我们说它的温度低,若两个物体冷热程度一样,它们的温度亦相同;我们凭感觉判断物体的冷热程度一般不可靠;
2、摄氏温度:
(1)温度常用的单位是摄氏度,用符号“C”表示;
(2)摄氏温度的规定:把一个大气压下,冰水混合物的温度规定为0℃;把一个标准大气压下沸水的温度规定为100℃;然后把0℃和100℃之间分成100等份,每一等份代表1℃。
(3)摄氏温度的读法:如“5℃”读作“5摄氏度”;“-20℃”读作“零下20摄氏度”或“负20摄氏度”
二、温度计
1、常用的温度计是利用液体的热胀冷缩的原理制造的;
温度计的构成:玻璃泡、均匀的玻璃管、玻璃泡总装适量的液体(如酒精、煤油或水银)、刻度;
温度计的使用:
使用前要:观察温度计的量程、分度值(每个小刻度表示多少温度)、零刻度线,并估测液体的温度,不能超过温度计的量程(否则会损坏温度计)
测量时,要将温度计的玻璃泡与被测液体充分接触,不能紧靠容器壁和容器底部; 读数时,玻璃泡不能离开被测液、要待温度计的示数稳定后读数,且视线要与温度计中夜柱的上表面相平。
…… …… 余下全文