实验报告格式模板-供参考
实验名称:粉体真密度的测定
粉体真密度是粉体质量与其真体积之比值,其真体积不包括存在于粉体颗粒内部的封闭空洞。所以,测定粉体的真密度必须采用无孔材料。根据测定介质的不同,粉体真密度的主要测定方法可分为气体容积法和浸液法。
气体容积法是以气体取代液体测定试样所排出的体积。此法排除了浸液法对试样溶解的可能性,具有不损坏试样的优点。但测定时易受温度的影响,还需注意漏气问题。气体容积法又分为定容积法与不定容积法。
浸液法是将粉末浸入在易润湿颗粒表面的浸液中,测定其所排除液体的体积。此法必须真空脱气以完全排除气泡。真空脱气操作可采用加热(煮沸)法和减压法,或两法同时并用。浸液法主要有比重瓶法和悬吊法。其中,比重瓶法具有仪器简单、操作方便、结果可靠等优点,已成为目前应用较多的测定真密度的方法之一。因此,本实验采用比重瓶法。
一.实验目的
1. 了解粉体真密度的概念及其在科研与生产中的作用;
2. 掌握浸液法—比重瓶法测定粉末真密度的原理及方法;
3.通过实验方案设计,提高分析问题和解决问题的能力。
二.实验原理
比重瓶法测定粉体真密度基于“阿基米德原理”。将待测粉末浸入对其润湿而不溶解的浸液中,抽真空除气泡,求出粉末试样从已知容量的容器中排出已知密度的液体,就可计算所测粉末的真密度。真密度ρ计算式为:
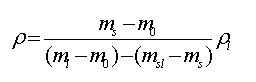
式中:m0—— 比重瓶的质重,g;
ms—— (比重瓶+粉体)的质重,g;
msl—— (比重瓶+液体)的质重,g;
ρl—— 测定温度下浸液密度;g/cm3;
ρ—— 粉体的真密度,g/cm3;
三.实验器材:
实验仪器:真空干燥器,比重瓶(2-4个);分析天平;烧杯。
实验原料:金刚砂。
四.实验过程
1. 将比重瓶洗净编号,放入烘箱中于110℃下烘干冷却备用。
2. 用电子天平称量每个比重瓶的质量m0。
3. 每次测定所需试样的题记约占比重瓶容量的1/3,所以应预先用四分法缩分待测试样。
4. 取300ml的浸液(实际实验中为去离子水)倒入烧杯中,再将烧杯放进真空干燥器内预先脱气。浸液的密度可以查表得知。
5. 在已干燥的比重瓶(m0),装入约为比重瓶容量1/3的粉体试样,精确称量比重瓶和试样的的质量ms。
6. 将预先脱气的去离子水注入有试样的的比重瓶内,到容器容量的2/3处为止,放入真空干燥器内。启动真空泵,抽气约20-30min时暂停抽气。
7. 从真空干燥器中取出比重瓶,向瓶内加满浸液并在电子天平上称其质量msl。
8. 洗净该比重瓶,向瓶内加满浸液,称其质量为ml。
9. 重复操作5.6.7.8测下一组数据,多次测量取平均值。
五.数据记录与处理
1. 数据记录
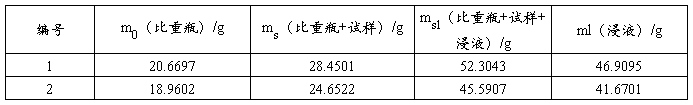
2. 数据处理:
根据公式
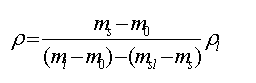
实验室室温为23.4℃,查表得此温度下水的密度是 ,因此
,因此


所以


绝对偏差:
六.思考题
1. 测定真密度的意义是什么 ?
(1)在测定粉体的比表面积时需要粉体真密度的数据进行计算。
(2)许多无机非金属材料都采用粉末原料来制造,因此在科研或生产中经常需要测定粉体真密度。
(3)在水泥或陶瓷材料制造中,需要对粘土的颗粒分布球磨泥浆细度进行测定,都需要真密度的数据.
(4)尤其对于水泥材料,其最终产品就是粉体,测定水泥的真密度对生产单位和使用单位都具有很大的实用意义。
2. 浸液法-比重瓶法测定真密度的原理是什么?
阿基米德原理:浸在液体(或气体)里的物体受到向上的浮力作用,浮力的大小等于被该物体排开的液体的重力。
七.实验心得(没有强制要求,可选写)
以往的实验都是比着实验书本操作,而本次实验实验方案则是自己自主完成的,毫无经验可谈,但是实验过程中享受到了独立自主的乐趣。这种实验课堂方式极大的激发了同学们对实验的探索能力和对未知的好奇心。继续下去,会有更大的收获。
第二篇:实验报告模板
四川以勒科技有限公司
实 验 报 告
项目名称:
实验人员:
指导老师:
报告日期:
(一)实验目的
了解和掌握水质中高锰酸盐的测定原理和方法。
(二)实验原理
样品中加入已知量的高锰酸钾和硫酸,在沸水浴中加热30min,高锰酸钾将
样品中的某些有机物和无机还原性物质氧化,反应后加入过量的草酸钠还原剩余的高锰酸钾,再用高锰酸钾标准溶液回滴过量的草酸钠,通过计算得到样品中高锰酸盐指数。
(三)仪器设备及试剂 1.仪器设备
水浴锅,有足够的容积和功率。 酸式滴定管,25.00mL
2.试剂
1.不含还原性物质的水; ;
2.硫酸,ρ20=1.84g/mL 3.硫酸溶液(V/V),1+3; 4.氢氧化钠溶液,500g/L;
5.草酸钠标准贮备液,C(1/2Na2C2O4)=0.1000mol/L ;称取0.6705g经120摄氏度烘干2h并放冷的草酸钠溶解于水中,转移至100mL容量瓶,加水至刻度,混匀。
6.草酸钠标准液,C(1/2Na2C2O4)=0.0100mol/L ;吸取10.00mL草酸钠标准储备液(2.5)至100mL容量瓶,加水至刻度,混匀。
7.高锰酸钾标准储备液,C(1/5KMnO4)= 0.1000mol/L,称取3.2g高锰酸钾溶解于水并稀释至1000mL。于90-95摄氏度水浴加热2h,冷却,存放2天后,倾出上清液,储于棕色瓶中。
8.高锰酸钾标准溶液,C(1/5KMnO4)=0.0100mol/L,吸取10.00mL高锰酸钾标准储备液(2.7)至100mL容量瓶,加水至刻度,混匀。
(四)实验步骤 1. 试料
采样前,静置30min,用吸管一次或几次移取水样,习惯进水尖嘴应插至水样表层50mm以下位置,采样后要加入硫酸(2.3),使样品pH1~2并尽快分析。如保存时间超过6h,则需置于暗处,0~5C保存,不得超过2天。
吸取100mL经充分摇动、混合均匀的样品置于250mL锥形瓶中,加入5±0.5mL硫酸(2.3),用滴定管加入10.00mL高锰酸钾溶液(2.8),摇匀,将锥形瓶置于沸水浴内30±2min。取出后用滴定管加入10.00mL草酸钠溶液(2.6)至溶液变为无色。趁热用高锰酸钾(2.8)滴定到刚好出现粉红色,并保持30s不褪色。记录消耗的高锰酸钾体积(4.1)。 2. 空白试验
用水代替试料,采用相同的步骤,且与采样和测定中所用的试剂用量相同做空白试验。记录下回滴高锰酸钾溶液的体积。
向空白试验滴定后的溶液中加入10.00mL草酸钠溶液,如果需要,将溶液加热至80C,用高锰酸钾溶液滴定至刚好出现粉红色,并保持30s不褪色。记录消耗的高锰酸钾体积(4.2)。 6.结果计算[3]
实验室样品中高锰酸盐指数IMn(O2,mg/L),按照下式计算:
式中;V1—样品滴定时消耗高锰酸盐的体积,mL。
V2—空白滴定时消耗高锰酸盐的体积(4.2),mL。 C—草酸钠标准溶液,0.0100mol/L。
如样品需稀释后测定:
V0—空白滴定时消耗高锰酸盐的体积(4.1),mL。
V3—所取样品的体积(4.2),mL。
f—稀释样品时,蒸馏水在100mL测定用体积内所占比例。
(五)结果表示
(高锰酸钾标准滴定液浓度:C=0.0100mol/L 取样体积:100mL
空白滴定消耗高锰酸钾体积:V2=10.00mL)
-
实验报告格式模板-供参考
实验名称:粉体真密度的测定粉体真密度是粉体质量与其真体积之比值,其真体积不包括存在于粉体颗粒内部的封闭空洞。所以,测定粉体的真密度…
-
实验报告模版和格式要求
本科实验报告实验报告课程名称:单片机导论指导老师:XX成绩:_______实验名称:___软件实验__________实验类型:_…
-
实验报告范本
学生实验报告书实验课程名称开课学院指导教师姓名学生姓名学生专业班级200200学年第学期实验教学管理基本规范实验是培养学生动手能力…
-
实验报告模板(文字格式,具体排版)
北京信息科技大学黑体1号居中实验报告宋体2号加粗居中课程名称学院专业学生姓名班级学号任课老师起止时间200年月日至200年月日以上…
-
实验报告格式
光电技术实验报告实验日期20xx年11月2425日一实验目的1干涉的实验目的1组装调节迈克尔逊干涉仪观察点光源产生的非定域等厚等倾…
-
化学实验报告格式
化学实验报告格式例一定量分析实验报告格式(以草酸中h2c2o4含量的测定为例)实验题目:草酸中h2c2o4含量的测定实验目的:学习…
-
实验报告 范本
研究生实验报告范本实验课程实验名称实验地点学生姓名学号指导教师范本实验时间年月日一实验目的熟悉电阻型气体传感器结构及工作原理进行基…
-
实验报告范本
学生实验报告书实验课程名称开课学院指导教师姓名学生姓名学生专业班级200200学年第学期实验教学管理基本规范实验是培养学生动手能力…
- 企业实验报告范本
-
实验报告规范格式
人文与艺术学院实验报告课程名称图文处理班级14编辑出版学指导教师任雪飞学号学生姓名20xx20xx学年第一学期实验报告填写说明1实…
-
大学生实习报告格式及范文(全)
《实践报告格式》系部名称:专业:______年级______班级:_________姓名:_____学号:____实践单位:XXX…