物理化学实验总结
就物理化学实验这门课来说,它是一门非常有意思,严谨,科学的实验。通过实验课,我更直观具体的了解学习到物质本身与物质间的有关物理和化学反应及实验现象,学会了写实验报告,学会了列数据表、画数据图等实验的基本技能。
因为每周的实验都不一样,各个装置仪器也不一样,因此每次试验都充满着新奇与挑战。就觉得做实验像一种游戏,充满了乐趣。自己和别人搭档,共同完成一项任务,最终达到预期的目标,收获喜悦与成就。而且在实验当中,我们充分享受过程,但绝不耽搁,几乎所有实验操作都是最先完成的。而我们组合理分工,默契配合,很快就记录完了数据,并且做出的曲线还很理想,那种又快又好的感觉真是特别让人觉得自豪。当然我们也有出问题的时候,记得有一次实验中,我们因为预习不全面,搞错了两个实验中加试剂的顺序,以致不停出现不该有的沉淀,导致我们重新做了好几次,最后折腾了半天才完成实验。所以对于实验来说,预习是最关键的第一步,没有很好的预习,就不会有顺利的实验,也不会有精确的数据,更不会有完美的图表,合理的结果。很多同学在抱怨物理化学实验要写两份报告,但我觉得这是不能缺少的。一步出错,步步皆错。所以写预习报告是必不可少,也是不能马虎的。
物化实验已经结束了,在这半学期的物化实验中我学到了不少知识,也遇到了不少问题,在这里我就举几个实验的例子来总结一下。
实验一 燃烧热的的测定
实验关键:点火成功、试样完全燃烧是实验成败关键,可以考虑以下几项措施:
①试样应进行磨细、烘干、干燥器恒重等前处理,潮湿样品不易燃烧且有误差。
压片紧实度:一般硬到表面有较细密的光洁度,棱角无粗粒,使能燃烧又不至于引起爆炸性燃烧残剩黑糊等状。
②点火丝与电极接触电阻要尽可能小,注意电极松动和铁丝碰杯短路问题。
③充足氧(2MPa)并保证氧弹不漏氧,保证充分燃烧。燃烧不完全,还时常形成灰白相间如散棉絮状。
实验的的改进:
在此次实验中,通常将点火电流控制旋钮事先测试并固定在第十个数据,这种处理方法长会出现电流过小或过大.点火的时间过短或过长的现象,可将点火电流控制旋钮在点火之前至最小值,按下点火键后,在将点火电流控制转钮匀速的向电流增加的方向旋转,并将点火时间控制在5s以内,在点火指示点火结束后,终止点火。这样控制点火电流,使燃烧丝有一个在小电流下预热.发亮的过程,同时也使药品受到预热而易被点燃,在较高压力氧气存在的条件下,红热的燃烧丝立即被高温氧化,耐火度迅速提高,在较高电流作用下,燃烧丝才会熔断,从而提高药品连同燃烧丝一起被烧掉的机会,提高点火功率。
实验二 纯液体饱和蒸气压的测定
本实验方法是否用于测定溶液的蒸汽压,为什么?
我觉得不能用来测定溶液的蒸汽压,因为蒸汽中混有水蒸气,影响测量结果。
实验的的改进:
采用蒸馏水代替异丙醇,因为异丙醇是有毒.有刺激性的气体。如果长期使用会对师生的身体健康产生威胁,还会污染实验室的环境。用蒸馏水代替异丙醇后不仅降低了原料的成本,又保护了实验室的环境,对师生的身体健康也是有益的。
实验三 完全互溶双液系的平衡相图
本实验要注意以下几点:
1. 沸点仪中没有装入溶液之前绝对不能通电加热,如果没有溶液,通电加热丝后沸点仪会炸裂。
2. 一定要在停止通电加热之后,方可取样进行分析。
3. 沸点仪中蒸气的分馏作用会影响气相的平衡组成,使得气相样品的组成与气液平衡时气相的组成产生偏差,因此要减少气相的分馏作用。本实验所用的沸点仪是将平衡的蒸气冷凝在小球(2)内(见图3),在容器中的溶液不会溅入小球(2)的前提下,尽量缩短小球(2)与原溶液的距离,以达到减少气相的分馏作用。
4. 使用阿贝折光仪时,棱镜上不能触及硬物(滴管),每次加样前,必须先将折光仪的棱镜面洗净,可用数滴挥发性溶剂(如丙酮)淋洗,再用擦镜纸轻轻吸去残留在镜面上的溶剂。在使用完毕后,也必须将阿贝折光率的镜面处理干净。
实验四 凝固点降低法测定摩尔质量
化合物的摩尔质量是一个重要的物理化学数据。凝固点降低法是一种简单而比较准确的测定摩尔质量的方法。凝固点降低法在实际应用和对溶液的理论研究方面都具有重要意义。
稀溶液的依数性之一为凝固点下降,溶液的凝固点低于纯溶剂的凝固点,对理想溶液来说,凝固点的下降与溶质的摩尔浓度成正比。
实验五 液相反应平衡常数
本实验测定电解质(甲基红)的电离常数,是根据甲基红在电离前后具有不同颜色和对单色光的吸收特性,借助于分光光度法的原理,测定其电离常数,甲基红在溶液中的电离可表示为:
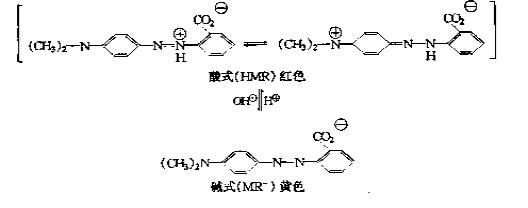
则其电离平衡常数K表示为:
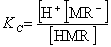
或  (1)
(1)
由(1)式可知测定甲基红溶液的pH值,再根据分光光度法(多组分测定方法),可测得[MR-]和[HMR]值,即可求得pK值。
实验六 电极的制备和原电池电动势的测定
原电池是化学能转变为电能的装置,它是由两个“半电池”所组成,而每一个半电池中有一个电极和相应的电解质溶液,由半电池可组成不同的原电池。在电池放电反应中,正极起还原反应,负极起氧化反应,电池反应是电他中两个电极反应的总和,其电动势为组成该电池的两个半电池的电极电势的代数和。
电池的书写习惯是左边为负极.右边为正极,符号“│”表示两相界面,“‖”表示盐桥,盐桥的作用主要是降低和消除两相之间的接界电势。
实验七 粘度法测定高聚物的摩尔质量
本实验测定的是数均摩尔质量,受环境的影响很大,温度、高聚物本身的粘度影响都很大,不适合测定分子量分布很大的聚合物,分子量太小或太大都不行,测定的 是相对分子质量,所以还需要找到一个已知分子量的物质同时测定。粘度太小会测不准(流出时间太小)。 实验八 电导的测定及其应用
1、实验中不必扣除水的电导。因为经测定,实验所使用的去离子水的电导与待测溶液的电导相差几个数量级,因此不会对实验结果产生很大的影响。
2、溶液配制时的问题:溶液时由大浓度向小浓度一瓶一瓶稀释过来的。一旦某一瓶配制出现偏差,则将影响到后面的几瓶,因此在溶液配制的时候要及其小心,我认为这也是影响实验准确性的一个很重要的因素。
3、浓度较小时,信号不明显,即某个电阻改变一个大阻值,其示波器的变化不大,可能会导致大的偏差。
实验九 最大气泡压力法测定液体表面张力
最大气泡法测表面张力实验中,理论计算所得值与实验测得数值存在偏差的因素是:
1:首先要保证装置不能有一点点漏气,所以在玻璃装置的某些接口处涂点凡士林。
2:要保证毛细管尖端的洁净与完好无损,但实际中总是会有点缺陷,如果将毛细管尖端换成是一次性的东西,然后再与毛细管相连,但这样之后就可能不能保证整个毛细管的垂直,所以不知道可不可行。
3.本实验还有一个问题,就是要求毛细管与液面相切,但实际中可能做不到;但伸入液面△h的话,测出来的又不是表面的张力,所以不知道这个问题还不知道怎么解决。
实验十 蔗糖水解反应速率常数的测定
1)把预测溶液盛入试管待测。但应注意试管两端螺旋不能旋得太紧(一般以随手旋紧不漏水为止),以免护玻片产生应力而引起视场亮度发生变化,影响测定准确度,并将两端残液揩拭干净;
2)接通电源,约点燃10min,待完全发出钠黄光后,才可观察使用;)
3)打开镜盖,把试管放入镜筒中测定,试管内不应有气泡,否则会影响观察和测定;
蔗糖水解反应速率常数的测定中可以用粗天平称取反应物蔗糖的用量是因为蔗糖水解为一级反应,反应物起始浓度不影响反应速度常数,还有实验中用到的蔗糖是普通的食用蔗糖,品质较差,里面混有比较多的杂质,纯度不是很高。所以,用粗天平称取蔗糖用量。因为即使用精密度很高的天平称蔗糖也没有太大意义。
试验十一 乙酸乙酯皂化反应
本实验的影响因素较多,且对实验造成的影响较大,具体的影响因素有:温度的波动,样品混合均匀与否,计时点晚于反应开始点,还有乙酸乙酯放置时间过久自行分解和挥发。这些因素都会对实验结果造成巨大影响,因此实验要精确控制。
实验十二 丙酮转化
本实验因注意以下几点:
1.温度对反应速度有一定的影响,本实验在开始测定透光率后未考虑温度的影响。实验表明,如选择较大的比色皿和在不太低的气温条件下进行实验,在数分钟之内溶液的温度变化不大。如条件允许,可选择带有恒温夹套的分光光度计,并与超级恒温槽相连,保持反应温度。
2.当碘浓度较高时,丙酮可能会发生多元取代反应。因此,应记录反应开始一段时间的反应速率,以减小实验误差。
3.向溶液中加入丙酮后,反应就开始进行。如果从加入丙酮到开始读数之间的延迟时间较长,可能无法读到足够的数据,甚至会发生开始读数时透光率已超过80%的情况,当酸浓度或丙酮浓度较大时更容易出现这种情况。为了避免实验失败,在加入丙酮前应将分光光度计零点调好,加入丙酮后应尽快操作,至少在两分钟之内应读出第一组数据。
实验十三 二组分金属相图的绘制
某些体系在析出固体时,会出现“过冷”现象,即温度到达凝固点时不发生结晶,当温度到达凝固点以下几度时才出现结晶,出现结晶后,体系的温度又回到凝固点。在绘制步冷曲线时,会出现一个下凹。在确定凝固点温度时,应以折线或平台作趋势线,获得较为合理的凝固点
实验十四 离子迁移数的测定
本实验的原理是:在电场的作用下,即通电于电解质溶液,在溶液中则发生离子迁移现象,正离子向阴极移动,负离子向阳极移动。正、负离子共同承担导电任务,致使电解质溶液能导电,由于正负离子移动的速率不同,因此它们对任务分担的百分数也不同,某一种离子迁移的电量与通过溶液总电量之比称为该离子的迁移数。注意:如果中间区的溶液浓度变化较大,则实验应该重做。
实验心得:
通过这个学期的大学物化实验,我体会颇深.首先,我通过做实验了解了许多实验的基本原理和实验方法,学会了基本物化量的测量分析方法,基本实验仪器的使用等;其次,我已经学会了独立作实验的能力,大大提高了我的动手能力和思维能力以及基本操作与基本技能的训练,并且我也深深感受到做实验要具备科学的态度,认真态度和创造性的思维. 在老师的耐心讲解及细心指导下,通过本学期的物理化学实验,实验技能有显著提高,接触并掌握了很多新仪器的使用方法,学会了将课堂上的知识灵活运用到实验中去,并可以自己用所学知识来解决实验中所出现的问题,做到理论与实际紧密结合,活学活用。 下面我就谈一下我在做实验时的一些技巧与方法.首先,做实验要用科学认真的态度去对待实验,认真提前预习,做好实验预习报告;第二,上课时认真听老师做预习指导和讲解,把老师特别提醒会出错的地方写下来,做实验时切勿出错;第三,做实验时按步骤进行,切不可一步到位,太心急.并且一些小节之处要特别小心,若不会,可以跟其他同学一起探讨一下,把问题解决.第四,实验后数据处理一定要独立完成,莫抄其他同学的,否则,做实验就没有什么意义了,也就不会有什么收获.
在实验中,我学到很多东西,特别是在做实验报告时,因为在做数据处理时出现很多问题,如果不解决的话,将会很难的继续下去。例如:数据处理画图时,也要用软件画图,这也要求懂得excel软件的插入图表命令。还有动手这次实验,使物理化学这门课的一些理论知识与实践相结合,更加深刻了我对这门课的认识,巩固了我的理论知识。
俗话说,人有两个宝,双手和大脑。双手会做工,大脑会思考。每一个理工科大学生不一定动手操作技能水平会很高,甚至有的大学生还很低。可是通过此次物化实验,经过三位名师(韩斌、李涛和姚明明)的指导,我了解并学会了很多东西。是我认识到物理化学实验作为化学实验课程的重要分支,是与物理化学课堂理论教学相辅相成的基础实验课程。物理化学实验课的主要目的是使学生初步了解物理化学的研究方法,通过实验手段了解物质的物理化学性质与化学反应规律之间的关系,熟悉重要的物理化学实验技术,掌握实验数据的处理及实验结果的分析、归纳方法,加深对物理化学基本理论和概念的理解,增强解决化学实际问题的能力,为将来工作和进一步深造打下良好的专业基础。
通过做物化实验,我清楚的认识到,做事要严谨,做人应诚信。知之为知之,不知为不知。只有这样,以后走向工作岗位,才能踏踏实实,做一个堂堂正正的人。
通过做物化实验,我感觉能力的培养和训练主要表现在三个方面:
(1)逻辑思维能力的增强。物理化学实验最后所得的结果往往不是直接测量的到的,而是通过理论分析,推导出一系列理论公式,再由直接测量到的物理量运算而得到的。因此,要求我们在实验中勤于思考,善于分析,充分发挥想象力,不断提高思维的逻辑性。
(2)自学能力的提高。物理化学实验是为大学二、三年级开设的一门独立课程,因此有条件多方面来培养学生的自学能力,包括自学教材和实验仪器说明书的能力和习惯,整理、归纳、综合和评价知识的能力,查找文献资料以及使用多种工具书和手册获取所需的新知识的能力。
(3)科学研究能力的培养。主要是通过科研实践培养研究和解决问题的创新能力。物理化学实验加强了这方面的初步训练,包括包括实验研究方案的设计,实验研究方法的比较,实验要求方面的选择,实验数据的正确记录和处理,相关文献资料的查阅,实验研究结果的分析、总结和归纳,实验研究报告的书写等基本科学研究能力的训练,为毕业论文和科研实践打下基础。
总之,这次物化实验对我影响很大,使我学会了很多东西,丰富了我自身的经历,开阔了眼界,加深了我对物理化学实验的认识,终将受益一生。
第二篇:物理化学实验总结
物理化学实验总结
实验一 液体饱和蒸气压的测定
本实验方法是否用于测定溶液的蒸汽压,为什么?
我觉得不能用来测定溶液的蒸汽压,因为蒸汽中混有水蒸气,影响测量结果(不知道对不对)
实验的的改进:
采用蒸馏水代替异丙醇,因为异丙醇是有毒.有刺激性的气体。如果长期使用会对师生的身体健康产生威胁,还会污染实验室的环境。用蒸馏水代替异丙醇后不仅降低了原料的成本,又保护了实验室的环境,对师生的身体健康也是有益的。
实验二 燃烧热的的测定
实验关键:点火成功、试样完全燃烧是实验成败关键,可以考虑以下几项措施:
①试样应进行磨细、烘干、干燥器恒重等前处理,潮湿样品不易燃烧且有误差。
压片紧实度:一般硬到表面有较细密的光洁度,棱角无粗粒,使能燃烧又不至于引起爆炸性燃烧残剩黑糊等状。
②点火丝与电极接触电阻要尽可能小,注意电极松动和铁丝碰杯短路问题。
③充足氧(2MPa)并保证氧弹不漏氧,保证充分燃烧。燃烧不完全,还时常形成灰白相间如散棉絮状。
实验的的改进:
在此次实验中,通常将点火电流控制旋钮事先测试并固定在第十个数据,这种处理方法长会出现电流过小或过大.点火的时间过短或过长的现象,可将点火电流控制旋钮在点火之前至最小值,按下点火键后,在将点火电流控制转钮匀速的向电流增加的方向旋转,并将点火时间控制在5s以内,在点火指示点火结束后,终止点火。这样控制点火电流,使燃烧丝有一个在小电流下预热.发亮的过程,同时也使药品受到预热而易被点燃,在较高压力氧气存在的条件下,红热的燃烧丝立即被高温氧化,耐火度迅速提高,在较高电流作用下,燃烧丝才会熔断,从而提高药品连同燃烧丝一起被烧掉的机会,提高点火功率。
实验三 最大气泡压力法测定液体表面张力
最大气泡法测表面张力实验中,理论计算所得值与实验测得数值存在偏差的因素是什么?
1:首先要保证装置不能有一点点漏气,所以在玻璃装置的某些接口处涂点凡士林。
2:要保证毛细管尖端的洁净与完好无损,但实际中总是会有点缺陷,如果将毛细管尖端换成是一次性的东西,然后再与毛细管相连,但这样之后就可能不能保证整个毛细管的垂直,所以不知道可不可行。
3.本实验还有一个问题,就是要求毛细管与液面相切,但实际中可能做不到;但伸入液面△h的话,测出来的又不是表面的张力,所以不知道这个问题还不知道怎么解决。
实验四 蔗糖水解反应速率常数的测定
1.WXG-4圆盘旋光仪的正确使用方法
1. 准备工作
1)先把预测溶液配好,并混合均匀;
2)把预测溶液盛入试管待测。但应注意试管两端螺旋不能旋得太紧(一般以随手旋紧不漏水为止),以免护玻片产生应力而引起视场亮度发生变化,影响测定准确度,并将两端残液揩拭干净;
3)接通电源,约点燃10min,待完全发出钠黄光后,才可观察使用;
4)检验度盘零度位置是否正确,如不正确,可旋松度盘盖四只连接螺钉、转动度盘壳进行校正
2. 测定工作:
1)打开镜盖,把试管放入镜筒中测定,试管内不应有气泡,否则会影响观察和测定;
2)调节视度螺旋至视场中三分视界清晰时止;
3)转动度盘手轮,至视场照度相一致时止;
4)从放大镜中读出度盘所旋转的角度;
2.蔗糖水解反应速率常数的测定中为什么可以用粗天平称取反应物蔗糖的用量 ?
答:因为蔗糖水解为一级反应,反应物起始浓度不影响反应速度常数,还有实验中用到的蔗糖是普通的食用蔗糖,品质较差,里面混有比较多的杂质,纯度不是很高。所以,用粗天平称取蔗糖用量。因为即使用精密度很高的天平称蔗糖也没有太大意义。
实验心得:通过这四个物理化学实验使我掌握了物理化学实验的的基本方法和技能,根据所学的内容设计实验,正确的选择和使用仪器。重要的是如何应用计算机软件进行数据模拟.数据分析等(学会了originr软件求斜率,excel绘图等),培养了我们正确的观察现象,记录数据以及分析式样的结果能力,还培养我们严肃认真.实事求是的科学态度。通过物理化学的实验加深和巩固了对所学的知识的理解,还提高了我们团队协作的能力。
-
物理化学实验总结
闽江学院化学与化学工程系10级应化(2)班柳泽玲120xx1202240通过这个学期的大学物化实验,我体会颇深。首先,我通过做实验…
-
物理化学实验总结
材料与冶金学院45-4-08白树华实验一液体饱和蒸气压的测定本实验方法是否用于测定溶液的蒸汽压,为什么?我觉得不能用来测定溶液的蒸…
-
物化实验总结
物化实验总结10环科林泽震120xx1202126大二的生活已经临近尾声了,伴随着我们走完一学期的物化实验也结束了。通过这一学期来…
-
物理化学实验结课总结
物理化学实验总结报告物理化学实验结课了,在本学期中,我们总共做了8个实验,应当说收获颇丰。首先由于实验室条件所限,所以我们采用了两…
-
物理化学实验心得
物理化学实验心得应用化学102班谢叔尧5503210114经过了大三上半学期物理化学基础知识到底学习这学期开设了物理化学实验这门课…
-
化学实验室工作总结
化学实验是化学教学中学生获得化学知识和检验化学知识的重要媒体和手段,能为学生形成化学基本概念和化学基础理论提供感性认识的材料,能激…
-
20xx年上半年初中化学实验室工作总结
普安中学吴盛旭蔡娟实验室工作是一个繁琐的工作,每学期初制定初步工作计划,根据教师的教学进度表制定这一学期的分组实验和演示实验的安排…
-
初中化学实验室工作总结
本学期在学校各级领导及学科教师的关心、配合下,学校化学实验室管理工作顺利完成。作为实验管理员来说,也从思想到行动,从理论到实践的一…
-
初中化学实验总结及练习题
1、蜡烛燃烧实验(描述现象时不可出现产物名称)(1)火焰:焰心、内焰(最明亮)、外焰(温度最高)(2(3)检验产物H2O:用干冷烧…
-
20xx-20xx学年度上学期九年级化学教学总结
20xx-20xx学年度第一学期九年级化学教学工作总结西冲镇中学:周圣华本学期我担任九(3)班的化学教学工作。化学是九年级新开的学…
-
物理化学学习总结
学习物理化学已经有一学年的时间了,感触颇深,早在以前就听说物理化学是化学基础课中的难点,因为学习这么门课有它自身的学习方法,与其他…