环己酮的制有机化学实验报告
有 机 化 学 实 验 报 告

实 验 名 称:环己酮的制备
学 院:化工学院
专 业:化学工程与工艺
班 级
姓 名: 学 号
指 导 教 师:房江华、李颖
日 期:
一、 实验目的:
1、学习次氯酸氧化法制环己酮的原理和方法;
2、进一步了解醇和酮之间的联系和区别。
3、学习搅拌反应装置。
二、实验原理:
用次氯酸钠作氧化剂,将环己醇氧化成环己酮。
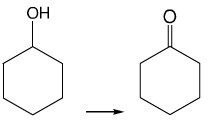
三、主要试剂及物理性质:
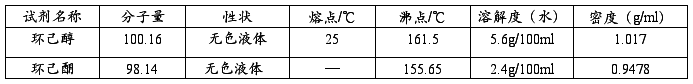
四、实验试剂及仪器:
药品:环己醇5g(5.2ml),冰醋酸,次氯酸钠溶液(约1.8mol/l),饱和亚硫酸氢钠溶液,氯化铝,碘化钾淀粉试纸,无水碳酸钠,氯化钠,无水硫酸镁,沸石。
仪器:250ml三颈烧瓶,搅拌器,低液漏斗,温度计,冷凝管,接收管,分液漏斗。
五、仪器装置:
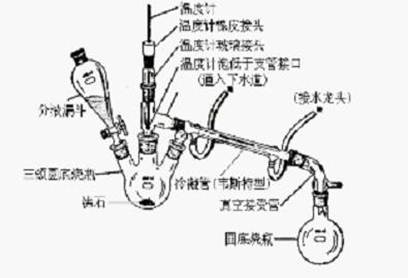
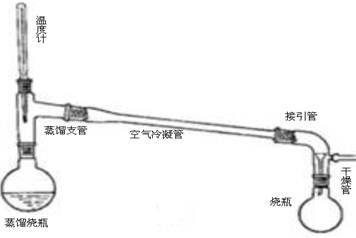
六、实验步骤及现象:
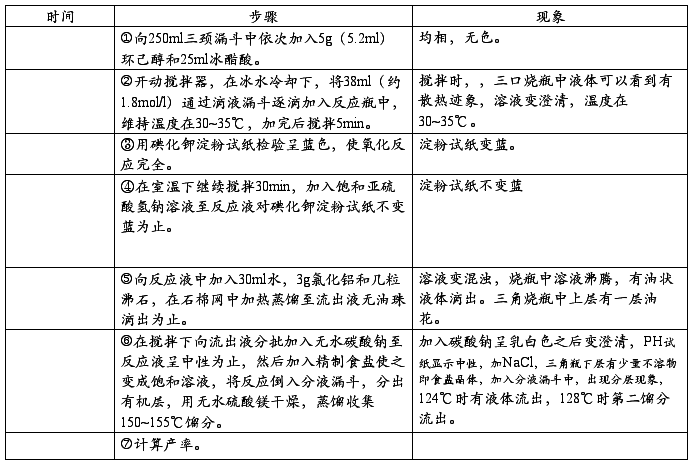
七、数据处理与实验结果:

m'=M(环己酮)×(V(环己醇)×P(环己醇))/M(环己酮)=98.14×(5.2×1.017)/100.16=5.65g
产率=m/m'×100%(四组合为一组,所以要除上4)
八、注意事项:
a在实验室步骤②中当温度不满足30~35℃时,需要用电炉加热温度高时,要用冰水降温。
b电炉加热时,烧瓶要离石棉网有一定距离,不能贴牢,以防爆炸。
c当步骤③中淀粉碘化钾试纸变蓝后又无色,需要加适量NaClO。
d蒸馏时要加几粒沸石。
e加NaClO时速度要适当慢一些。
f分层时要注意自己取的是哪一层。
g蒸馏时仪器要干燥。
九、实验讨论及误差分析:
①在对三口烧瓶中液体进行第一次蒸馏时,由于暴沸冲开瓶盖,使液体溅出;
②防暴沸要用好一点的沸石,以防暴沸伤人;
③加入粗食盐是为了降低环己酮在水中的溶解度并有利于环己酮的分层。
第二篇:环己酮的制备实验报告
??大学实验报告
20##年11月19日
姓名/////////// 系年级2010级应用化学系 组别 30 同组者???
科目有机化学 题目 环己酮的制备 仪器编号 30
一、 实验目的
1、 学习铬酸氧化法制备环己酮的原理和方法。
2、 通过醇转变为酮的实验,进一步了解醇和酮的联系和区别。
二、 实验原理
实验室制备脂环醛酮,最常用的方法是将伯醇和仲醇用铬酸氧化。铬酸是重要的铬酸盐和40%~50%硫酸的混合物。仲醇用铬酸氧化是制备酮最常用的方法。酮对氧化剂比较稳定,不易进一步氧化。铬酸氧化醇是一个放热反应,必须严格控制反应的温度,以免反应过于剧烈。反应方程式为:

三、 主要物料及产物的物理常数
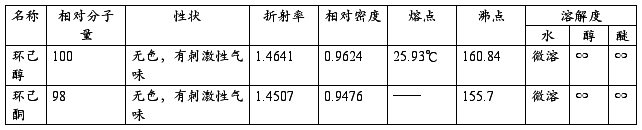
四、 主要物料用量及计算
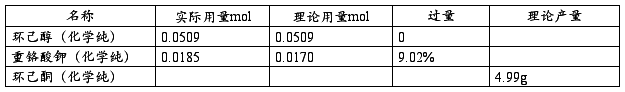
五、 实验装置
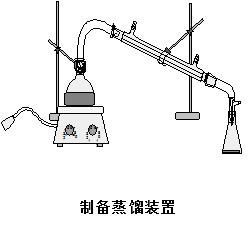
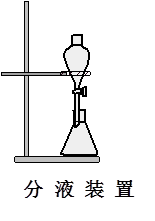
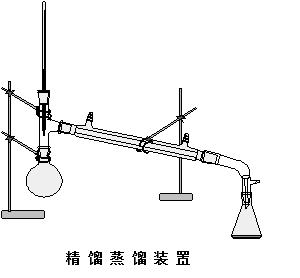
六、 实验步骤
1、配制铬酸溶液:在200mL烧杯中加入30mL水和5.5g重铬酸钠,搅拌使之全部溶解。然后在搅拌下慢慢加入4.5mL浓硫酸,将所得橙红色溶液冷却到30℃以下备用;
2、250mL圆底烧瓶中加入5.3mL环己醇,然后一次加入配制好的铬酸溶液,并充分振摇使之混合均匀。用水浴冷却,控制反应温度在55~60℃。当温度开始下降时移去冷水浴,室温下放置0.5h,其间要间歇振摇反应瓶;
3、反应完毕后在反应瓶中加入30.0mL水和几粒沸石,改成蒸馏装置进行蒸馏。将环己酮和水一起蒸出来,直至馏出液不再浑浊再多蒸8~10mL,约收集馏出液25mL。
4、将馏出液用食盐饱和后转入分液漏斗中,分出有机相。水相用7.5mL乙醚提取一次,将乙醚提取液和有机相合并,用1~2g无水碳酸钾干燥;在水浴上蒸除乙醚,换空气冷凝管,蒸馏收集151~155℃馏分。
5、称量产品。纯粹环己酮沸点155.7℃,d420为0.9476,折射率n420为1.4507.
七、实验记录
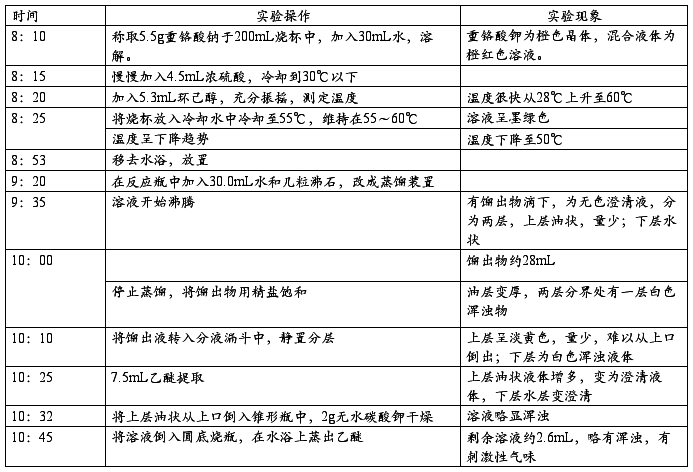
八、产率计算
实际产品质量:2.5g
理论产品质量:4.99g
产率=(实际产品质量/理论产品质量)*100%=(2.5/4.99)*100%=50.1%
九、讨论
本实验中,铬酸氧化醇是一个放热反应,需要严格控制温度以防反应过于剧烈,用冷水和热水来维持;温度过高副反应增多,温度过低反应困难。干燥时时间要充分,否则溶液中含水浑浊,造成蒸馏时达不到预定温度。
-
有机化学实验实验报告
实验一有机化学实验基本操作实验目的1使学生明白进入有机化学实验学习必须阅读有机化学实验的一般知识的内容及安全实验是有机化学实验的基…
-
有机化学实验报告模板
有机化学实验报告专业班级学号姓名实验名称实验时间年月日学生姓名同组人姓名第一部分实验预习报告一实验目的二实验原理包括实验装置简图三…
-
有 机 化 学 实 验 报 告
学院:化学工程学院专业:化学工程与工艺班级:姓名:李云龙学号104020xx224指导教师:肖勋文王冠南日期:20xx年x月x日实…
-
有机化学实验报告格式
实验学专班姓指导日机化学实验报告业化学工程与工艺教有一二三主要试剂及物理性质四试剂用量规格五仪器装置六实验步骤及现象七实验结果八实…
-
有机化学实验报告
实验学专班姓指导日机化学实验报告名称熔点测定院化工学院业化学工程与工艺级名学号教师房江华李颖期有一实验目的1了解熔沸点测定的意义2…
-
有机化学实验报告:环己酮的制备
环己酮的制备华南师范cai前言环己酮无色透明液体分子量9814密度09478gmL熔点164C沸点15565C在水中微溶在乙醇中混…
-
聚己内酰胺的制备实验报告
聚己内酰胺的制备三主要试剂和产物的物理常数四实验装置图五实验步骤和现象六实验结果七注意事项八问题与讨论1因为环己酮肟的纯度对反应有…
-
环己酮的制备实验报告
20xx年11月19日姓名系年级20xx级应用化学系组别30同组者科目有机化学题目环己酮的制备仪器编号一实验目的1学习铬酸氧化法制…
-
环己酮的制备实验报告
实验学专班姓指导日机化学实验报告名称环己酮的制备院化学工程学院业化学工程与工艺级化工124班名王伟杰学号124020xx414教师…
-
环己酮的制备实验报告
实验学专班姓指导日机化学实验报告名称环己酮的制备院化学工程学院业化学工程与工艺级化工106班名严晓晓学号104020xx602教师…
-
环己酮的制备实验报告(4)沈杰
实验学专班姓指导日机化学实验报告名称院化学工程学院业化学工程与工艺级化工114班名沈杰学号114020xx417教师肖勋文何炎军期…