高一化学必修1化学方程式及离子方程式汇总(背诵版)
高一化学必修1重要方程式及离子方程式汇总(精选)

常见离子检验:
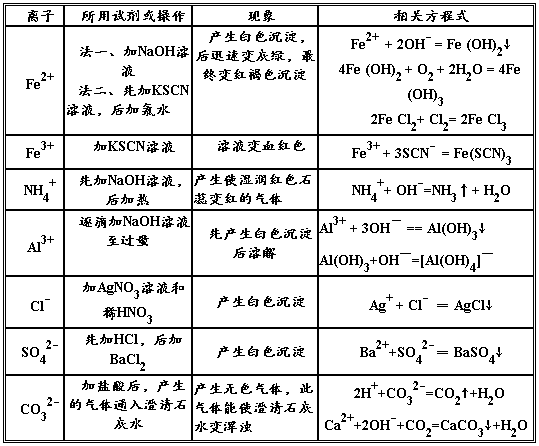
第二篇:s高一化学必修1重要方程式及离子方程式汇总(精选)沙县一中罗仙福整理

高一化学必修1重要方程式及离子方程式汇总(精选)沙县一中罗仙福整理
序号 1 2
化学方程式
2Na+2H2O=2NaOH+H2↑ Na 与CuSO4 溶液 2Na+2H2O=2NaOH+H2↑
2NaOH+ CuSO4=Cu(OH)2↓+ Na2SO4 2Na2O2+2H2O=4NaOH+O2↑ 2Na2O2 + 2CO2 = 2Na2CO3 + O2 点燃
2Fe + 3Cl2 2FeCl3
Cl2 + H2O = HCl + HClO
离子方程式
2Na + 2H2O == 2Na+ + 2OH- + H2↑ +-
2Na + 2H2O == 2Na + 2OH + H2↑
Cu+2OH== Cu(OH)2↓
2Na2O2+2H2O =4Na+4OH+O2↑ 过氧化钠可用在呼吸面具和潜水艇中作供氧剂 铁在氯气中剧烈燃烧(棕红色烟) Cl2 + H2O = H+ + Cl - + HClO Cl2+ 2OH-=ClO-+ Cl -+H2O 工业制漂白粉 MnO2 +4H+2Cl
3+
-+
-
+
-
2+
-
3 4 5 6 7 8 9 10 11 12
2NaOH+Cl2 =NaClO+NaCl+H2O 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O 实验室制Cl2 ::
MnO2 +4HCl(浓) MnCl2+Cl2↑+2H2O FeCl3 + 3NaOH = Fe(OH)3 ↓+3NaCl 4Fe (OH)2 + O2 + 2H2O = 4Fe (OH)3 氯化亚铁溶液中通入氯气(或加氯水) Cl2 +2FeCl2 =2FeCl3
2FeCl3+Fe = 3FeCl2
FeCl3溶液腐蚀铜板做印刷线路板: FeCl3 +Cu=2FeCl2+Cu Cl2 3Fe+4H2O(g)
高温
Mn+Cl2↑+2H2O
2+
Fe + 3OH = Fe(OH)3 ↓
氢氧化亚铁在空气中被氧化(白色沉淀变为红褐色沉淀)
2 Fe + Cl2 = 2 Fe
2+
3+
+ 2Cl-
13 14
2Fe3+ + Fe = 3Fe2+
2Fe3++Cu= 2 Fe2++Cu2+
15 16 17 18 19 20 21
Fe3O4+4H2
Fe粉与水蒸汽反应
CO32- + 2H+ = H2O + CO2↑ HCO3-+H+ = H2O +CO2↑
小苏打受热分解(可鉴别Na2CO3与NaHCO3)
HCO3-+ OH - = H2O + CO32-
Na2CO3+2HCl = 2NaCl+ H2O+CO2↑ NaHCO3+HCl=NaCl+H2O+CO2↑ 2NaHCO3
△
Na2CO3 + H2O +CO2↑
NaHCO3 + NaOH = Na2CO3 + H2O
22
--2+2-
2NaHCO3+Ca(OH)2=Ca CO3↓+Na2CO3+2 H2O 2HCO3+2OH +Ca= Ca CO3↓+CO3+
2 H2O
向澄清石灰水中不断通入CO2至过量:
2+-
(先浑浊):Ca(OH)2+CO2=Ca CO3↓+H2O Ca+2OH +CO2=Ca CO3↓+H2O (后澄清):Ca CO3↓+CO2+ H2O=Ca(HCO3)Ca CO3+CO2+H2O=Ca2++2HCO3- 2
CO2+NH3+NaCl+H2O=NaHCO3↓+NH4Cl 侯氏制碱法:向饱和NaCl溶液中先通入NH3后通
CO2 △
2NaHCO3 Na2CO3 + H2O +CO2 ↑
集全国化学资料精华,按“四套教材(旧人教版、新课标人教版、苏教版、鲁科版)目录、知识体系”编排。资源丰富,更新及时。欢迎上传下载。 第1页

序号 23 24 25 26 27 28 29 30 31 32 33
4HNO3(浓)+C 34 35 36 37 38 39 40 41 42 43 44 45
4HNO3
化学方程式
向Na2CO3溶液中通入CO2
Na2CO3+CO2+ H2O=2NaHCO3
C+ CO2
△
离子(化学)方程式
CO32-+CO2+ H2O=2HCO3- 高炉练铁主要反应:
3CO+Fe2O3=3CO2+ 2Fe
Ca CO3+2H+=Ca2++CO2↑+ H2O
N2 + O2 = 2NO 2NH4Cl + Ca(OH)2
△
2CO
石灰石与盐酸反应制CO2 :Ca CO3+2HCl=Ca Cl2 +CO2↑+ H2O N2+3H2
催化剂 高温高压
2NH3
3NO2+H2O=2HNO3+NO 4NO2 +O2 + 2H2O NH3+HCl=NH4Cl(白烟)
4NO2↑+O2↑+2H2O
4HNO3
CaCl2 + NH3↑ + H2O
4HNO3
4NO +3O2 + 2H2O NH4HCO3
△

NH3↑+H2O+CO2↑
(NH4)2CO △
2NH3↑+H2O+CO2↑
Fe与浓HNO3加热
Fe+6 HNO3(浓)= Fe(NO3)3+ 3NO2↑+3H2O Fe与稀HNO3反应
Fe+4HNO3(稀)= Fe(NO3)3+ NO↑+2H2O
△
+-3+
Fe+6H+3NO3== Fe + 3NO2↑+ 3H2O
+-3+
Fe+4H+NO3== Fe + NO↑+ 2H2O 4H+4NO3+C
+
-
4HNO3(浓)+Cu=Cu(NO3)2+2NO2↑+2H2 O 8HNO3+3Cu=3Cu(NO3)2+2NO↑+4H2O
CO2↑+4NO2↑+2H2O
△
CO2↑+4NO2↑+2H2O
2NO3- + Cu + 4H+ == Cu2+ + 2NO2↑+ 2H2O 2NO3- + 3Cu + 8H+ == 3Cu2+ + 2NO↑+ 4H2O 催化剂
2SO2+O2加热 2SO3
SO2+H2O=H2SO3
Cl2 + SO2 + 2H2O == 2Cl- + SO42- + 4H+
S+Fe
△
△
2S S+O2
点燃
SO2
SO2 + 2H2S=3S+2H2O
Cl2+SO2 +2H2O=H2SO4 +2HCl (Cl2可换成Br2或I) 2NaOH+SO2(少量)=Na2SO3+H2O
SO2 + 2OH- == SO32- + H2O
2 + OH- == HSO3- SONaOH+SO2(足量)=NaHSO3
Na2SO3+H2SO4= Na2SO4+ SO2↑+ H2O(实验室制 SO32- + 2H+ == SO2↑+ H2O SO2) △
△ 2H2SO4(浓 CuSO4+SO2↑+2H2O
C+2H2SO4(浓)2↑+2SO2↑+2H2O
△
Mg + 2H2O = 2Mg(OH)2↓ + H2↑ 2H2SO4(浓 2↑+2H2O 2Mg +CO2
点燃
2MgO+C
现象:发出耀眼白光,试管壁纸生成黑色小颗粒
Mg(OH)2 + 2H+ = Mg2+ + 2H2O
Cl2 + 2Br = Br2 + 2Cl
-
-
海水中提镁
Mg2+ +Ca(OH)2(石灰乳)= Mg(OH)2↓+Ca2+ Mg(OH)2 + 2HCl = MgCl2 +2H2O MgCl2(熔融)= Mg+Cl2↑
海水中提溴:Cl2 + 2NaBr = Br2 + 2NaCl
46
集全国化学资料精华,按“四套教材(旧人教版、新课标人教版、苏教版、鲁科版)目录、知识体系”编排。资源丰富,更新及时。欢迎上传下载。 第2页

序号 47 48 49 50 51 52 53 54 55 56 57 58 59 60 61 62 63 64 65 66 67 68 69
△
化学方程式
Cl2 + 2KI =2KCl + I2 2C+SiO制得粗硅)
-
离子(化学)方程式
Cl2 + 2I == 2Cl + I2 △ △
Si(粗)+2Cl2 SiCl4 SiCl4+2H2 Si(纯)+4HCl
-
+ H2O == SiO32- + 2H2↑ Si + 2OH
-
Si+2NaOH+H2O=Na2SiO3+2H2↑ 4HF+SiO2=SiF4+2H2O
SiO2+2NaOH=Na2SiO3+H2O (不能用玻璃塞装碱液) SiO2+Na2CO3
高温
工业上用HF(氢氟酸)刻蚀玻璃
SiO2 + 2OH == SiO3 + H2O
高温
SiO2+CaCO3CaSiO3+CO2(工业制玻璃)
-
2-
Na2SiO3+CO2(工业制玻璃)
Na2SiO3 + CO2 + H2O == H2SiO3↓+ Na2CO3 4Al+3O2(纯氧)
点燃
SiO32- + CO2 + H2O == H2SiO3↓+ CO32- 2Al+Fe2O3
—
2Al2O3
高温
2Fe + Al 2O3 (铝热反应:焊接钢轨)
—
2Al+3H2SO4=Al2(SO4)3+3H2↑
2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑
Al2O3+3H2SO4=Al2(SO4)3+3H2O Al2O3+2NaOH+3H2O=2Na[Al(OH)4] 2Al2O3(熔融)
3O2↑ + 4Al
2Al + 6H+ = 2Al3+ + 3H2↑
2Al+2OH+6H2O=2[Al(OH)4]+3H2↑
Al2O3+6H+=2Al3++3H2O
—— AlO+2OH

+3HO=2[Al(OH)]
2
3
2
4
2Al(OH)3
3+
△
Al2O3+3H2O
+
AlCl3+3NH3·H2O=Al(OH)3↓+3NH4Cl (制备Al(OH)3) Al(OH)3+3HCl=AlCl3+3H2O
Al + 3NH3.H2O == Al(OH)3↓+ 3NH4
Al(OH)3+3H+=Al3++3H2O
Al3+ + 3OH- == Al(OH)3↓ AlCl3+3NaOH=Al(OH)3↓+3NaCl
Al(OH)3+OH—=[Al(OH)4]— Al(OH)3+NaOH=Na[Al(OH)4]
Na[Al(OH)4]+ HCl(少量)= Al(OH)3↓+NaCl+H2O [Al(OH)4]—+H+= Al(OH)3↓+H2O Na[Al(OH)4]+4HCl(过量)= AlCl3+NaCl +4H2O 2Na[Al(OH)4]+CO2(少量)= 2Al(OH)3↓+Na2CO3 +H2O
Na[Al(OH)4]+ CO2(足量)= Al(OH)3↓+NaHCO3 2Cu +O △
[Al(OH)4]—+4H+= Al3++4H2O 2[Al(OH)4]—+ CO(少量)=2Al(OH)3↓+CO32-+H2O 2
[Al(OH)4]—+ CO2(足量)=Al(OH)3↓+HCO3- 4CuOCu(OH)2
△
2Cu2O+ O2↑
2Cu +O2+ CO2+ H2O= Cu 2(OH)2CO3
△
CuO + H2O
集全国化学资料精华,按“四套教材(旧人教版、新课标人教版、苏教版、鲁科版)目录、知识体系”编排。资源丰富,更新及时。欢迎上传下载。 第3页
-
高中化学必修1化学方程式总结
1、钠及其化合物的转化关系2②NaCl2①Na2O+2HCl=2NaCl+H2O②2Na+2HCl=2NaCl+H2↑++++Na…
- 高一化学必修1化学方程式及离子方程式汇总(背诵版)
-
高中化学必修一方程式大全
化学方程式一化学方程式总结1硫酸根离子的检验BaCl2Na2SO4BaSO42NaCl2碳酸根离子的检验CaCl2Na2CO3Ca…
-
高中化学必修1化学方程式总结
高中化学必修1化学方程式总结一钠及其化合物的转化关系1钠在空气中燃烧2NaO2点燃Na2O22钠在氧气中燃烧4NaO2点燃2Na2…
-
高一化学必修一化学方程式及离子方程式小结
必修一化学方程式及离子方程式小结1硫酸根离子的检验BaCl2Na2SO4BaSO42NaClSO4BaBaSO42碳酸根离子的检验…
-
高中必修1化学方程式大全
高中化学必修1化学方程式总结1、钠及其化合物的转化关系2②NaCl2①Na2O+2HCl=2NaCl+H2O②2Na+2HCl=2…
-
高一化学必修一第三章化学方程式总结
高一化学必修1化学方程式归纳小结一、钠及其化合物1.钠与氧气:常温:4Na+O2=2Na2O点燃:2Na+O22.钠与水反应:2N…
-
高一化学必修一化学方程式总结
1、钠及其化合物的转化关系①Na2②2①Na2O+2HCl=2NaCl+H2O②2Na+2HCl=2NaCl+H2↑Na2O+2H…
-
高中化学必修1化学方程式总结
1、钠及其化合物的转化关系2②NaCl2①Na2O+2HCl=2NaCl+H2O②2Na+2HCl=2NaCl+H2↑++++Na…
-
必修1化学方程式总结
必修1化学方程式总结1、硫酸根离子的检验:BaCl2+Na2SO4=BaSO4↓+2NaCl2、碳酸根离子的检验:CaCl2+Na…
-
高中化学必修一第三章金属及其化合物化学方程式或离子方程式总汇(完美编辑版)
高中化学必修一第三章金属及其化合物化学方程式或离子方程式总汇第一节金属的化学性质一、钠、镁、铝、铁、铜分别与氧气反应1、4Na+O…