�߶���ѧ�����������ˮ��1Microsoft Word �ĵ�
���⣺������ �����ˮ�⣨��һ��ʱ��
���� ���ڿ� ��� ʱ�� 20##-11-5
�����ˣ� ���꼶 ��ѧ ������
�� �ܵ� ��ʱ �ܵ� ��ʱ
�����鳤ǩ�� �γ�ǩ��
ѧ������ ���
�� ѧϰĿ�
1��������������ˮ��ĸ����������ˮ���ʵ�ʡ�
2���ܹ���������ˮ��֪ʶ�ж�����Һ������ԡ�
3�����տ�ѧ��ѧϰ������
��ѧϰ�ص㡿
����ˮ���ʵ�ʣ�����Һ������Թ��ɼ��ж�
��ѧϰ�ѵ㡿
ѧ��������ʵ������ܽ��������
��ʹ��˵��������ָ����
1Ԥϰ�α� 54�� 56ҳ�������ص����ݣ��ú�ɫ�ʹ��������ѵ㡣
2 ������ɱ���ʱ��ѧ����
3���÷������۽�ѧ���������⣬��ʦ�����ص�֪ʶ��
��ѧ������ѧϰ���ݡ�
һ ̽������Һ�������
̽������ 1 �ⶨ��ͬ����Һ��pH

����ѧ���̡�
̽������2 ���÷��෨�ҳ��ε����������Һ����ԵĹ�ϵ������������Һ����������ε����͵Ĺ�ϵ��
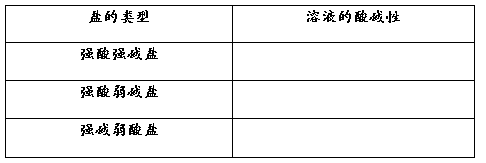
��ϰ ���ж���������Һ������ԡ�
��1��KF��2��FeCl3��3��K2SO4
�� ����Һ���ֲ�ͬ����Ե�ԭ��
̽������3 ��ͬ��������Һ�������Ϊʲô��ͬ�أ�
ʵ�飺�������Ĵ����ơ��Ȼ�李��Ȼ��Ƶľ���ֱ�Ͷ������ʢ������ˮ���Թܣ��ܽ⣬Ȼ����pH��ֽ���Լ��顣
���� CH3COONa pH>7 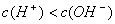
NH4Cl pH<7 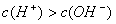
NaCl pH=7 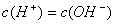
˼���������ơ��Ȼ�臨����Σ���ǿ����ʣ���������ˮ��ȫ��������ӣ�������������м�û�������ӣ�Ҳû�����������ӣ�OH����H���������ʶ�������ˮ�ĵ��룻Ҳ����˵����ˮ���������H����OH�������ʵ���Ũ��������ȵģ�Ϊʲô����ֲ���ȵ�����أ�
�����������Ƶ�����������Ӹ�ˮ���������á�
 CH3COONa === Na�� + CH3COO��
CH3COONa === Na�� + CH3COO��
+
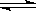 H2O OH�� + H��
H2O OH�� + H��
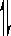
CH3COOH
CH3COO������ˮ��Һ�е������ӽ�������ѵ���Ĵ�����ӣ��Ӷ�ʹˮ�ĵ���������Ӧ�����ƶ�����ʱ��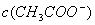 �½���
�½��� ���ߡ�
���ߡ�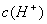 �½��� ʹ��
�½��� ʹ��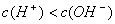 ����Һ�ʼ��ԡ�
����Һ�ʼ��ԡ�
��ѧ����ʽΪ��
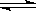 CH3COONa + H2O CH3COOH +NaOH
CH3COONa + H2O CH3COOH +NaOH
ͬ����NH4Cl��Һ�У�
 NH4Cl === NH4+ + Cl��
NH4Cl === NH4+ + Cl��
+
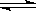 H2O OH�� + H+
H2O OH�� + H+

NH3·H2O
��ѧ����ʽΪ��
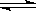 NH4Cl + H2O NH3·H2O + HCl
NH4Cl + H2O NH3·H2O + HCl
1. �����ˮ�⣺
����Һ�����ε����������������ӻ�����������Ӹ�ˮ������������ӻ����������ӽ����������������������ƻ���ˮ�ĵ���ƽ�⣬ʹ��ƽ�������ƶ������������ӻ�����������Ũ�ȵı仯��
��������ˮ��Ӧ��ʵ���ǣ������Ƶ�����Ĵ�������Ӻ�ˮ������������ӽ������������ʴ���Ĺ��̡�
�Ȼ����ˮ��Ӧ��ʵ���ǣ��Ȼ�淋����������Ӻ�ˮ����������������ӽ�������������һˮ�ϰ��Ĺ��̡�
ˮ��Ľ������������ͼ����ε�ˮ�ⷴӦ������кͷ�Ӧ���淴Ӧ��
�ᣫ�� �Σ�ˮ
�Σ�ˮ
�������ܽ �����ˮ��
1�����壺
2������
����ϰ������±���
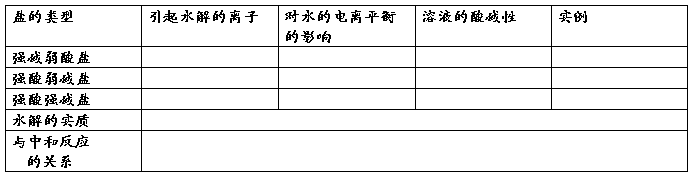
�����ü�⡿
1��_____________________________���������ˮ�⡣
2��NH4Cl��ǿ�������Σ����з���ˮ�������Ϊ________����Һ��_____�ԣ�CH3COONa��ǿ���������У�����ˮ�������_________����Һ��_____�ԡ�
3������ˮ���ʵ��Ϊ���е�__________��ˮ�е�_______������_______��Ӧ.
4���ж���������Һ�������
��1��NaF��2��FeCl3��3��Na2SO4
5��̼������Һ�е����̪�ʺ�ɫ��ԭ���ǣ������ӷ���ʽ��ʾ��
��
6����ʹH2O  H+ + OH-����ƽ������뷽���ƶ�������������Һ�Լ��Ե��ǣ� ��
H+ + OH-����ƽ������뷽���ƶ�������������Һ�Լ��Ե��ǣ� ��
A����ˮ���ȵ�99�棬ʹˮ��pH=6.1 B����ˮ�е���ϡH2SO4
C����ˮ�м���С�մ� D����ˮ�м����Ȼ�������
7����Na2CO3��Һ�У��й�����Ũ�ȵĹ�ϵ��ȷ���ǣ� ����
A��c��Na+����2c��CO32���� B��c��H+����c��OH����
C��c��CO32������c��HCO3���� D��c��OH������c��CO32-��
8����pH=9��NaOH��CH3COONa��Һ�У�����ˮ���������OH-Ũ�ȷֱ�ΪAmol/L��Bmol/L,��A��B�Ĺ�ϵΪ�� ��
A��A>B B. A=10-4B C . B=10-4A D. A=B
����ҵ���á�
Ԥϰ��һ�ڽ�ѧ��
���⣺������ �����ˮ�⣨�ڶ���ʱ��
���� ���ڿ� ��� ʱ�� 20##-11 -5
�����ˣ���� ���꼶 ��ѧ ������
�� �ܵ� ��ʱ �ܵ� ��ʱ
�����鳤ǩ�� ����ΰ �γ�ǩ��
ѧ������ ���
�� ѧϰĿ�
1.�˽�ˮ�ĵ��롢��Һ������ԡ�C(H+)��pH�Ĺ�ϵ
2.����ˮ��ԭ��
3.�˽��ε�ˮ���Ӧ��
��ѧϰ�ص㡿
1. ��������ˮ���ʵ�ʣ��ܳ��������ε�����ж�����Һ������ԡ�
2. ѧ�Ტ��������ˮ������ӷ���ʽ��
3���˽�ָʾ���ı�ɫ��Χ��ѧ����pH��ֽ�ⶨ��Һ��pHֵ��
��ѧϰ�ѵ㡿
1. ��������ˮ���ʵ�ʣ��ܳ��������ε�����ж�����Һ������ԡ�
2. ѧ�Ტ��������ˮ������ӷ���ʽ��
��ʹ��˵��������ָ����
1Ԥϰ�α� 56�� 58ҳ�������ص����ݣ��ú�ɫ�ʹ��������ѵ㡣
2 ������ɱ���ʱ��ѧ����
3���÷������۽�ѧ���������⣬��ʦ�����ص�֪ʶ��
��ѧ������ѧϰ���ݡ�
һ. ����ˮ��Ĺ��ɣ�
������ˮ�⣬������ˮ�⣻
Խ��Խˮ�⣬˭��˭ˮ�⣻
˭ǿ��˭�ԣ�ͬǿ�����ԡ�
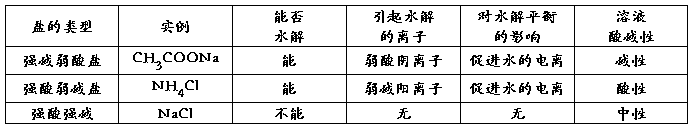
����ѧ���̡�
�� ˮ�����ӷ���ʽ����д��
�� ����ˮ���ǿ��淴Ӧ��Ҫд��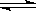 ������
������
�� һ��ˮ��̶Ⱥ�С��ˮ�������٣�ͨ�������ɳ��������壬���á��������������š��������H2CO3��NH3·H2O�ȣ�Ҳ��д�ֽ���
�� ��Ԫ�����ηֲ�ˮ�⣬�Ե�һ��Ϊ����
����K2CO3��ˮ��
��һ����
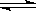

�ڶ�����
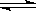
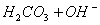
4����ˮ������ӷ���ʽͬ����ѭ�����غ㶨�ɺ͵���غ㶨�ɡ�
����ϰ����ͬѧ���Լ���ϰһ��Na2S��K3PO4��Һˮ�����ӷ���ʽ��д����
5���ڶ�Ԫ�����ˮ��Ҳ�Ƿֲ����еģ���ˮ�ⷽ��ʽһ�㲻�ֲ�д����Al2(SO4)3��ˮ�����ӷ���ʽΪ��
Al3+ + 3H2O 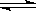 Al(OH)3 + 3H+
Al(OH)3 + 3H+
�����ܽ���ǿ�������Ρ�ǿ�������κ�ǿ��ǿ���ε�ˮ���������ô�����������Ƿ�ˮ���أ���ˮ��̶�����Σ�������Ȥ��ͬѧ�κ�����Լ������й����ϡ�
����ϰ���ж���������Һ������ԣ�����ˮ���д��ˮ�ⷴӦ�����ӷ���ʽ��
NH4NO3 Cu(NO3)2 Na2S FeCl3 NaClO
��. Ӱ������ˮ������أ�
�����ε�������ˮ�е������ӻ����������ӽ�ϵ������Ĵ�С������ε�����Խ�����ε�ˮ��̶�Խ��������ˮ�⣬������ˮ�⣬Խ��Խˮ�⣬˭ǿ��˭�ԡ�
����
�� �¶ȣ�����ˮ�ⷴӦ���кͷ�Ӧ���淴Ӧ�����кͷ�Ӧ�Ƿ��ȷ�Ӧ����ˣ�ˮ�ⷴӦ�����ȷ�Ӧ�����ԣ������¶Ȼ�ʹ�ε�ˮ��̶�����
�� Ũ�ȣ���ҺŨ��ԽС��ʵ������������ˮ��������ʹƽ��������Ӧ�����ƶ���ʹ�ε�ˮ��̶������������ɳ����ԭ����Ũ��ͬʱ��С��ԭ�������ͣ���
3��������������ܴٽ��������ε�ˮ�⡣
�����ü�⡿
1���������ʼ��뵽ˮ�У��ܴٽ�ˮ�ĵ��룬��ҺpH��С���ǣ� ��
A��HCl B. Al2(SO4)3 C . Na2S D.NaOH
2��0.1mol/LNaHCO3��ҺpH��ӽ��ڣ� ��
A��5.6 B.7.0 C .8.4 D.14
3�����ʵ�����ͬ��������Һ�У��������������� �� ��
A��CaCl2 B��CH3COONa C��K2SO4 D��Na2CO3
4���������ʼ������þ���Բ����������ǣ� ��
A��ŨHNO3 B��NaHCO3 C��NH4Cl D��CH3COONa
5������ˮ�������Ϻ������Һ�У�c(NH4+) = c(Cl��)������Һ��pHΪ�� ��
A������7 B��С��7 C������7 D�����ж�
6���ڳ����£���pH=11��ij����Һ��pH=3��ij����Һ�������ϣ�����˵����ȷ���ǣ� ��
A����������Һ�����ԣ������ɵ��ο��ܲ�ˮ��
B�������õ���Һ�ʼ��ԣ������������ɵ���ˮ���ԭ��
C����������Һ�����ԣ��������ǿ����������Һ��Ӧ
D����������Һ��pH=9�������ǿ����������Һ��Ӧ
7. ��0.1 mol·L��1NaOH��Һ��ͨ�����CO2����Һ�д��ڵ���Ҫ������( )
A��Na����CO32�� B��Na����HCO3�� C��HCO3����CO32�� D��Na����OH��
8�����ʵ���Ũ����ͬ��������Һ�У�NH4+Ũ�������ǣ� ��
A.NH4Cl B.NH4HSO4
C.CH3COONH4 D.NH4HCO3
9. (05�Ϻ�)��ʹ0.1mol/L��NaHCO3��Һ��c(H+)��c(CO32¯)��c(HCO3��)�����٣��䷽����( )
A. ͨ�������̼���� B. �����������ƹ���
C. ͨ���Ȼ������� D. ���뱥��ʯ��ˮ��Һ
10��CH3COOH��CH3COONa�����ʵ���������Ƴɵ�ϡ��Һ��pHΪ4.7������˵���������
A.CH3COOH�ĵ������ô���CH3COONa��ˮ������
B.CH3COONa��ˮ�����ô���CH3COOH�ĵ�������
C.CH3COOH�Ĵ���������CH3COONa��ˮ��
D.CH3COONa�Ĵ���������CH3COOH�ĵ���
11��������Һ�и������ӵ����ʵ���Ũ�ȴ�С��ϵ�ܹ�ȷ�����ǣ� ��
A.c(K��)��c(Al3+) B.c(K��)��c(Al3+)
C.c(H��)��c(OH��) D.c(Al3��)��c(H��)
12��Ϊ��ͬʱ��ijũ����ʩ�÷ֱ���N��P��K����Ԫ�صĻ��ʣ����ڸ����Ļ��ʣ�
��K2CO3 ��KCl ��Ca(H2PO4)2 ��(NH4)2SO4 �ݰ�ˮ�����ʺϵ������ ( )
A���٢ۢ� B.�ڢۢ� C.�٢ۢ� D.�ڢۢ�
13 ����˵����ȷ���ǣ� ��
A. ��ʽ�ε�ˮ��Һһ���Լ��ԡ�
B. ֻҪ��ͼ�����ʵ���Ũ�Ⱥ�����ֱ���ȣ����Ƿ�Ӧ�����Һ�ͳ����ԡ�
C. ��ˮ����������Ϊˮ�������ӵ����ʵ���Ũ�Ⱥ����������ӵ����ʵ���Ũ����ȡ�
D. ̼����Һ�������ӵ����ʵ���Ũ����̼������ӵ����ʵ���Ũ�ȵ�2����
14���ڴ�����Һ�е����̪����Һ��졣���ڸ���Һ���ٵ���������Ȼ�����Һ�����۲쵽��������____________________________________________����ԭ����(�����ӷ���ʽ�ͼ�Ҫ����˵��)��_______________________________________ ��
����ҵ���á�
Ԥϰ��һ�ڽ�ѧ��
���⣺������ �����ˮ�⣨������ʱ��
���� ���ڿ� ��� ʱ�� 20##-11-5
�����ˣ���� ���꼶 ��ѧ ������
�� �ܵ� ��ʱ �ܵ� ��ʱ
�����鳤ǩ�� ����ΰ �γ�ǩ��
ѧ������ ���
�� ѧϰĿ�
1.�˽�����ˮ���������������е�Ӧ�á�
2.�˽�����ˮ���ڻ�ѧʵ��Ϳ�ѧ�о��е�Ӧ�á�
3.������Һ������Ũ�ȵĴ�С�Ƚ����⡣
��ѧϰ�ص㡿
1.�˽�����ˮ���������������е�Ӧ�á�
2.�˽�����ˮ���ڻ�ѧʵ��Ϳ�ѧ�о��е�Ӧ�á�
��ѧϰ�ѵ㡿
������Һ������Ũ�ȵĴ�С�Ƚ����⡣
��ʹ��˵��������ָ����
1Ԥϰ�α� 56�� 58ҳ�������ص����ݣ��ú�ɫ�ʹ��������ѵ㡣
2 ������ɱ���ʱ��ѧ����
3���÷������۽�ѧ���������⣬��ʦ�����ص�֪ʶ��
��ѧ������ѧϰ���ݡ�
1���ô�����Һ��ϴ����ʱ�� ����ǿȥ��������
2�����ʵ�ʩ��
���磺��ľ�����̬���ʲ��ܻ��ʩ�ã������ʹ��Ч��ġ����������η���ˮ����ٽ���Ӧ�ų�������Ե�ʡ�
3������Һ������
���磺����FeCl3��SnCl2��ҺʱӦ�����������ᣬĿ����
4����������ˮ��
���磺����FeCl3��������ˮ��Һ�з���ˮ������Ľ��壬������ˮ�����������ʣ���ˮ�����á�
5����ĭ�����ԭ��
Al2(SO4)3��Һ��С�մ���Һ����ˮ����ٽ���Ӧ������ ����ȼ��������������뿪�������ӷ���ʽΪAl3����3HCO3��===Al(OH)3����3CO2����
6������ˮ�ⷴӦ�������ײ���(��������ɱ�Ϊ������)
TiCl4��(x��2)H2O(����)���TiO2·xH2O����4HCl
TiO2·xH2OTiO2��xH2O
����ѧ���̡�
����ˮ����ۺ�Ӧ��
(1) �ж�����Һ���������pH
���磺�� ��ͬ���ʵ���Ũ�ȵ���ҺpH��
NaAlO2>Na2CO3>NaHCO3>NaCl>CuCl2��
�� ��pH��ֽ����NH4Cl(����)��NaCl(����)��CH3COONa(����)��
(2) �ж��ζ�Ӧ��������ǿ��
���磺֤��CH3COOHΪ�������ķ�����ȡ����CH3COONa��������ˮ����pH��ֽ������Һ��pH>7��
(3) ������������Һ��������
��
�� ˮ�����ɻӷ��������(��AlCl3)�������� ������
�� �ϵ��¶������ȷֽ����[��Ca(HCO3)2]�εķֽ����
(4) ����������Һ��Ӧ����H2
���磺����þ��FeCl3��AlCl3��NH4Cl��Һ���ܷ�Ӧ����H2����Ϊ��Щ��ˮ�������ԡ�
(5) �ж���Һ�������ܷ�
���磺Al3����Fe3����CO32����HCO3����Ϊ�ܷ���ˮ����ٽ���Ӧ������Һ�в��ܴ������档
(6) �ж�����Һ�������������(��Na3PO4��Һ�д�����Щ����)��
(7) ���ü��ȵķ������ٽ���Һ��ijЩ�ε�ˮ�⣬ʹ֮������������������Գ�ȥ��Һ��ijЩ�������ӡ����磬������KNO3��Һ�г���������Fe3�������ü��ȵķ�������ȥKNO3��Һ��������Fe3����
(8) ��ĭ�����ԭ��
Al2(SO4)3��Һ��С�մ���Һ����ˮ����ٽ���Ӧ������CO2�����Al(OH)3��������ȼ��������������뿪�������ӷ���ʽΪAl3����3HCO3��===Al(OH)3����3CO2����
(9) ���ʵĺ���ʹ��
���̬�������ľ��(��Ҫ�ɷ���K2CO3)���ܻ��ʩ�á���ΪNH4����ˮ��Һ���ܷ���ˮ������H����CO32����ˮ��Һ��ˮ�����OH����������ͬʱ����ʱ�������ˮ�������H����OH- �ܷ����кͷ�Ӧ��ʹˮ��̶ȶ��������ˮ�����NH3·H2O�ӷ��������˷�Ч��
�������ܽ
������Ũ�ȴ�С�ıȽϹ���
(1) ��Ԫ������Һ
���ݶಽ������������磺��H2CO3����Һ�У�c(H��)>c(HCO3��)>c(CO32��)��
(2) ��Ԫ�����������Һ
����������ķֲ�ˮ��������磺Na2CO3��Һ�У�c(Na��)>c(CO32��)>c(OH��)>c(HCO3��)��
(3) ��Ԫ�������ʽ����Һ
Ҫ����������ӵĵ���̶���ˮ��̶ȵ���Դ�С����HCO3����ˮ��Ϊ����NaHCO3��Һ��c(Na��)>c(HCO3��)>c(OH��)>c(H��)����HSO3���Ե���Ϊ���� NaHSO3��Һ��
c(Na��)>c(HSO3��)>c(H��)>c(OH��)��
(4) ��ͬ��Һ��ͬһ����Ũ�ȵıȽ�
Ҫ����Һ���������Ӷ���Ӱ������ء����磺����ͬ���ʵ���Ũ�ȵ�������Һ�У�a.NH4Cl��b.CH3COONH4��c��NH4HSO4��c(NH4��)�ɴ�С��˳����c>a>b��
��5)�����Һ�и�����Ũ�ȵĴ�С�Ƚ�
���ݵ���̶ȡ�ˮ��̶ȵ���Դ�С������
�� ���ӵĵ��������Ӧ���ӵ�ˮ��
���� �������ʵ���Ũ�ȵ�NH4Cl��NH3·H2O�����Һ��
c(NH4��)>c(Cl��)>c(OH��)>c(H��)��
�� ���ӵĵ���С����Ӧ���ӵ�ˮ��
���磺��0.1 mol·L��1��NaCN��0.1 mol·L��1��HCN��Һ�Ļ��Һ�У�������Ũ�ȵĴ�С˳��Ϊc(Na��)>c(CN��)>c(OH��)>c(H��)��
(6) �����غ����
ԭ�ӣ��������غ�
����غ�
�����غ�
�����ü�⡿
1����������������ˮ���ص���(���� )
A����ĭ������еķ�Ӧԭ��
B����ľ��(��Ҫ�ɷ�K2CO3)��Ϊũ������ϲ������̬���ʻ���
C��������Ư�۳���Ϊ�����������
D��CuSO4��ʹ�����ʱ���
2�������й�����������ˮ���ٽ�����Һ���ȣ������ᾧ�������գ��ܵõ���ѧ�����ԭ����������ͬ����(���� )
�ٵ����� ���Ȼ����� �������� ����Na2CO3�� ��NaHCO3 ���Ȼ�ͭ
A���ۢ� B���٢ۢ� C���٢ڢۢܢ� D��ȫ��
3 ����ʵ������ܴﵽĿ�ĵ���(˫ѡ)(���� )
A����Na2S��Һ��Al2(SO4)3��Һ��Ӧ�Ƶ�Al2S3����
B���ü�������K2CO3��Һ�ķ������K2CO3����
C����Na2S��Һ��CuSO4��Һ��Ӧ�Ƶ�CuS����
D������MgCl2��Һ�Ƶ�MgCl2����
4������������Һ���ܴ����������(�� ��)
A��Na����Fe2����SO42����NO3����������
B��Fe3����K����Cl����CO32��
C��Al3����Na����SO42����AlO2��
D��Ca2����H����NO3����SO32��
5����������������ɲ�����(����400 ��)�������ʵ���Һ�����Եõ��ù������ʵ���(���� )
A���Ȼ��� B��̼������ C�������� D���������
6 ����Ũ�ȹ�ϵ��ȷ����(�� ��)
A����ˮ�У�c(Cl2)��2[c(ClO��)��c(Cl��)��c(HClO)]
B����ˮ�У�c(Cl��)>c(H��)>c(OH��)>c(ClO��)
C���������Ũ�ȵ�����������Һ������ϣ�c(Na��)��c(CH3COO��)
D��Na2CO3��Һ�У�c(Na��)>c(CO32��)>c(OH��)>c(HCO3��)>c(H��)
7��Ϊ�˳�ȥMgCl2������Һ�е�Fe3�������ڼ��Ƚ���������¼���һ���Լ������˺��ټ���������HCl�������Լ��Ǹ�(����)
A��NH3·H2O���� B��NaOH C��Na2CO3 D��MgCO3
8�������������þƾ��Ƽ��������������ʵ���Һ��Ȼ�����գ����Եõ������ʹ������(�� ��)
A��AlCl3 B��Na2SO3 C��KMnO4 D��MgSO4
9�����ʵ���Ũ����ͬ��������Һ�У�NH4��Ũ��������(����)
A��NH4Cl B��NH4HSO4
C��CH3COONH4 D��NH4HCO3
10��ij������Һ��ֻ��Na����CH3COO����H����OH���������ӡ�������������ȷ����(�� ��)
A������Һ��pH��3��CH3COOH��pH��11��NaOH��Һ�������϶���
B������Һ�ɵ����ʵ���Ũ�ȡ��������NaOH��Һ��CH3COOH��Һ��϶���
C����������NaOH����Һ������Ũ��Ϊ��c(CH3COO��)��c(Na��)��c(OH��)��c(H��)
D������������ˮ��c(CH3COO��)һ������c(Na��)��c(NH4��)֮��
11�������£���A��B��C��D������ɫ��Һ�����Ƿֱ���CH3COONa��Һ��NH4Cl��Һ�������NaNO3��Һ�е�һ�֡���֪A��B��ˮ��Һ��ˮ�ĵ���̶���ͬ��A��C��Һ��pHֵ��ͬ��
�� B��________��Һ�� C��________��
�� ��������B��Һ��c(OH��)��C��Һ�е�c(H��)��ͬ��B��Һ��pH��pHb��ʾ��C��Һ��pH��pHc��ʾ����pHb��pHc��________(��ij����)��
����ҵ���á�
Ԥϰ��һ�ڽ�ѧ��
-
self-introduction ��ȫ
HottopicSelfintroductionVolunteerwanted��ļ��Ը��foranInternationalEng��
-
Self-introduction
UnitThreeSelfintroductionPartIHowtoWriteSelfintroduction1BriefInt��
-
Self Introduction����
SelfIntroductionHelloeveryoneImverygladtointroducemyselftoyouMynameisYangYi��
-
My Self-introduction
MySelfintroductionGoodmorningafternooneveryteacherandprofessorsThankyouvery��
-
self-introduction ���ҽ��ܷ���
FirstIwannasaythatallofusmusthavemadeorlistenedhundredsofthesocalledselfint��
-
��ѧѡ��4�����µ����ڡ������ˮ�⡷֪ʶ�ܽ�
��ѧѡ���ĵ����µ�3�ڡ������ˮ�⡷֪ʶ�ܽ�һ��̽������Һ�������ǿ�������ε�ˮ��Һ���ʼ��ԣ�ǿ�������ε�ˮ��Һ�������ԣ�ǿ��ǿ�
-
�����ˮ��֪ʶ���ܽ�
1�����ˮ��1��ϰ�ص�1�����ˮ��ԭ������Ӧ��2��Һ����������ϵ���غ�ԭ��2�ѵ�۽�һH2OH�ε�ˮ��ʵ��nnn����AB�ܵ硭
- ����ˮ��֪ʶ���ܽ�
-
�����ˮ��֪ʶ���ܽ�
1�����ˮ��1��ϰ�ص�1�����ˮ��ԭ������Ӧ��2��Һ����������ϵ���غ�ԭ��2�ѵ�۽�һH2OH�ε�ˮ��ʵ��nnn����AB�ܵ硭
-
�����ˮ��֪ʶ���ܽ�
�����ˮ��֪ʶ���ܽ�1��ϰ�ص�1�����ˮ��ԭ������Ӧ��2��Һ����������ϵ���غ�ԭ��2�ѵ�۽�һH2OH�ε�ˮ��ʵ��nnn���Ρ�