���ʵ���֪ʶ���ܽ�
���ʵ���֪ʶ�㸴ϰ
1�� Ħ��
���ʵ����ǹ��ʹ涨���߸�����������֮һ��������ʾ��һ����Ŀ���ӵļ��壬������n����λ��mol��
Ħ���Ǽ���ԭ�ӡ����ӡ������ӵ������ӵ����ʵ����ĵ�λ�� ����٤���������κ����ӵ���������������NA������6.02��1023
�������ֵ��
2�� Ħ������
1mol�κ����ӻ����ʵ������Կ�Ϊ��λʱ������ֵ�϶������ԭ����������Է���������ȡ�
Ħ��������ָ��λ���ʵ��������������е�������������M�����õ�λ��g��mol-1
3�� ʹ��Ħ���������ʱӦע�������
��1�� Ħ�������ʵ�����λ��ÿĦ�����ʺ��а���٤�����������ӣ�
Ħ�����Ħ������mol��
��2�� Ħ�������ȶ����ǹ������ʵĻ������ӣ�����ġ����ӡ���ָ
��������Ԫ�������������Ԫ�����Ƿ��ӡ�ԭ�ӡ����ӡ����ӡ����ӡ����ӵȵ�һ���ӣ�Ҳ��������Щ���ӵ��ض���ϡ���1molCaCl2����˵��1molCa2+��2molCl-��3mol���������ӣ���
��54mole-�ȡ�
��3�� Ħ������ֻ�����۲������ں�ۡ�
��4�� ʹ��Ħ����ʾ���ʵ���ʱ��Ӧ���û�ѧʽָ���������࣬����
��ʹ�ø����ӵ��������ơ�
4�� ����Ħ�����
��������Ŀ��ͬʱ�����������С��Ҫ������������Ӽ�ľ��롣Ҫ�Ƚ�һ�������������������������ͬ�¶Ⱥ�ѹǿ�½��С�
����Ħ���������λ���ʵ���������ռ�����������ΪVm,��λ��L/mol��m3/mol��
��״���������Ħ���������״���£����¶�Ϊ0�棬ѹǿΪ101Kpaʱ��1mol�κ�������ռ�������Լ��22.4L��
5����٤�����ɼ����ۣ�
��������״̬����PV��nRT��mRT���Եõ����¶��ɺ����ۣ� M
��1�� ͬ��ͬѹ�£���ͬ������κ����嶼������ͬ��Ŀ�ķ��ӡ�����
��٤�����ɣ�
��2��ͬ��ͬѹ�µIJ�ͬ���壬�����֮�ȵ������ʵ���֮�ȣ���������������Ŀ֮�ȡ�V1n1N1?? V2n2N2
(3) ͬ��ͬѹ�µIJ�ͬ���壬���ܶ�֮�ȵ�����Է�������֮�ȣ���������ܶȡ�M1?1����D12 (4)ͬ��ͬѹ��ͬ�����IJ�ͬ���壬M2?2
���ܶ�֮�ȵ������ʵ����ıȡ���n1
n2?1 ?2
��5��ͬ��ͬѹ��ͬ�����IJ�ͬ���壬�����֮�ȵ�����Է��������ķ��ȡ�V1M2�� V2M1
��6��ͬ��ͬ����IJ�ͬ���壬��ѹǿ֮�ȵ������ʵ���֮�ȣ���
�����ȣ���P1n1N1���� P2n2N2
��7��ͬ��ͬѹͬ����IJ�ͬ���壬������֮�ȵ�����Է�������֮�ȣ��ܶ�֮�ȣ�m1M1?1���� m2M2?2
�ص㽲��
һ�� ���ʵ������õļ��㹫ʽ��ע������
1��m��n��N֮��ļ��㹫ʽ
��1�������ϵ��n��mN��(2)���÷�Χ��ֻҪ������ɲ��䣬����MNA
�Ǻ���״̬����ʹ��
2��V��n��N֮��ļ����ϵ
��1�������ϵ��n��VNV���� NA22.4Vm
(2)���÷�Χ�����������������壬�����Ǵ������廹�ǻ������ �ڵ�����Ħ�������22.4L/molʱ�����DZ�״��
3���������ƽ�����������йؼ���
��1���������ݣ�
��1mol�κ����ʵ���������gΪ��λʱ������ֵ������ʽ����� ��1mol�κ������������LΪ��λ������ֵ��������Ħ��������
��2�� ���������ϵ��M��m n
m��
n�ܣ�M(A)?n(A)��M(B)?n(B)��?? �� M��n(A)��n(B)��??��3���任�����ϵ����M��
M(A)��n(A)����M(B)n(B)������ �� M ��M(A)��V(A)����M(B)��V(B)��������
��4��ʹ��˵�����٣�2���ļ���ʽ���������еĻ������� �ڣ�3��
�еļ���ʽֻ�����ڻ������ļ��� �ۣ�3���еļ���ʽ֮��Ӧ���˰���٤������
4���ܶ�������ܶ�
�ټ������ʽ��?��m ��ʹ��˵����A���������������ʣ�������V
��״̬���ƣ�Ҳ���������л���� ��B��������������M��Vm?����״��������M��22.4?
��2������ܶ�
�ټ������ʽ��D��?1/?2��M1/M2 ��ʹ��˵����A������ܶ���
ͬ��ͬѹ�����������ܶ�֮�ȣ�B���ȿ������ڴ�������֮��ļ��㣬Ҳ�����ڻ������֮��ļ��㡣
�ڶ�ƪ�����ʵ����ܽ�
��ѧ������ʵ���е�Ӧ�á������ʵ���
һ��֪ʶ���磺
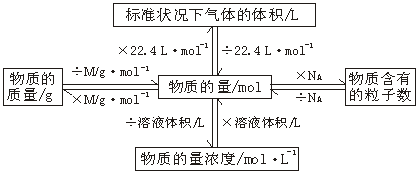
����������ʽ��
(1) ���ʵ������������Ĺ�ϵ��n=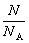
(2) ���ʵ����������Ĺ�ϵ�� n=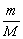 M=
M= m=M·n
m=M·n
(3) �������ʵ���������Ĺ�ϵ��n=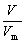 n=
n=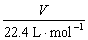 (��״��) Vm =
(��״��) Vm =  V=
V=
(4) ���ʵ���Ũ�ȣ�c=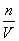 n=c·V
n=c·V
(5) ��Һ���ʵ���Ũ�������������Ĺ�ϵ�� c =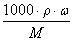 ���ܶȵĵ�λ��g/cm3 �� n=
���ܶȵĵ�λ��g/cm3 �� n=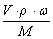
(6) ��Һϡ�ͣ� c1V1=c2V2
�������ʵ��������֪ʶ���
1�����ʵ������DZ�ʾ�������Ӽ����һ��������������Ϊn����λ��Ħ����mol����
2��Ħ���������ʵ����ĵ�λ��
�����Ϲ涨�� 1Ħ�����Ӽ�����������������0.012 kg C��������̼ԭ������ͬ��ԼΪ6.02×1023
3�������ӵ�������1Ħ�����κ����ӵ�����������1Ħ����������ȷֵ���÷���NA��ʾ��NA�Ľ���ֵΪ6.02×1023mol-1��
���㹫ʽ��n=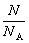
4��ʹ��Ħ�������λʱҪע�⣺��ʹ�÷�Χ��ֻ�������ۣ�ԭ�ӡ����ӵȣ����������ں��
��ʹ��ʱӦ���û�ѧʽָ�����ӵ����࣬����ʹ�ø����ӵ��������ơ�
5�����ʵ��������������Ĺ�ϵ��
1�κ����ӻ����ʵ������Կ�Ϊ��λ������ֵ��������ӵ����ԭ����������Է���������ȡ�
6��Ħ����������λ���ʵ��������������е���������~ ���÷���M��ʾ����λ��g.mol-1��
���㹫ʽ��M=
ע�⣺Ħ����������Է������������ԭ�������Ĺ�ϵ��Ħ��������g?mol-1Ϊ��λ����ֵ������Է������������ԭ��������ȣ����ԭ����������Է���������λ��
7������Ħ���������λ���ʵ��������������е��������~ ���÷���Vm��ʾ����λ��L.mol-1��
���㹫ʽ��Vm =  �˸���Ҫ�߱���Ҫ�㣺�ٱ��������壨�����ǻ�����壩��Ҫ�������״��
�˸���Ҫ�߱���Ҫ�㣺�ٱ��������壨�����ǻ�����壩��Ҫ�������״��
���磺�����壨�����ǻ�����壩���ڱ�״���� �����ʵ���Ϊ1mol �������ԼΪ22.4L��
��������嵫���ڱ�״���£����ʵ�����ʹ��1mol�����Ҳ������22.4L��
8�������ӵ����ɣ�ͬ��ͬѹ�£���ͬ������κ����庬����ͬ��Ŀ�ķ��ӡ���T��p�㶨ʱ��V1/V2=n1/n2=N1/N2��
9�������ӵ��������ۣ� PV=nRT
��1��T��p�㶨ʱ��V1/V2=n1/n2=N1/N2 ��2��T��p�㶨ʱ����1/��2=M1/M2
��3��T��p��V�㶨ʱ��m1/m2=M1/M2 ��4��T��p��m�㶨ʱ��V1/V2=M2/M1
��5��T��V�㶨ʱ��p1/p2=n1/n2=N1/N2 ��6��T��V��m�㶨ʱ��p1/p2=M2/M1
10��������������������أ�
��1���������ӣ�����Ŀ����2���������ӣ������Ĵ�С����3��������֮��ľ��롣
A�����ڹ����Һ�壬�������ǵķ����ǽ��ܶѻ��ģ��������Ƿ���֮��ľ�����Ϊ�㡣
���������Һ����������أ�������Ŀ���������Ĵ�С
B���������壬����֮��ľ����Զ�����ӵ�ֱ���������Ĵ�С�������֮��ľ���������Ǻ�С��С�ģ����Է��ӵ�ֱ���������Ĵ�С������Ϊ�㡣
����������������أ�������Ŀ����֮��ľ���
11�����ʵ���Ũ�ȣ���ʾ��λ�����Һ����������B�����ʵ���������cB ����λ�� mol?L-1
12����Һ��ϡ�ͣ���Һϡ�͵���ԭ�����ʵ�������
����������������Һ�����ʵ��������䣬m1W1==m2W2
�������ʵ�����Һ�����ʵ����ʵ������䣬c1V1==c2V2
13�����ʵ���Ũ��c����������W֮��Ĺ�ϵ��c ==1000��W/M ���ܶȵĵ�λ��g/cm3 ��
14��һ�����ʵ���Ũ����Һ�����ƣ�����ƿ
��1�����裺���㡢��������ȡ�����ܽ⡢��ȴ����Һ��ϴ�ӡ����ݡ�ҡ�ȡ�װ���Լ�ƿ���á�
��2����������A�����ӡ����� B��δ��ȴ
��ϰ��ѵ��
1�����й������ʵ������������������( )
A.�� mol�κ����ʶ�����6.02×����23������ B.0.012 kg 12���к���Լ6��02×����23��C
C.1 molˮ�к���2 mol��ԭ�Ӻͣ� mol��ԭ�� D.1 mol ��e�к���6.02×����24������
2���������ʵ�����ͬ����������ᣬ����˵������ȷ����( )
A.���Ӹ������ B.���е���ԭ������� C.���е���ԭ������� D.�������
3����ѧ�Ҹոշ�����ij��Ԫ�ص�ԭ�ӣ���������a g��12C��ԭ��������b g��NA�ǰ����ӵ�������ֵ������
˵������ȷ���ǣ� ��
A����ԭ�ӵ�Ħ��������aNA B��Wg��ԭ�ӵ����ʵ���һ���� 
C��Wg��ԭ���к���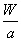 ����ԭ�� D������֪��Ϣ�ɵã�
����ԭ�� D������֪��Ϣ�ɵã�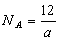
4����ijԭ�ӵ�Ħ�������� g·mol��1����һ����ԭ�ӵ���ʵ�����ǣ��� ����
g·mol��1����һ����ԭ�ӵ���ʵ�����ǣ��� ����
����A�� g������B��
g������B��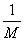 g C��
g C��
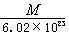 g������D��
g������D��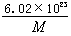 g
g
5����50��ˮ������ mL����1��ˮ�����ķ������ǣ�������
mL����1��ˮ�����ķ������ǣ�������
������A�� ×50×18×6.02×1023������B��
×50×18×6.02×1023������B��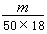 ×6.02×1023
×6.02×1023
������C��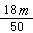 ×6.02×1023������������D��
×6.02×1023������������D��
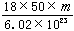
6��n g O2����m��Oԭ�ӣ����ӵ�����NA����ֵ�ɱ�ʾΪ( )
A��32m/n B��16m/n C��n/32m D��n/16m
7����֪1.505×1023��X������ӵ�����Ϊ8g����X�����Ħ��������( )
A��16g B��32g C��64g /mol D��32g /mol
8�����״����V��L��CO2������ԭ����Ŀ��ͬ��ˮ�������ǣ� ��
A��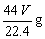 B��
B��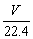 g�� C.
g�� C.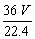 g D��
g D��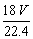 g
g
9��NAΪ�����ӵ�����������������ȷ���ǣ� ��
A..40 g NH4NO3�к��е�ԭ��NA�� B.��״���£�22.4 L H2��N2�Ļ�������У�H2��N2������֮��Ϊ2NA
C.��״���£�22.4 L CCl4����������ΪNA D.��Fe��Cl2��Ӧ�У�1 mol Fe��1 mol Cl2ǡ�÷�Ӧ
10����֪m g����A��n g����B������������ȣ�����˵������ȷ���ǣ� ��
A.��״��ʱ����ͬ���������A������B������֮��Ϊm��n
B.25 ��ʱ����ͬ����������A������B�ķ�����֮��Ϊn��m
C.ͬ�¡�ͬѹ�£�����A������B���ܶ�֮��Ϊn��m
D.ͨ��״���£���ͬ����������A������B�����֮��Ϊn��m
11����һ���ܱ�������ʢ��11 g X����(X��Ħ������Ϊ44 g·mol��1)ʱ��ѹǿΪ1×104 Pa���������ͬ�¶��£��Ѹ��������X����������ʹ������ѹǿ����5×104 Pa����ʱ����������X�ķ�����ԼΪ( )
A.3.3×1025 B.3.3×1024 C.7.5×1023 D.7.5×1022
12������ͬ״���£�����ΪWg�IJ���ƿ������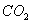 �����������Ϊ124.4g����Ϊ��������ʱ������Ϊ123.2g����
�����������Ϊ124.4g����Ϊ��������ʱ������Ϊ123.2g����
Ϊ��������X��������Ϊ122.8g�������Ŀ���Ϊ�� �� A��CO B��NO C��SO2 D��CH4
13��ͬ��ͬѹ�µ����������ͬ�Ĵ���ƿ��һ��װ��C2H4����һ��װ��C2H2��C2H6�Ļ�����壬��ƿ�е�����һ��������ͬ��( )
A.���� B.ԭ������ C.̼ԭ���� D.�ܶ�
14���ڱ�״���¢�6.72L CH4 ��3.01×1023��HCl���� ��13.6g H2S ��0.2mol NH3, ���ж�����������Ĺ�ϵ�Ӵ�С������ȷ���ǣ� ��
a������ڣ��ۣ��٣��� b���ܶȢڣ��ۣ��ܣ���
c�������ڣ��ۣ��٣��� d����ԭ�Ӹ����٣��ۣ��ܣ���
A��abc B��bcd C��cba D��abcd
15����4 g NaOH�ܽ���10 mLˮ�У���ϡ�ͳ�1 L������ȡ��10 mL����10 mL��Һ�����ʵ���Ũ��Ϊ( )
A.1 mol·L��1 B.0.1 mol·L��1 C.0.01 mol·L��1 D.10 mol·L��1
16��ȡ100 mL 0.3 mol·L��1��300 mL 0.25 mol·L��1������ע��500 mL������ƿ�У���ˮϡ�����̶��ߣ��û����Һ��H+�����ʵ���Ũ����( ) A.0.21 mol·L��1 B.0.56 mol·L��1 C.0.42 mol·L��1 D.0.26 mol·L��1
17����ͬ�����Na2SO4��MgSO4��Al2(SO4)3��Һ�ֱ���������BaCl2��Һ���õ����������ʵ���֮��Ϊ1��1��3����������Һ�����ʵ���Ũ��֮��Ϊ( )
A.2��2��3 B.1��1��3 C.1��1��1 D.3��3��1
18�����ܶ�Ϊd g·cm��3����������μ�����������Һ�����������ɳ�����������ԭ�����������ȣ�ԭ��������ʵ���Ũ��Ϊ( ) A.25.4d mol·L��1 B.12.7d mol·L��1 C.6.97d mol·L��1 D.6.35d mol·L��1
19������״���µ�a L��������1000 gˮ�У��õ���ˮ���ܶ�Ϊb g·cm��3����ð�ˮ�����ʵ���Ũ��Ϊ( )
A.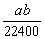 mol·L��1 B.
mol·L��1 B.  mol·L��1 C.
mol·L��1 C.  mol·L��1 D.
mol·L��1 D. 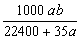 mol·L��1
mol·L��1
20������������Ϊ2 w�����ʵ���Ũ��Ϊc1��H2SO4��Һ��ˮϡ�ͣ�ʹ����������Ϊw�����ʵ���Ũ�ȱ�Ϊc2����c1��c2֮���ϵ��ȷ����
A.c1>2c2 B.c2=2c1 C.c1<2c2 D.c1=2c2
21����NAΪ�����ӵ����������й���0.2 mol ·L��1 Ba��NO3��2��Һ��˵������ȷ���ǣ�����ˮ�ĵ��룩�� ��
A.1 L��Һ�к�����������������0.6 NA B.500 mL��Һ��Ba2+��Ũ����0.2 mol·L��1
C.500 mL��Һ��NO��3��Ũ����0.4 mol·L��1 D.1 L��Һ�к���0.2 NA��NO��3
22����a gп�ӵ�V L c mol·L��1�������У����ų�n L��������״���£�����ԭ��HCl�����ʵ����ǣ� ��
A. mol B.
mol B.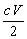 ×10��3 mol C.
×10��3 mol C.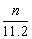 mol D. cV mol
mol D. cV mol
23������100 mL 1 mol·L��1����������Һ�����в���������ǣ� ��
A.��������ƽ�Ϸ���Ƭ��С������һ����ֽ��Ȼ���������Ʒ���ֽƬ�Ͻ��г���
B.�ѳƵõ��������Ʒ���ʢ����������ˮ���ձ��У��ܽ⡢��ȴ���ٰ���Һ��������ƿ��
C.������ˮϴ���ձ���������2~3�Σ�ϴ��ҺҲ��������ƿ��
D.���Ų�����������ƿ�м�������ˮ������̶���2~3 cmʱ���ý�ͷ�ιܵμӣ�ֱ����Һ����ǡ����̶�����
24��������һ�����ʵ���Ũ�ȵ�������Һʱ�����д��������ʹ��������ҺŨ��ƫ�ߵ���( )
A.����Ͳ��ȡŨ����ʱ���Ӷ��� B.�ܽ����ʱ��Һ��ɽ�
C.����ʱ��������ƿƿ���̶��� D.ҡ�Ⱥ��Һ���½����ټ�ˮ���̶���
25������500 mL 1 mol·L��1��NaCl��Һʱ�����в�����ʹʵ����ƫ�ߵ���______________��ƫ�͵���______________����Ӱ�����______________��
A.��ҡ����Һ����Һ����ڿ̶��ߣ��ٲ���ˮ
B.����ʱ������������̣�����������̣�δ�����룩
C.ԭ����ƿϴ�Ӻ�δ����
D.��Һʱ��δϴ���ձ��Ͳ�����
E.����ʱ�����ӿ̶���
-
���ʵ���֪ʶ���ܽ�
���ʵ���֪ʶ�㸴ϰ1Ħ�����ʵ����ǹ��ʹ涨���߸�����������֮һ������ʾ��һ����Ŀ���ӵļ��������n��λ��molĦ���Ǽ���ԭ�ӷ��ӻ�
- ���ʵ�����Ԫ֪ʶ�㸴ϰС��
- ��һ��ѧ���ʵ���֪ʶ�����2
- ���ʵ���֪ʶ��С��
- ���ʵ���֪ʶ������
- ���ʵ������֪ʶ���ܽ�
-
�����ˮ��֪ʶ���ܽ�
����ˮ���Ӧ�ÿ���1�жϻ��������Һ���������������KXKYKZ����Һ���ʵ���Ũ����ͬ��pHֵ�ֱ�Ϊ789��HXHYHZ������ǿ����
- ���ʵ�����Ԫ֪ʶ�㸴ϰС��
- ��һ��ѧ���ʵ���֪ʶ�����2
- ���ʵ���֪ʶ��С��
-
���������ලԱ�����ܽ�
���蹤�������ලԱ���չ����ܽ�20xx�걾����ס���ֺͽ��蹤����������վ����ȷ�쵼�£����㱾ְ����������������쵼�����ĸ�������