实验三:乙酰苯胺的重结晶及熔点的测定
实验二:乙酰苯胺的重结晶及熔点的测定
一、实验目的
1、学习重结晶的基本原理、用途。
2、掌握重结晶提纯固体有机物的操作步骤。
3、学习热过滤和减压过滤的操作技术。
4、了解熔点测定的方法和意义。
二、实验原理
重结晶法是提纯固体有机物的常用方法。固体有机物在溶剂中的溶解度一般随温度的升高而增大,反之溶解度降低。。把固体有机物溶解在热的溶剂中制成饱和溶液,然后冷却至室温以下,则原溶液变成过饱和溶液,这时有机物又重新析出晶体。利用溶剂对被提纯物质及杂质的溶解度不同,使被提纯物质从过饱和溶液中析出。让杂质全部或大部分留在溶液中,从而达到提纯的目的。
三、主要试剂及产品的物理常数:(文献值)

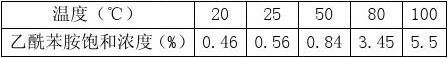
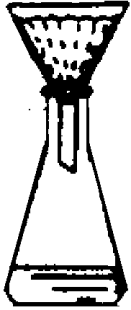
乙酸苯胺在水中的溶解度与温度的关系
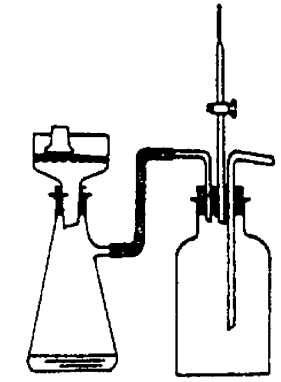
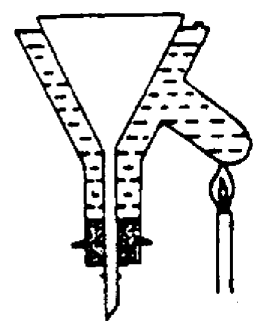
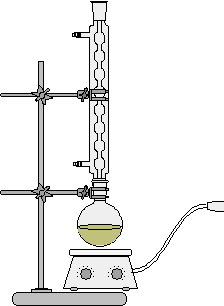
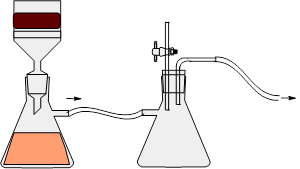
四、实验装置图
(1) (2) (3)
热滤及减压过滤装置
1
五、实验流程
粗乙酰苯胺 + 水
时间 实验记录
加热

滤液
滤渣
乙酰苯胺
+可溶性杂质 活性碳+不溶性杂质
可溶性杂质
产品回收
六、数据处理
实际产量= 回收率= 熔程=
七、思考题
1.理想溶剂应具备的条件是什么? 2.活性炭使用时应注意什么? 3.抽气过滤时应注意什么?
2
乙酰苯胺=? 水=?
观察乙酰苯胺是否完全溶解? 活性碳=? 煮沸多少时间?
观察热过滤后溶液的状态? 冷却结晶方式?
晶体的状态? 产品重=总重-纸重? 初熔温度=?
终熔温度=?
乙酰苯胺
第二篇:实验3 乙酰苯胺的重结晶
实验三、乙酰苯胺的重结晶 (6学时)
一、实验目的
掌握重结晶的基本原理和基本操作
二、基本原理
固体有机物在溶剂中的溶解度与温度密切相关。一般温度升高,溶解度增大。
将不纯固体有机物溶于热的适当溶剂使成近饱和溶液,以活性炭脱除有色杂质。热过滤后冷却,利用固体有机物在高、低温溶剂中溶解度的差异,使固体有机物呈结晶析出,从而与杂质分离开来。
三、仪器与试剂
仪器:
台称天平;电热套(或集热式磁力搅拌器);电吹风;铁架台及铁夹;量筒;100ml单口烧瓶;球形冷凝管;橡胶管;短颈漏斗;100ml三角瓶;布氏漏斗;玻璃棒;表面皿;水循环泵;抽滤瓶;干燥箱;滤纸;称量纸等
试剂:
粗乙酰苯胺;活性炭;水;沸石等
四、实验步骤
1、粗乙酰苯胺溶解、脱色
将150ml单口烧瓶以合适的高度固定于铁架台上,向瓶内加入2g乙酰苯胺、70ml水及2粒沸石。安装球形冷凝管并接通冷凝水,电热套加热至微沸。视溶解情况而定是否从冷凝管上口补加水。
若溶液有色,撤去加热装置,待溶液冷却后向烧瓶中加入少许活性炭,并再加入2粒沸石,重新加热,沸腾5~10分钟。
2、热过滤 (关键步骤)
将折叠滤纸放入预热短颈漏斗,并用预热的水润湿滤纸,迅速倒入热的粗乙酰苯胺溶液,用预热的水润洗烧瓶并转移至漏斗内过滤(必要时用电吹风加热漏斗)。最后用少量预热水洗涤滤纸。
滤毕,先将滤液于室温下静置结晶,然后冰水冷却。
3、抽滤及干燥
将裁剪合适的滤纸放入布氏漏斗内,并用冷水润湿。减压以使滤纸贴紧布什漏斗底壁,然后倒入乙酰苯胺晶体滤液,抽滤时要尽可能将溶剂除去,并用母液洗涤有残留产品的烧杯,并用冷的少量水洗涤乙酰苯胺结晶2-3次。
抽干后将乙酰苯胺晶体转移到表面皿上, [产物抽干后称重,计算回收率]
4、上交产品
注意事项:
1、粗乙酰苯胺溶解时补加水至烧瓶内固体物不再减少或全溶。
2、待溶液冷却后才加入活性炭,并重新加入2粒沸石方可重新加热。
3、滤纸折成扇形以利于过滤。
4、短颈漏斗需提前预热,热过滤动作要快。
-
实验6_乙酰苯胺熔点的测量
实验六乙酰苯胺等物质熔点的测量一实验目的1掌握毛细管法测定乙酰苯胺等物质的熔点2掌握用测量熔点的方法鉴定物质的种类和检验物质的纯度…
- 熔点的测定实验报告
-
实验三:乙酰苯胺的重结晶及熔点的测定
实验二乙酰苯胺的重结晶及熔点的测定一实验目的1学习重结晶的基本原理用途2掌握重结晶提纯固体有机物的操作步骤3学习热过滤和减压过滤的…
-
1乙酰苯胺的重结晶及熔点的测定
乙酰苯胺的重结晶及熔点的测定实验目的1熟悉重结晶的基本操作2了解乙酰苯胺的结晶制备3了解熔点测定的原理4掌握毛细管法测定熔点的操作…
-
实验论文 乙酰苯胺的重结晶及熔点的测定
乙酰苯胺的重结晶及熔点的测定学号1505100103班级应化1005姓名苑蕊蕊摘要根据乙酰苯胺在各种溶剂中的溶解度与温度的关系采用…
- 熔点的测定实验报告
-
实验6_乙酰苯胺熔点的测量
实验六乙酰苯胺等物质熔点的测量一实验目的1掌握毛细管法测定乙酰苯胺等物质的熔点2掌握用测量熔点的方法鉴定物质的种类和检验物质的纯度…
-
乙酰苯胺的制备实验报告南昌大学
南昌大学有机化学实验报告学生姓名彭以振学号专业班级实验类型验证综合设计创新实验日期20xx年9月28日实验地点同组学生姓名指导教师…
-
实验论文 乙酰苯胺的重结晶及熔点的测定
乙酰苯胺的重结晶及熔点的测定学号1505100103班级应化1005姓名苑蕊蕊摘要根据乙酰苯胺在各种溶剂中的溶解度与温度的关系采用…
-
1乙酰苯胺的重结晶及熔点的测定
乙酰苯胺的重结晶及熔点的测定实验目的1熟悉重结晶的基本操作2了解乙酰苯胺的结晶制备3了解熔点测定的原理4掌握毛细管法测定熔点的操作…
-
乙酰苯胺的制备(实验报告实验总结范文模板)
(实验报告)乙酰苯胺的制备【目的要求】⑴熟悉氨基酰化反应的原理及意义,掌握乙酰苯胺的制备方法;⑵进一步掌握分馏装置的安装与操作;⑶…