大学有机化学实验报告:肉桂酸的制备
有 机 化 学 实 验 报 告

实 验 名 称: 肉桂酸的制备
学 院: 化学工程学院
专 业: 化学工程与工艺
班 级:
姓 名: 学 号
指 导 教 师:
日 期: 20##年12月22日
一、实验目的
1. 了解肉桂酸的制备原理和方法;
2. 掌握水蒸气蒸馏的原理、用处和操作;
3. 学习并掌握固体有机化合物的提纯方法:脱色、重结晶。
二、实验原理
1. 用苯甲醛和乙酸酐作原料,发生Perkin反应,反应式为:
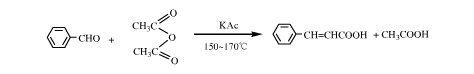
2. 反应机理如下:乙酸肝在弱碱作用下打掉一个H,形成CH3COOCOCH2-,然后
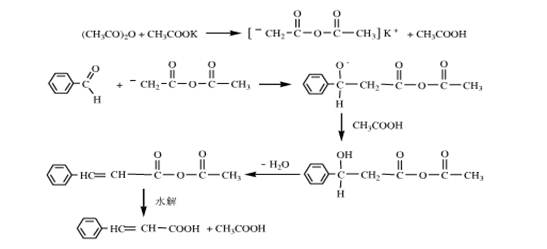
三、主要试剂及物理性质
1. 主要药品:无水碳酸钾、苯甲醛、乙酸酐、氢氧化钠水溶液、1:1盐酸、活性炭
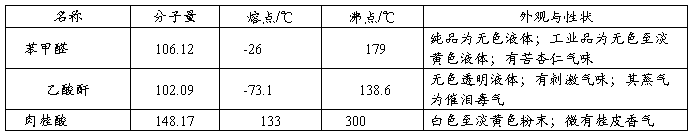
2. 物理性质
主要试剂的物理性质
四、试剂用量规格
试剂用量

五、仪器装置
1. 仪器:150ml三口烧瓶、500ml烧杯、玻璃棒、量筒、200℃温度计、直形冷凝管、电磁炉、球形冷凝管、表面皿、滤纸、布氏漏斗、吸滤瓶、锥形瓶
2. 装置:

图1.制备肉桂酸的反应装置 图2.水蒸气蒸馏装置
六、实验步骤及现象
实验步骤及现象

七、实验结果
实验数据记录
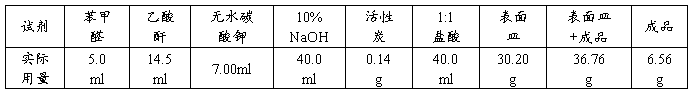
理论产量:0.05*148.17=7.41g
实际产量:6.56g
产率:6.56/7.41*100%=88.53%
八、实验讨论
1. 产率较高的原因:
1) 抽滤后没有干燥,成品中还含有一些水分,使产率偏高;
2) 加活性炭脱色时间太短,加入活性炭量太少。
2. 注意事项
1) 加热时最好用油浴,控制温度在160-180℃,若用电炉加热,必须使烧瓶底离电炉远一点,电炉开小一点;若果温度太高,反应会很激烈,结果形成大量树脂状物质,减少肉桂酸的生成。
2) 加热回流,控制反应呈微沸状态,如果反应液激烈沸腾易对乙酸酐蒸气冷凝产生影响,影响产率。
第二篇:苯基肉桂酸合成实验报告
实验名称 Z ,E -α-苯基肉桂酸的合成与分离
实验者 ____________ 实验日期 9月6日 9月20日
Z ,E -α-苯基肉桂酸的合成与分离
摘要 以乙酸酐、苯甲醛、苯甲酸为原料,三乙胺作为碱催化,通过Perkin反应制备Z、E-α-苯基肉桂酸,并利用Z、E-α-苯基肉桂酸的酸性差异进分离。重结晶后所得的Z、E-α-苯基肉桂酸利用TLC检测,结果表明分离效果较好。
关键词 Perkin反应 α-苯基肉桂酸 Z、E异构的分离
引言Perkin反应,又称普尔金反应,由William Henry Perkin 发展的,由不含有α-H的芳香醛(如苯甲醛)在对应的羧酸盐或三级胺的催化下,与含有α-H的酸酐所发生的缩合反应,并生成α,β-不饱和羧酸盐,后者经酸性水解即可得到α,β-不饱和羧酸。本次反应利用Perkin反应制备Z ,E -α-苯基肉桂酸,并利用Z、E-α-苯基肉桂酸的酸性差异进分离。
机理
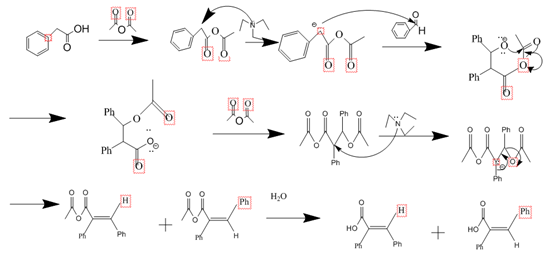
(本报告所有机理及分子构象图均亲手用chemdraw 及chem3d绘制,初次使用做得不好多多包涵)
 实验部分
实验部分
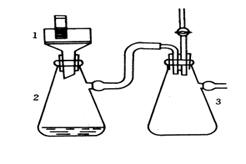
 实验装置图
实验装置图
实验试剂
苯乙酸2.50g(18.4mmol) 苯甲醛3.0ml(29.6mmol) 三乙胺2.0ml(14.4mmol)
乙酸酐2.0ml(21.2mmol) 石油醚 乙醇
实验步骤
100ml烧瓶加入苯乙酸2.50g(18.4mmol),苯甲醛3.0ml(29.6mmol),三乙胺2.0ml(14.4mmol),乙酸酐2.0ml(21.2mmol),加入搅拌磁子。加热回流30min,冷却至室温,液体为黄色。在搅拌下缓缓加入4.0ml浓盐酸。得到白色粉状固体。加30.0ml乙醚,水浴至全溶,转至分液漏斗,分出水相。有机相用15ml水洗两次。将乙醚倒入100ml烧瓶,加25ml 5%NaOH及10ml水,温热,澄清后冷却至20-25摄氏度。分液,乙醚用5ml 5%NaOH萃取一次,合并萃取液。
萃取液加2.5ml乙酸有白色固体E -α-苯基肉桂酸生成,继续加乙酸至无沉淀生成,过滤后测母液pH,pH为6-7表明E -α-苯基肉桂酸已完全析出。保留母液。
用乙醇-石油醚重结晶。用2.5-3ml少量无水乙醇溶解,加热后,加石油醚至刚好出现浑浊,加热变澄清。减压热过滤,静置析晶。
母液加浓盐酸至pH 1-2,至无沉淀析出,放置0.5h以上,过滤干燥,用3-5 95%乙醇重结晶,常压过滤,加去离子水至浑浊,回滴乙醇至澄清,放置析晶。
纯化流程图
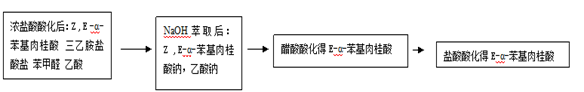
实验结果
E-α-苯基肉桂酸粗品3.34g,重结晶后1.68g(重结晶冷却时烧瓶倒掉冰浴的水进入烧瓶,纯度受影响,产品微黄)产率40%
Z-α-苯基肉桂酸粗品0.26g,由于课时有限没有做Z-α-苯基肉桂酸重结晶。
TLC板检验如下,表明纯化效果较好。
结果与讨论
本实验表明通过Perkin反应制备Z、E-α-苯基肉桂酸产率较好,纯化方法能较有效地分离Z、E-α-苯基肉桂酸异构体。该方法适用于制备芳基取代α,β-不饱和羧酸。一下将对实验中一些细节加以讨论
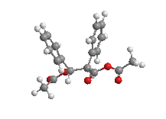
 1.本实验为何主要得到E-α-苯基肉桂酸?
1.本实验为何主要得到E-α-苯基肉桂酸?
答:中间体 的构象如下
(由chem3D MMFF94算法计算所得)
由于构象上的优势得到动力学产物
E-α-苯基肉桂酸。
2.本实验为何在不同酸度下可以分离Z、E-α-苯基肉桂酸异构体?在pH6-7得到E型,pH 1-2得到Z型。顺反异构为何酸性相差如此大?
答:这是因为E-α-苯基肉桂酸两个苯基的距离小于其范德华半径,两个苯环偏离共轭平面,不能很有效共轭分散羧基负电荷,其酸性较弱。
Z-α-苯基肉桂酸两个苯环能很好地与双键共轭,羧基负电荷能有效分散,其酸性很强,需要在pH 1-2的条件下才能以酸的形式析出。构象分析如下
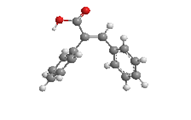 E-α-苯基肉桂酸
E-α-苯基肉桂酸
(不能有效共轭)
Z-α-苯基肉桂酸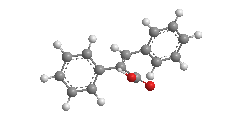
(较好共轭)
3教训:本人见同学在做E-α-苯基肉桂酸重结晶热过滤时晶体析出严重,加了过多的乙醇,企图通过加更多的石油醚逼出晶体。结果发现忽略了结晶对于浓度的要求。只得通过蒸掉溶剂来获得晶体。明白了加过量良溶剂再加更多的不良溶剂来结晶是不可行的。
致谢
基础有机实验张奇涵老师及李刚助教及全体实验室同学
参考文献
基础有机实验(北京大学出版社、关烨第、李翠娟等)
-
实验二 香豆素-3-羧酸的制备预习报告
香豆素3羧酸的制备1实验目的1掌握Perkin反应原理和芳香族羟基内酯的制备方法Perkin反应是指由不含有H的芳香醛如苯甲醛在强…
-
肉桂酸的制备实验报告(4)沈杰
实验学专班姓指导日机化学实验报告名称院化学工程学院业化学工程与工艺级化工114班名沈杰学号114020xx417教师肖勋文何炎军期…
-
大学有机化学实验报告:肉桂酸的制备
大学有机化学实验报告肉桂酸的制备一实验目的1了解肉桂酸的制备原理和方法2掌握水蒸气蒸馏的原理用处和操作3学习并掌握固体有机化合物的…
-
实验八肉桂酸的制备
实验八肉桂酸的制备一实验目的1学习肉桂酸的制备原理和方法2学习水蒸气蒸馏的原理及其应用掌握水蒸气蒸馏的装置及操作方法二基本原理1P…
-
北京大学有机化学实验要点总结
据当年出题助教给的要点进行的总结见文末图片可能由没写全或者自己比较熟悉就没总结的地方每年考核重点也在变化仅供参考一般考试涉及知识点…
-
肉桂油的提取实验报告
广州大学化学化工学院本科学生综合性设计性实验报告实验课程化学工程与工艺专业实验实验项目肉桂油的提取专业化学工程与工艺班级12化工2…