三组分体系相图的制备实验报告

三组分体系相图的制备
一:实验目的
制备等温、等压下苯-水-乙醇三组分体系相图。
二、实验原理
三组分体系的组成可用等边三角坐标表示。等边三角形三个顶点分别代表纯组分A、B和C。则AB线上各点相当于A和B组分的混合体系,BC线上各点相当于B和C组分的混合体系,AC线上各点相当于A和C组分的混合体系。
在苯-水-乙醇三组分体系中,苯与水是部分互溶的,而乙醇和苯、乙醇和水都是完全互溶的。设由一定量的苯和水组成一个体系,其组成为K,此体系分为两项:一相为水相,一项为苯相。当在体系中加入乙醇时,体系的总组成沿AK线移至N点。此时乙醇溶于水相及苯相,同时乙醇促进苯与水互溶,故此体系由两个分别含有三个组分的液相组成,但这两个液相的组成不同。若分别用b1、c1表示这两个平衡的液相的组成,此两点的连线称为连系线,这两个溶液称为共轭溶液。代表液-液平衡体系中所有共轭液相组成点的连线称为溶解度曲线(如图1-1)。曲线以下区域为两相共存区,其余部分为均相区。此图称为含一对部分互溶组分的三组分体系液-液平衡相图。

图1-1 三组分体系液-液平衡相图
按照相律,三组分相图要画在平面上,必须规定两个独立变量。本实验中,它们分别是温度(为室温)和压力(为大气压)。
三、实验仪器与药品
1、仪器
25ml酸式滴定管2支、5ml移液管1支、50ml带盖锥形瓶8个。
2、药品
苯(分析纯)、无水乙醇(分析纯)、蒸馏水。
四、实验步骤
1、取8个干燥的5毫升带盖锥形瓶,按照记录表格中的规定提及用滴定管即移液管配制六种不同浓度的苯乙醇溶液,即两种不同浓度的水乙醇溶液。
2、用滴定管向已配好的水-乙醇溶液中滴苯,至清液变浑浊,记录此时每种清液中水的体积。滴定时必须充分摇荡,同时注意动作迅速,尽量避免由于苯、乙醇的挥发而引起的误差。
3、读取室温。
4、记录表格。
五、实验数据
表1-2 溶解度曲线有关数据记录表
室温:22℃
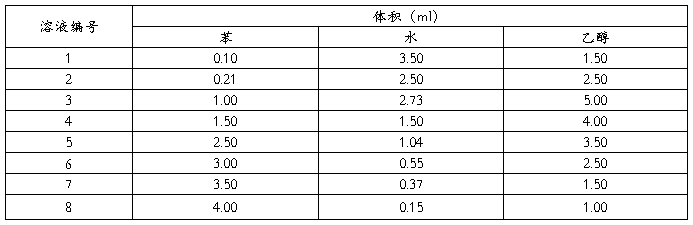
六、数据处理
将各溶液滴定终点时各组分的体积,根据它们在实验温度下的密度(查附录二和 附录三)换算为质量,求出各溶液滴定终点时的质量分数或质量分数的浓度。求出各溶液滴定终点时的质量分数或质量分数的浓度。将所得的点及笨与水的相互溶解的点(见附录一)绘于三角坐标纸上,并将各点连成平滑曲线。
实验数据的处理方法如下:
已知苯、水、乙醇的体积,参照附录二、附录三以及其中的公式,可求出各自的密度,再换算为质量。
公式为:d =A +B+Ct2+Dt3
式中:d -密度(g/cm3);
t -温度(℃),。实验中t=22℃
可得水的密度d(水)=0.9983g/cm3,
d(苯)=0.876509g/cm3
d(乙醇)=0.79032g/cm3
表1-3 溶解度曲线数据处理表
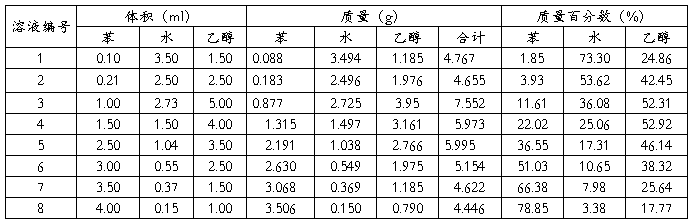
例如
对第一组数据进行处理
m(苯)=0.876509g/cm3×0.10ml=0.088g
m(水)=0.9983g/cm3×3.50ml=3.494g
m(乙醇)=0.79032g/cm3×1.50ml=1.185 g
m= m(苯)+m(水)+m(乙醇)=4.767g
w(苯)=0.088g/4.767g×100%=1.85%
w(水)=3.494g/4.767g×100%=73.30%
w(乙醇)=1.185g/4.767g×100%=24.86%
七、注意事项
1、用蒸馏水瓶将蒸馏水倒入酸式滴定管,并记录初始刻度值;
2、用烧杯量取30mL苯倒入酸式滴定管中,待用;
3、实验完毕,酸式滴定管中的苯回收至原瓶中;
4、锥形瓶中的废液倒入废液桶中,把锥形瓶冲洗干净,放入烘干箱烘干,再换上8个烘干瓶摆好。
八 思考题
1.本实验所用的滴定管(盛苯的)、锥形瓶、移液管等为什么必须干燥?
答::由于本实验对数据要求比较精确,微小的误差就会对实验产生较大的误影响,会影响三组分体系相图的绘制。因此,实验前将滴定管(盛苯的)、锥形瓶、移液管等干燥是为了减小实验误差,提高实验的准确度。如果上述仪器不干燥,会使苯,水和乙醇质量有所误差,影响三相体系图的绘制和实验结果精度。
2.当体系组成分别在溶解度曲线上方及下方时,这两个体系的相数有什么不同? 在本实验中是如何判断体系总组成正处于溶解度曲线上的?此时为几相?
答:在溶解度曲线上方时,体系为均相,相数为1,在溶解度曲线下方时,体系的相数为2;溶液刚出现浑浊时体系总组成正处于溶解度曲线上,此时为单相。
3.温度升高,体系的溶解度曲线会发生什么样的变化?在本实验操作中 应注意哪些问题,以防止温度变化而影响实验的准确性?
答:当温度升高时,溶解度增大,三组分体系溶解度曲线会下降,曲线包围面积变小。实验时应尽量避免用手接触溶液附近的容器壁,避免用手捂住容器,防止因温度升高而影响实验结果;还有滴定时动作要迅速, 减少震荡时因乙醇等挥发的影响。
九、实验小结
通过这次“三组分体系相图的制备”的实验,我学会了如何制备在等温等压下苯—水—乙醇三组分体系相图的方法,掌握了移液管量取液体的操作和酸式滴定管的使用方法。在实验过程中,需要细心和耐心,再往水和乙醇混合溶液中滴加苯时,要不断摇晃小锥形瓶。千万不要因粗心失误引入人为误差。动手操作能力是慢慢锻炼出来的,希望在以后的实验中也会不断总结,逐渐提高。
第二篇:三组分体系相图绘制
实验八 三组分体系等温相图的绘制
【目的要求】
1. 熟悉相律,掌握用三角形坐标表示三组分体系相图。
2. 掌握用溶解度法绘制相图的基本原理。
【实验原理】
对于三组分体系,当处于恒温恒压条件时,根据相律,其自由度f*为:
f*=3-Φ
式中,Φ为体系的相数。体系最大条件自由度f*max=3-1=2,因此,浓度变量最多只有两个,可用平面图表示体系状态和组成间的关系,通常是用等边三角形坐标表示,称之为三元相图。如图2-8-1所示。
等边三角形的三个顶点分别表示纯物A、B、C,三条边AB、BC、CA分别表示A和B、B和C、C和A所组成的二组分体系的组成,三角形内任何一点都表示三组分体系的组成。图2-8-1中, P点的组成表示如下:
经P点作平行于三角形三边的直线,并交三边于a、b、c三点。若将三边均分成100等份,则P点的A、B、C组成分别为:A%=Pa=Cb,B%=Pb=Ac,C%=Pc=Ba。
苯-醋酸-水是属于具有一对共轭溶液的三液体体系,即三组分中二对液体A和B,A和C完全互溶,而另一对液体B和C只能有限度的混溶,其相图如图2-8-2所示。
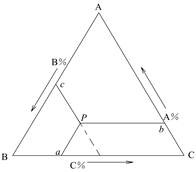
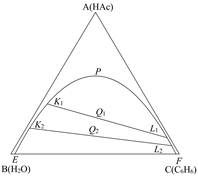
图2-8-1 等边三角形法表示三元相图 图2-8-2 共轭溶液的三元相图
图2-8-2中,E、K2、K1、P、L1、L2、F点构成溶解度曲线,K1L1和K2L2是连结线。溶解度曲线内是两相区,即一层是苯在水中的饱和溶液,另一层是水在苯中的饱和溶液。曲线外是单相区。因此,利用体系在相变化时出现的清浊现象,可以判断体系中各组分间互溶度的大小。一般来说,溶液由清变浑时,肉眼较易分辨。所以本实验是用向均相的苯-醋酸体系中滴加水使之变成二相混合物的方法,确定二相间的相互溶解度。
【仪器试剂】
具塞锥形瓶(100mL,2只、25mL,4只);酸式滴定管(20mL,1支);碱式滴定管(50mL,1支); 移液管(1mL,1支、2mL,1支);刻度移液管(10mL,1支、20mL,1支);锥形瓶(150mL,2只)。
冰醋酸(A.R.);苯(A.R.);NaOH (0.2000mo1·dm-3);酚酞指示剂。
【实验步骤】
1. 测定互溶度曲线
在洁净的酸式滴定管内装水。
用移液管移取10.00mL苯及4.00mL醋酸,置于干燥的100mL具塞锥形瓶中,然后在不停地摇动下慢慢地滴加水,至溶液由清变浑时,即为终点,记下水的体积。向此瓶中再加入5.00mL醋酸,使体系成为均相,继续用水滴定至终点。然后依次用同样方法加入8.00mL、8.00mL醋酸,分别再用水滴至终点,记录每次各组分的用量。最后一次加入10.00mL苯和20.00mL水,加塞摇动,并每间隔5min摇动一次,30min后用此溶液测连结线。
另取一只干燥的100mL具塞锥形瓶,用移液管移入1.00mL苯及2.00mL醋酸,用水滴至终点。之后依次加入1.00mL、1.00mL、1.00mL、1.00mL、2.00mL、10.00mL醋酸,分别用水滴定至终点,并记录每次各组分的用量。最后加入15.00mL苯和20.00mL水,加塞摇动,每隔5min摇一次,30min后用于测定另一条连结线。
2. 连结线的测定
上面所得的两份溶液,经半小时后,待二层液分清,用干燥的移液管(或滴管)分别吸取上层液约5mL,下层液约1mL于已称重的4个25mL具塞锥形瓶中,再称其质量,然后用水洗入150mL锥形瓶中,以酚酞为指示剂,用0.2000mol·dm-3标准氢氧化钠溶液滴定各层溶液中醋酸的含量。
【注意事项】
? 因所测体系含有水的成分,故玻璃器皿均需干燥。
? 在滴加水的过程中须一滴一滴地加入,且需不停地摇动锥形瓶,由于分散的“油珠”颗粒能散射光线,所以体系出现浑浊,如在2~3min内仍不消失,即到终点。当体系醋酸含量少时要特别注意慢滴,含量多时开始可快些,接近终点时仍然要逐滴加入。
? 在实验过程中注意防止或尽可能减少苯和醋酸的挥发,测定连结线时取样要迅速。
? 用水滴定如超过终点,可加入1.00mL醋酸,使体系由浑变清,再用水继续滴定。
【数据处理】
1. 从附录中查得实验温度时苯、醋酸和水的密度。
2. 溶解度曲线的绘制
根据实验数据及试剂的密度,算出各组分的质量百分含量。图2-8-2中E、F两点数据如下:
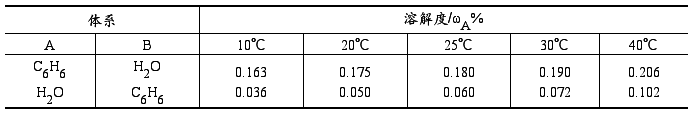
将以上组成数据在三角形坐标纸上作图,即得溶解度曲线。
2. 连结线的绘制
(1) 计算二瓶中最后醋酸、苯、水的质量百分数,标在三角形坐标纸上,即得相应的物系点Q1和Q2。
(2) 将标出的各相醋酸含量点画在溶解度曲线上,上层醋酸含量画在含苯较多的一边,下层画在含水较多的一边,即可作出K1L1和K2L2两条连结线,它们应分别通过物系点Q1和Q2。
思 考 题
1. 为什么根据体系由清变浑的现象即可测定相界?
2. 如连结线不通过物系点,其原因可能是什么?
3. 本实验中根据什么原理求出苯-醋酸-水体系的连结线?
【讨论】
1. 该相图的另一种测绘方法是:在两相区内以任一比例将此三种液体混合置于一定的温度下,使之平衡,然后分析互成平衡的二共轭相的组成,在三角坐标纸上标出这些点,且连成线。此法较为繁琐。
2. 含有两固体(盐)和一液体(水)的三组分体系相图的绘制常用湿渣法。原理是平衡的固、液分离后,其滤渣总带有部分液体(饱和溶液),即滤渣,但它的总组成必定是在饱和溶液和纯固相组成的连结线上。因此,在定温下配制一系列不同相对比例的过饱和溶液,然后过滤,分别分析溶液和滤渣的组成,并把它们一一连成直线,这些直线的交点即为纯固相的成分,由此亦可知该固体是纯物还是复盐。
-
二组分金属固液相图的绘制
专业材料化学学号080240008实验人胡文想同实验人李会勇实验名称物化实验气压101325Kpa温度25二组分金属固液相图的绘制…
- 二组分固液相图的绘制
-
Sn-Bi二组分固液相图的绘制
SnBi二组分固液相图的绘制实验目的1掌握热分析法绘制二组分固液相图的原理和方法2了解纯物质与混合物步冷曲线的区别并掌握相变点温度…
- 二组分固液相图的绘制
-
二组分合金相图的绘制实验报告
二组分合金相图的绘制一实验目的1通过实验用热分析法测绘锡铋二元合金相图2了解热分析法的测量技术与有关测量温度的方法二实验原理绘制相…
-
二组分合金相图的绘制实验报告
二组分合金相图的绘制一实验目的1通过实验用热分析法测绘锡铋二元合金相图2了解热分析法的测量技术与有关测量温度的方法二实验原理绘制相…
-
二组分金属相图的绘制
实验七二组分金属相图的绘制实验目的1学会用热分析法测绘SnBi二组分金属相图2了解纯物质的步冷曲线和混合物的步冷曲线的形状有何不同…
-
实验六 二组份合金体系相图的绘制
深圳大学实验报告课程名称报告人实验时间实验报告提交时间教务部制目的要求一用热分析法测量铅锡二元金属相图了解固液相图的基本特点二学会…
-
实验六 二组份合金体系相图的绘制
二组份合金体系相图的绘制目的要求一用热分析法测量铅锡二元金属相图了解固液相图的基本特点二学会热电偶测温技术三掌握可控升降温电炉和数…
-
二组分金属相图的绘制
二组分金属相图的绘制一实验目的1用热分析法冷却曲线法测绘BiSn二组分金属相图2了解固液相图的特点进一步学习和巩固相律等有关知识二…
-
物化实验报告_双液系的气液平衡相图
实验5双液系的气液平衡相图丛乐20xx011007生51实验日期20xx年11月10日星期六提交报告日期20xx年11月24日星期…