化学-电解质溶液-同离子效应”实验报告
中国石油大学(华东)现代远程教育
实验报告
课程名称:普通化学 / 化学原理1
实验名称:电解质溶液-同离子效应
实验形式:在线模拟+现场实践
提交形式:在线提交实验报告
学生姓名: 学号:
年级专业层次:
学习中心:
提交时间: 2014年 5月 9日

备注:该报告纳入考核,占总评成绩的10%。
第二篇:实验报告 - 副本

化学工程与工艺专业
“工程化关键技术研究实验”
实验报告

实验项目:ZrO2基固体电解质的制备、结构
 与电学性能表征
与电学性能表征
 姓 名: 朱钊
姓 名: 朱钊
学 号: 041102219
指导教师: 钟富兰
化学化工学院
20##年10月
ZrO2基固体电解质的制备、结构与电学性能表征
摘要
本论文采用共沉淀法,以一定计量的Y(NO3)3·6H2O和ZrOCl2·8H2O为原料,氨水为沉淀剂,制备一系列掺杂不同含量的Y2O3-ZrO2固体电解质,通过进行XRD、SEM表征以及利用电化学分析仪测试了固体电解质的导电率,研究了不同Y2O3含量及温度对ZrO2固体电解质的晶体结构、形貌对其导电性能的作用规律。结果表明:
关键词:共沉淀法;Y2O3-ZrO2固体电解质;XRD;SEM;电导率
第一章 前言
1.1研究背景
固体电解质或称为快离子导体是是在一定温度以上具有离子导电性质的一类固体物质。它与材料的晶体结构和物理性能有着直接的关系。研究最多的固体电解质是以ZrO2为代表的氧离子导体(实质是氧空穴传导)[1]。ZrO2是一种新型的陶瓷材料,也是应用得最早的固体电解质材料之一[2]。Nernst 在 1900 年发现了 Y2O3稳定化 ZrO2 的离子导电性,20 世纪 50 年代 Kingery 和 Wagner 提出离子空位导电机理[3]。Y2O3稳定的ZrO2(YSZ)固体电解质,具有较高的氧离子导电性,良好的机械性能,优秀的耐氧化和耐腐蚀性以及不与电极材料反应等优点而成为制作氧传器、高温固体燃料电池、压电陶瓷、铁电陶瓷以及氧泵等的主要材料,而氧化钇稳定氧化锆粉体超细的晶粒粒度、颗粒的均匀性和合理的成分配比是获得高离子电导性能和良好机械强度YSZ固体电解质的关键。目前人们研究、使用了共沉淀法,so-l gel法、水热法、共沉淀-凝胶法、醇-水溶液法、共沸蒸馏技术、微波辅助法、反胶团法或微乳液法等多种制备氧化锆粉体的方法[4]。但这些方法都有其各自的优点,同时也有其不足之处,所以,探索一种操作简单,成本低廉,并且可以得到高质量 ZrO2纳米粉体的制备方法,并提高其电导率和载氧量就成了人们努力的方向。
1.2 ZrO2的晶体结构及其稳定化
ZrO2有三种晶型结构:单斜(M)、四方(T)和立方(C)晶型。其晶型变化如下:

这些相变导致很大的体积效应,如加热时,单斜晶转变为四方晶,体积收缩 7-9%;在冷却过程中,其结果与前者相反。四方晶向立方晶转变也会出现类似的情况。加上材料的导热系数小,热膨胀系数大,使得纯ZrO2的抗热震性极差而无法直接使用。因此,首先要对纯 ZrO2进行稳定化处理。对 ZrO2进行稳定化处理就是在纯 ZrO2中添加适量的二价或者三价立方对称氧化物(如 Y2O3、MgO、CaO、CeO2等)。高温下这些立方格子的氧化物在 ZrO2的原始晶格上施加一个很小的压力,强迫 ZrO2形成立方萤石结构[5,6]。
1.3 Y2O3-ZrO2固体电解质的反应机理
在ZrO2晶格中,2个Zr4+周围最近邻有4个O2-,而加入Y2O3后,Y3+置换了晶格上的Zr4+,为了保持电中性,2个Y3+周围只能有3个O2-,而置换前应有4个O2-,这样就出现了1个氧离子(O2-)空位。在高温下,当YSZ两侧存在氧浓度差或电压时,这些氧离子空位可接受氧离子,使氧离子从一侧向另一侧定向移动,这就是YSZ的氧离子空位导电机理,YSZ也被称为固体电解质[7]。因此,全稳定化 ZrO2在形成的立方固溶体中产生大量的氧离子空位,具有很高的离子导电性,是优良的固体电解质,已在许多方面得到广泛应用。
1.4研究意义
汽车发动机工作时除了排出CO2外,还会产生大量的光化学烟雾气体CO、HC、NOX(以NO为主的氮氧化合物)等,对人类及动植物的生存环境造成严重的污染。出于环保的要求,许多汽车在排气系统中安装了三元催化器以减少CO、HC、NOX的排放量。但是三元催化器只有在理论空燃比(A/F=14.7:1)附近时净化率才最高,若混合气浓度偏离理论空燃比,则净化效果将急剧下降。因此,必须使用氧传感器,并通过检测排气管中氧的含量,向电子控制器提供混合气空燃比反馈信息,使电子控制器及时修正喷油量,将混合气浓度严格控制在理论空燃比左右很窄的范围内[8]。而用钇、钙、镁等元素的氧化物作稳定剂制备的氧化锆陶瓷,在高温下是以氧离子为载流子的固体电解质,可以广泛应用于制作氧气传感器和高温燃料电池等领域。再通过控制发动机的空燃比,并与三元催化剂、电喷、电子控制单元共同组成闭环控制系统 , 达到彻底治理汽车尾气污染的目的。日本、美国的汽车用氧气传感器的年用量均达几千万只[9]。
目前,ZrO2基的电解质材料是人们研究得最为充分的材料,ZrO2基固体电解质是迄今为止最为有实际意义和应用前景的固体电解质,这其中,可以挖掘的“宝藏”巨大。所以,实验以Y(NO3)3·6H2O和ZrOCl2·8H2O为原料,氨水为沉淀剂,制备一系列掺杂不同含量的Y2O3-ZrO2固体电解质,并对其进行测试,以探究Y2O3含量及温度对ZrO2固体电解质的体密度和导电性能的影响。
第二章 实验部分
2.1.实验目的
(1)加深对固体电解质及其导电性能基本原理的理解,通过该实验,了解固体电解质的晶体结构、形貌对其导电性能的作用规律,理解反应过程中热力学与动力学的不同作用原理;
(2)掌握共沉淀法合成Y2O3-ZrO2固体电解质,并用粉末压片机压片的原理与方法,学会应用电化学分析仪测试固体电解质电导率的方法。
2.2 实验药品及仪器
1.实验药品:
表2-1 化学试剂
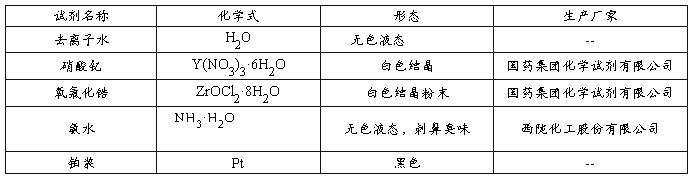
2.实验仪器和设备
锥形瓶4个,小坩埚4个,小瓷碗4个,玻棒4只,烧杯4个,药匙、称量纸若干
电子天平,电动搅拌器(D2004W),粉末压片机,电化学分析仪(CHI660),高速离心分离机(TDL-5-4),电热恒温鼓风干燥箱;
2.3.Y2O3-ZrO2固体电解质的制备
2.3.1实验流程及装置
本实验流程如图2-1所示。
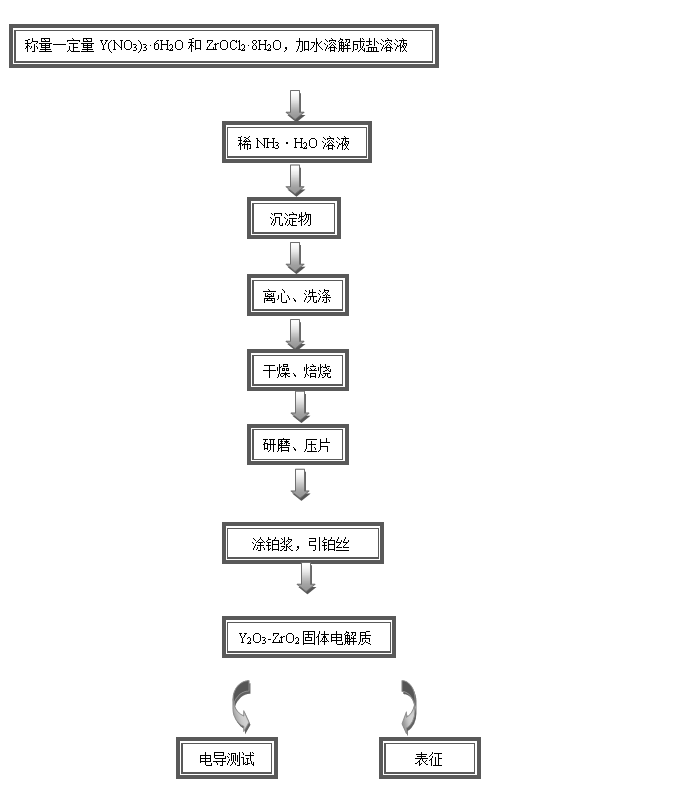
图2-1Y2O3-ZrO2固体电解质研究实验流程图
2.3.2实验步骤
1准备工作
(1)计算化学计量比2.0mol%,5.0mol%,8.0mol%,12.0mol%Y(NO3)3·6H2O和ZrOCl2·8H2O固体。
计算过程:(以5.0mol%的计量比为计算示例,其余结果详见表2.2。)
Y(NO3)3·6H2O分子量:383.04 ZrOCl2·8H2O分子量:322.25
n(Y2O3):n(ZrO2)=5:95
n(Y3+):n(Zr4+)=n(Y(NO3)3·6H2O):n(ZrOCl2·8H2O)=10:98
m(Y(NO3)3·6H2O):m(ZrOCl2·8H2O)= nM(Y(NO3)3·6H2O):nM(ZrOCl2·8H2O)
m(Y(NO3)3·6H2O):m(ZrOCl2·8H2O)=3830.4:30613.8
表2-2 不同含量Y(NO3)3·6H2O和ZrOCl2·8H2O固体
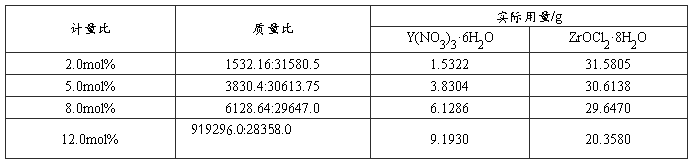
(2)称量已经计算好质量的Y(NO3)3·6H2O和ZrOCl2·8H2O固体,并加入250ml的去离子水于烧杯中溶解成盐溶液。
(3)称量一定量的浓度为14.79mol/L浓NH3·H2O溶液于锥形瓶中,加入去离子水配成稀溶液。
计算过程:(以2.0mol%的计量比为计算示例)
Y2O3-ZrO2粉体的合成反应式如下:
Y3+ + 3OH- → Y(OH)3
Zr4+ +4OH- → Zr(OH)4
n(Y3+) : n(OH-)=1 :3 n(Zr4+) : n(OH-)=1:4
理论所需n(NH3·H2O)=0.404mol
理论所需V(NH3·H2O)=n/c =0.404/14.79=0.0273L
但由于浓氨水的挥发性较强,且为保证合成液PH≥9,所以实际每个样品浓氨水的用量都为45ml,并加入400ml去离子水进行稀释置于4个锥形瓶中;
2. 进液合成、陈化、老化
(1)合成阶段首先是在较高转速800r/min下往锥形瓶中迅速倒入溶解好的盐溶液,并重复此步骤,将四个含量不同的盐溶液分别迅速加入四个有碱液的锥形瓶中进行反应;
现象:瓶中立刻产生白色浑浊沉淀,且由于沉淀的产生,搅拌桨转速略有降低,待其合成反应基本稳定后,将转速降至600r/min。
为控制合成反应的PH值≥9左右。实验过程中,使用玻璃棒将溶液滴至测量PH值为8.2-10的试纸上,观察试纸颜色变化,对照比色卡,若PH试纸显深蓝色,可认为PH值在9左右。若浅于这个颜色,则认为盐过量,加碱。若深于这个颜色,则视为碱过量,可视为正常。经检验,四个合成液的PH值都符合要求。
(2)陈化是在不滴加溶液的条件下,保持温度、PH值、搅拌速率(600r/min)
不变,使原溶液充分反应。
该过程时间约为5-6h。
(3)老化是停止搅拌,静置。
该过程时间较长,可直接等到第二天再进行下步操作。
3.离心、洗涤
为了充分滤去杂质,进行5次离心、洗涤。将锥形瓶中的反应沉淀物和合成液仔细倒入两个离心杯中,加蒸馏水使两杯质量大致相同,放入高速离心分离机中。当离心机转速到达4000 r/min时,时间持续为7-8min后停止,完成后取出,倒掉上层溶液,加蒸馏水至离心杯2/3处,充分搅拌,使之完全溶解。再次放入离心机中,转速仍设为4000r/min,。重复以上实验5次,即可得到所需的干净样品。
现象:得到白色泡沫状,粘性较大,含水量较多的样品。
4.烘干
将离心后得到的样品小心刮入小瓷碗中,放入烘箱进行干燥,设置温度为110℃。
现象:得到干燥的白色呈块状固体。
5.焙烧
从烘箱得到干燥的样品,并将其转移进4个干净的小坩埚中放入炉中焙烧,设置温度1000℃,使氢氧化物转化成氧化态。焙烧完成后使之降至室温。
现象:得到干燥的白色小块状固体。
6.研磨压片
将焙烧好的样品研磨成粉末状后用压片机进行压片;
现象:得到小圆片状固体电解质。
7. 涂铂浆,引铂丝
将压片好的Y2O3-ZrO2固体电解质点上少许Pt 浆,并引出Pt 丝作为敏感电极SE,同时在基片的另一侧,刷上Pt 浆并引出Pt 丝作为参考电极RE。
至此,Y2O3-ZrO2固体电解质基本已经制备完成,接下来就是进行电化学分析仪测试和XRD,SEM表征。
2.4. 实验数据处理和分析
实验过程中,由于2mol%Y2O3-ZrO2的样品电极制作未成功,所以实际测得有含量为5.0mol%,8.0mol%,12.0mol%Y2O3-ZrO2固体电解质这三组数据。
2.4.1样品的表征
对烧结后的样品用SEM分析粉末的颗粒形貌、大小及其分布;高温烧结后的陶瓷片用X - 射线衍射方法分析其致密性及结构;对制备有电极及电极引线的样品用电化学分析仪(CHI660)测量其电导率等性能。
(1)采用X 射线衍射仪对粉体的相结构和组成进行测定。图2.2 为1 000 ℃烧结的3 种含量样品的 XRD 谱图。
结果表明:
1.从图中可以看出,图中所有谱线均是ZrO2,而没有钇的任何化合物谱线出现,表明Y2O3在ZrO2中完全形成了固溶体。
2. 从图中谱线看出, Y2O3-ZrO2经高温烧结、压制成型后 , 存在立方晶体结构。所以,Y2O3对于ZrO2高温立方相在室温下的稳定起决定作用。
3.从图中三种含量的Y2O3-ZrO2谱线都出现在同一位置说明,当Y2O3的含量到5.0mol%以上后的样品基本就都转化为了立方相。

图 2.2 不同含量Y2O3-ZrO2 X - 射线衍射图
(2)选取含量采用扫描电子显微镜观察其样品的形貌,图2.3 为含量为8.0mol%的Y2O3-ZrO2样品的SEM图。
结果表明:
从图中可以看出,烧结体没有硬团聚,结构紧密,致密性程度高。

图 2.3 含量8.0mol%的Y2O3-ZrO2 的SEM图
2.4.2样品的电导测试
采用电化学分析仪(CHI660)测试固体电解质的电阻,运用软件excel制表,oringin绘图,可得以下图表:
表2-3 5mol%Y2O3-ZrO2固体电解质导电性能与温度关系
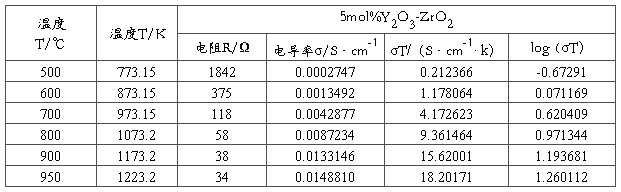
表2-4 8mol%Y2O3-ZrO2固体电解质导电性能与温度关系

表2-5 12mol%Y2O3-ZrO2固体电解质导电性能与温度关系
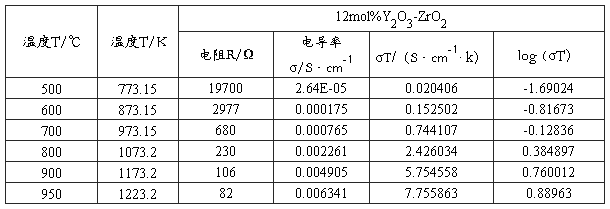
根据表2-3、2-4、2-5的数据结果,根据Arrhenius定律:σ=(σo/T)exp(-Ea/kT)对两边取对数得:log(σT)=(-Ea/kT)+logσo
其中:k 为波尔兹曼常数,k =0. 86 ×10-4eV·K-1;σ0为起始电导率,在一定的温度范围内近似为一常数; E 为材料的电导活化能。
将log(σT)对1/T作图,根据所得直线的斜率可求得电导激活能。

图 2.4 三种含量Y2O3-ZrO2的log(σT)-1 000/T 曲线
通过oringin的绘图和线性拟合公式y=A+Bx,其中,A表示logσo,B表示(-Ea/k)可得表2.6的数据:
表2-5 三种不同含量Y2O3-ZrO2lg(σT)-1 000/T 曲线斜率
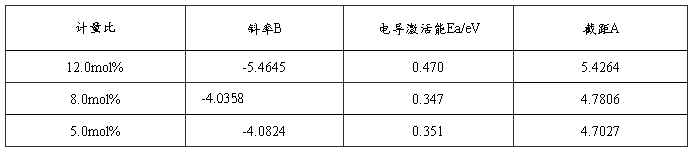
结果表明:
(1)由图2.4可以看出1og(σT )与1/T表现出良好的线性关系,其中,含量为5.0mol% 与8.0mol%的Y2O3-ZrO2电导率比较相近,而与含量12.0mol%的晶体电导率与温度线性关系最好,但与另两种含量电导率差别较大。
(2)Y2O3-ZrO2固体电解质电导率随温度的变化关系如图2.4所示,可以看出虽然随着温度的升高,晶粒电导率有增大趋势,由表2-3、2-4、2-5可知,含Y2O3-ZrO2固体电解质随着温度的升高,其电导率增大的幅度是减小的。
(3)由图2.4和表2-6可知,含量为8.0%的Y2O3-ZrO2电解质的电导率最大,电导激活能最小,电导率的关系是含量8.0mol%>5.0mol%%>12.0mol%,而电导活化能关系则与之相反。
2.5 结论
通过对不同Y2O3含量的ZrO2基固体电解质性能的研究表明,添加适量的Y2O3可以提高ZrO2基固体电解质的稳定性和电导性等各种性能,并且在不同温度和不同含量上有不同的表现:
(1)添加一定量的Y2O3后,可与ZrO2形成固溶体,其晶体结构为立方相保证了ZrO2基固体的稳定性,并且提高了其致密化程度。
(2)添加一定量的Y2O3后,固体电解质的电导率在一定含量Y2O3内随含量的增加,电导率也增大,这是因为随着稳定剂含量的增加,氧离子空位浓度增加,所以,电导率也随之增加。但当稳定剂的含量超过一定量时,其电导率反而减小,所以,在本实验中电导率的关系是含量8.0mol%>5.0mol%%>12.0mol%,这是由于氧离子空位浓度过大,使空位有序化,在库仑力、偶极矩作用力或共价键力等的共同作用下,过多的氧空位与稳定剂中的金属离子发生缺陷缔合,使氧离子空位移动的活化能增加,结果导致可以有效迁移的氧离子空位浓度减小,电导率又逐渐减小。
(3)添加一定量的Y2O3后,ZrO2基固体电解质电导率在一定的温度区域范围内,随温度的升高而增大,导电性能增强,这说明添加Y2O3对ZrO2的导电性能具有一定的作用。这是因为采用在ZrO2中添加Y2O3化合物作稳定剂的方法 , 既可以提高ZrO2系列固体电解质中的载流子——氧离子空位的浓度,又可以使ZrO2在低温下以四方或立方晶体的形式存在,在晶胞中存在较大的空隙,氧离子空位可以在其中畅通无阻的移动,从而显著提高其电导率。
(4)综上所述,根据样品的电导性能测试结果表明,含8.0%的Y2O3-ZrO2固体电解质以立方相存在,晶胞空隙较大,其电导率最高,电导激活能最低,性能最优,这与查阅到的相关文献结论基本一致。表明本实验基本成功。
参考文献
[1] 豆斌朝,林振汉, 吴 亮, 平信义.氧化锆固体电解质的掺杂性能和应用.综合评述[J].2004.23(6).
[2] 唐超群,章天金,吴蓉,王世敏.ZrO2基固体电解质型燃料电池的研究现状及发展趋势.材料导报[J].1996.37-38
[3] 李英,龚江宏,唐子龙,张中太. ZrO2基固体电解质研究进展.陶瓷学报[J].1997.18(4).
[4] 王洪升,王 贵,张景德,徐廷鸿. 钇稳定氧化锆纳米粉体制备技术研究进展.硅酸盐通报[J].2006.25(6).
[5] 斯温M V.陶瓷的结构与性能[M].郭景坤译.北京:科学技术出版社,1998.508-509.
[6] 雷复兴,寇志奇,曾忠琼,等.ZrO2·Y2O3固体电解质及测氧探头的研制[J].耐火材料,1996,30(5):248-251.
[7] 石敏,刘宁.ZrO2基固体电解质氧传感器的研究现状及发展趋势. 合肥工业大学学报(自然科学版).2003,26(3).
[8] 孙焕军, 于春鹏. ZrO2基固体电解质氧传感器在汽车上的应用. 黑龙江工程学院学报(自然科学版).2004,18(4).
[9] 陈家林,万吉高,王开军,陈亮维,马骏. 氧传感器用 Z rO2- Y2O3 固体电解质电导性能的研究. 贵金属. 2001,22(1).
致谢
很感谢钟富兰老师的悉心指导以及耐心的为我们解答,以致我们能顺利地完成这篇论文。钟老师用自己超强的耐力和亲切的态度让我们在做实验的同时也感到愉快,并在试验完成后及时督促我们按时完成实验报告。同时也要感谢冯小璐和许佳源同学的共同努力,期间密切的合作和互相信任才使得实验能够更快的完成
-
实验四 电解质溶液
实验四电解质溶液一实验目的1了解强弱电解质电离的差别及同离子效应2学习缓冲溶液的配制方法及其性质3熟悉难溶电解质的沉淀溶解平衡及溶…
-
电解质溶液实验报告
化学教学论实验电解质溶液实验报告学院:化学化工学院班级:10级化教班组:第八组组员:###电解质溶液一、实验目的1、了解电解质溶液…
-
电解质溶液及配位化合物 实验报告
西安交通大学实验报告课程大学化学实验实验名称电解质溶液及配位化合物系别电气实验日期2011年11月11日专业班号钱学森12组别二交…
-
实验一 电解质溶液
实验一电解质溶液一目的要求1学习和掌握酸碱解离平衡的特点及其移动2学习和掌握难溶电解质的多相解离平衡及其移动3进一步学习缓冲溶液的…
-
化学-电解质溶液-同离子效应”实验报告
中国石油大学华东现代远程教育实验报告课程名称普通化学化学原理1实验名称电解质溶液同离子效应实验形式在线模拟现场实践学生姓名号年级专…
-
化学-电解质溶液-同离子效应”实验报告
中国石油大学华东现代远程教育实验报告课程名称普通化学化学原理1实验名称电解质溶液同离子效应实验形式在线模拟现场实践学生姓名吴洪涛号…
-
化学-电解质溶液-同离子效应”实验报告
中国石油大学华东现代远程教育实验报告课程名称普通化学化学原理1实验名称电解质溶液同离子效应实验形式在线模拟现场实践学生姓名赵达飞号…
-
普通化学-电解质溶液-同离子效应”实验报告
中国石油大学华东现代远程教育实验报告课程名称普通化学化学原理1实验名称电解质溶液同离子效应实验形式在线模拟现场实践学生姓名学号年级…
-
电解质溶液实验报告
化学教学论实验电解质溶液实验报告学院:化学化工学院班级:10级化教班组:第八组组员:###电解质溶液一、实验目的1、了解电解质溶液…
-
实验四 电解质溶液
实验四电解质溶液一实验目的1了解强弱电解质电离的差别及同离子效应2学习缓冲溶液的配制方法及其性质3熟悉难溶电解质的沉淀溶解平衡及溶…
-
氯化钠溶液的配置实验报告
实验4配制100mL100molL的NaCl溶液班级姓名实验目的1练习配制一定物质的量浓度的溶液2加深对物质的量浓度概念的理解3练…