库仑滴定测定硫代硫酸钠的浓度实验报告
库仑滴定测定硫代硫酸钠的浓度
一、 目的要求
1、掌握库仑滴定法的原理及化学指示剂指示终点的方法
2、应用法拉第定律求算未知物的浓度
二、 原理
在酸性介质中,0.1mol/L KI在Pt阳极上电解产生“滴定剂”I2来“滴定”S2O32-,用淀粉指示终点。通过电解所消耗的库仑数计算Na2S2O3的浓度。
具体为:使碘离子在铂阳极上氧化为碘,然后与试液中S2O32-的作用,工作电极对的电极反应为: 阳极: 2I- = I2 +2e
阴极: 2H+ +2e = H2
滴定反应:I2 + 2S2O32- 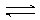 S4O62- +2I-,可用淀粉指示剂指示终点。当S2O32-全部被氧化为S4O62-后,过量的碘将在指示电极上析出,溶液出现淀粉蓝,停止电解。根据电解产生碘时所消耗的电量,即可按法拉第定律计算溶液中Na2S2O3含量。
S4O62- +2I-,可用淀粉指示剂指示终点。当S2O32-全部被氧化为S4O62-后,过量的碘将在指示电极上析出,溶液出现淀粉蓝,停止电解。根据电解产生碘时所消耗的电量,即可按法拉第定律计算溶液中Na2S2O3含量。
三、 仪器与试剂
仪器: 恒电流库仑滴定装置一套,铂电极两支。
试剂: 0.1mol/L KI溶液:称取1.7gKI溶于100ml蒸馏水中待用;未知浓度的Na2S2O3溶液;0.1% 淀粉溶液。
四、 实验步骤
(1)将Pt片工作电极接仪器的白、绿夹子,Pt丝辅助电极接黄、红夹子。
阳极电解杯中加入20ml H2SO4,5ml 0.1mol/L KI溶液, 0.1%淀粉2-3滴,放入搅拌子,阴极电解杯中加入20ml H2SO4,分别插入Pt片和Pt丝电极,使电极恰好被溶液浸没,
(2)预电解
该步骤的目的是为了除去KI溶液存在比I- 更容易被氧化的杂质,溶液变蓝后,滴加几滴稀Na2S2O3,使溶液的兰色褪去。
(3) 测量:准确移取Na2S2O3试液0.5ml置于阳极电解杯中,开始电解的同时记录时间。溶液变蓝即为电解终点,停止电解,记下所用时间。
(4) 重复三次
(5) 关闭搅拌器,清洗电解杯和电极。关闭软件、仪器、电脑,将实验台收拾干净。
五、 结果处理
1.计算Na2S2O3的浓度:
C Na2S2O3 =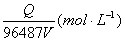
式中:Q为库仑数,V为试液体积数

I=30mA=0.03A V=0.5mL Q=It
计算得:
C1=0.0460mol·L-1
C2=0.0454mol·L-1
C3=0.0485mol·L-1
2.计算浓度的平均值。
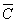 =0.0466mol·L-1
=0.0466mol·L-1
3.标准偏差:S=1.6×10-3
RSD=(1.6×10-3 ÷0.0466)×100%=3.43%
六、实验反思
本次试验比较简单,但是由于仪器的问题,耗时较长,关键在于溶×液变蓝的观察是否敏锐与及时,在电化学中是一个典型知识点的应用,将理论与实际相结合,比较有趣。且在本次试验中,小组之间的配合显得尤为重要,只有组员之间分工明确,才能做好本次试验。
第二篇:库伦法滴定硫代硫酸钠的浓度
陕西师范大学
仪器分析实验报告
姓名:徐碧云
年级:2013级
班级:化学三班
库仑滴定法测定硫代硫酸盐
一、实验目的
1、巩固库仑滴定法和死停终点法的原理。
2、掌握库仑滴定法的实验技术。
二、实验原理
库仑滴定法是建立在恒电流电解过程基础上的一种准确而灵敏的分析方法。可用于常量和痕量物质的测定,通过电极反应产生与待测物质定量反应的“滴定剂”,滴定终点借助电化学方法或指示剂指示。根据法拉第定律由滴定过程中消耗的电量计算被测量物质的含量。
在酸性介质中,碘离子极容易以100%的电流效率在铂电极上氧化生成碘,电极生成的碘滴定S2O3,以死停终点法指示终点,可进行Na2S2O3的测定。
在含有Na2S2O3的碘化钾溶液中进行恒电流电解质, 阳极反应为2I=I2+2e-
阳极产生的碘与S2O3进行定量反应:I2+2S2O3=2I+S4O6,阴极的反应为H+2e-=H2
为了防止阴极产物对测定的干扰,可用盐桥或底部为微孔玻璃板的玻璃套管将阳极和阴极分开。
由于上述反应,在化学计量点之前溶液中没有过量的I2,不存在可逆电对,因而两个铂指示电极回路中无电流通过,当继续电解,产生的I2全部与Na2 S2O3作用完毕,稍过量的2+2-2--2--2-
I2即可与I离子形成I2/ I可逆电对,此时在指示电极上发生下列反应:
指示阳极 2I=I2+2e-
指示阴极 I2+2e-=2I- ---
由于在两个指示电极之间保持一个很小的电位差(约200mV),所以此时在指示电极回路中立即出现电流的突跃,以指示终点到达。
正式滴定前,需进行预电解,以清除系统内还原性干扰物质,提高标定确度。
本实验采用江苏电分析仪器厂生产的KLT-I型通用库伦仪进行测定,其工作原理是:
1、 终点方式选择控制电路:指示电极由用户自己选用,其中有一片铂片,电位法和电流法指示共用,面板设有“电位,电流”“上升、下降”琴键开关,任用户根据需要选择。指示电极的信号经过放大器进行放大,然后经微分电路输出一脉冲信号到触发电路,推动开关执行电路去带动继电器是电解回路吸合、释放。
2、 电解电流变换电路:由电压源,隔离电路及跟随电路组成。电解电流大小可通过变换射极电阻大小获得,电解电流共用5mA、10Ma、50mA三档,由于电解回路与指示回路的电流是分开的,故不会产生电解对指示的干扰。
3、 电量积算电路:该电路包括电流采样电路、V-f转换电
路及微型电路。分频电路等组成部分。积分精度可达0.2-0.3%,能满足一般通用库伦分析的要求。
4、 数字显示电路:该电路全采用CMOS集成复合块,数码管是4位LED显示。
三、实验仪器与试剂
1、仪器:KLT-I型通用库伦仪、配套电解池、磁力搅拌器、10mL移液管、2mL吸量管、烧杯2个。
2、 试剂:电解液0.1mol/LKI溶液,0.1mol/LHAc-NaAc缓冲溶液;待测约含 Na2 S2O3
四、实验步骤
1、仪器准备,接通电源,打开仪器预热10min
2、将电解池清洗干净,量取0.1 mol/L KI 溶液和0.1 mol/L HAc-NaAc 缓冲溶液个40 mL于电解池中,放入磁子,将电解池放在电磁搅拌器上,搅拌。
3、将电极系统装在电解池上(铂片要完全浸入试液中,磁子不能碰到电极),在铂丝阴极隔离管中注入电解液至管的2/3部位,是隔离管内的液面略高于电解池中的液面。铂片电极接“阳极”(红线),隔离管中铂丝电极接“阴极”(黑线)。将指示电极连线夹头接在另一对铂片电极的引出线上。
4、预电解:加入3-5滴Na2S2O3溶液。
“量程选择”置10mA档,按下【电流】、【上升】、和【启2-
动键】,调节“补偿极化电位”旋钮使其指针至0.4,按下【极化电位】,调节微安表示数为10,弹起【极化电位】。【工作/停止】开关置工作状态,按下【电解】按钮,此时指示灯灭,电解过程开始。观察显示器数值,当指示灯亮,电解停止,显示器显示的电量即为此次电解KI所消耗的电量(注意电量是mQ)。弹起【启动】按键,再滴加几滴Na2S2O3溶液,按下【启动】按键,按下【电解】按钮开始电解,“终点指示灯”亮,终点到。为能熟悉终点的判断,可如此反复练习几次。
5、准确移取待测Na2S2O3溶液1mL加入到电解池中,按下【启动】按键,按【电解】按钮开始电解,“终点指示灯“亮,终点到,记下电量值(mQ),【工作/停止】开关置停止状态,弹起【启动】,示数清零。重复试验5次。电解液可反复多次使用,不必更换;若电解池中溶液过多,可倒去部分后,继续使用。
6、关闭仪器电源。将电解液倒入回收瓶中,洗净电解池及电极(注意清洗铂丝阴极隔离管)。
五、数据处理。
根据几次测量的结果,根据法拉第定律计算Na2S2O3溶液的浓度(mol/L)。
C=Q/96487V
式中Q为消耗的电量(mQ),V是所取待测溶液的体积(mL),
测量次数:3次
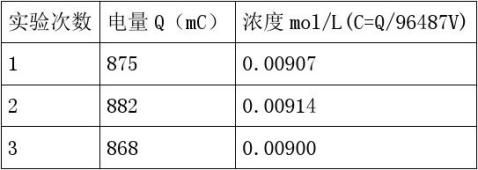
则C(Na2S2O3)=(0.00907+0.00914+0.00900)/3=0.00907 mol/L
式中:Q为毫库伦数,V为试液体积数
相对标准偏差
SD={[(0.00907-0.00907)+(0,。00914-0.00907)+(0.00900-0.00907)]/2}=0.00007
RSD=(SD/0.00907)*100%=(0.00007/0.00907)*100%=0.772% 经计算Na2S2O3溶液的浓度为0.00907 mol/L
六、思考题
1、本实验是如何获得恒电流的?
2、指示电极上所加电压太大或太小对终点指示有何影响?
3、讨论本实验可能产生的物产的来源和减小误差的方法。 解:1、通过外加电压,保持电流恒定。电解电流大小可通过变换射极电阻大小获得。
2、指示电极上所加的电压太大,导致滴定终点延后,是测定值偏大;指示电极上所加的电压太小,导致滴定终点提前,使测定值偏小。 20.522
3、(1)误差来源:移取Na2S2O3的时不准确;按下“停止电解”建出现延迟;(2)减小误差的措施:移取溶液时应正确操作,平视读数,避免出现漏液的现;或者采取更为精密的移液仪器,移液应由一人来完成,按键的操作也应由同一人来完成。
七、实验反思与讨论
1、电极的极性切勿接错,若接错必须仔细清洗电极。
2、每次试液必须准确移取。
3、本次实验不需要配制标准溶液和加入指示及,就不存在标准溶液稳定性和判断滴定终点颜色偏差的问题
4、 电流效率低于100%时,可能会发生非预期的副反应
5、 工作电极采用大面积的铂电极,加大了反应的电流利用效率
6、这次实验我们小组测试了11次,由于库伦滴定仪内部电路出现了问题,当电解停止时,溶液变成了黄色,说明到达指示终点时,电解过程仍在进行,溶液中有I2生成。我们小组在11组数据中选择了三组电解结束后溶液不变色的数据,其余数据均舍弃了
7、通过这次的实验,说明我们不能一味的依赖仪器,在用仪器做实验的过程中,要有思考,有自己的见解,实验过程中出现的问题要学会判断是仪器出现问题还是实验操作出现问题,不断的探索不断的改进。
-
硫代硫酸钠的制备实验报告
硫代硫酸钠的制备班级化工122姓名茆邦宇学号120xx280327摘要实验目的在于提升同学对于硫代硫酸钠制备方法的了解进一步熟悉蒸…
-
实验十八教案 硫代硫酸钠的制备
硫代硫酸钠的制备关键词硫代硫酸钠实验目的1制备Na2S2O35H2O2练习气体的制备和仪器的安装3进一步练习过滤蒸发结晶与干燥等基…
-
硫代硫酸钠的制备
硫代硫酸钠的制备班级姓名学号摘要用亚硫酸纳法制备硫代硫酸纳在制备过程中要注意控制反应过程中的温度以及在减压热过滤冷却结晶过滤过程中…
-
硫代硫酸钠的制备实验报告
硫代硫酸钠的制备摘要实验目的在于提升同学对于硫代硫酸钠制备方法的了解进一步熟悉蒸发浓缩减压过滤结晶等相关基本操作采用亚硫酸钠法用近…
-
硫代硫酸钠的制备(化学设计实验)
摘要采用亚硫酸钠法用近饱和的亚硫酸钠溶液和硫粉共煮来制备硫代硫酸钠由于硫代硫酸钠具有不稳定性较强的还原性和配位能力所以对制好的产品…
-
硫代硫酸钠的制备实验报告
硫代硫酸钠的制备摘要实验目的在于提升同学对于硫代硫酸钠制备方法的了解进一步熟悉蒸发浓缩减压过滤结晶等相关基本操作采用亚硫酸钠法用近…
-
硫代硫酸钠的制备实验报告
硫代硫酸钠的制备班级化工122姓名茆邦宇学号120xx280327摘要实验目的在于提升同学对于硫代硫酸钠制备方法的了解进一步熟悉蒸…
-
实验十八教案 硫代硫酸钠的制备
硫代硫酸钠的制备关键词硫代硫酸钠实验目的1制备Na2S2O35H2O2练习气体的制备和仪器的安装3进一步练习过滤蒸发结晶与干燥等基…
-
硫代硫酸钠的制备
硫代硫酸钠的制备班级姓名学号摘要用亚硫酸纳法制备硫代硫酸纳在制备过程中要注意控制反应过程中的温度以及在减压热过滤冷却结晶过滤过程中…
-
硫代硫酸钠的制备(化学设计实验)
摘要采用亚硫酸钠法用近饱和的亚硫酸钠溶液和硫粉共煮来制备硫代硫酸钠由于硫代硫酸钠具有不稳定性较强的还原性和配位能力所以对制好的产品…
-
滴定法实验总结报告
蒸馏后碱滴定法1原理亚硫酸盐在酸性条件下用碱中和加热亚硫酸盐被过氧化氢吸收用碱中和并滴定至终点根据消耗标液用量计算其含量H2O2H…