邻二氮菲分光光度法测定微量铁实验报告
邻二氮菲分光光度法测定微量铁
课程名称:仪器分析
指导教师:李志红
实验员 :张丽辉 李国跃 崔凤琼
刘金旖 普杰飞 赵 宇
时 间: 20##年5月12日
一、 实验目的:
(1) 掌握研究显色反应的一般方法。
(2) 掌握邻二氮菲分光光度法测定铁的原理和方法。
(3) 熟悉绘制吸收曲线的方法,正确选择测定波长。
(4) 学会制作标准曲线的方法。
(5) 通过邻二氮菲分光光度法测定微量铁在未知式样中的含量,掌握721型,723型分光光度计的正确使用方法,并了解此仪器的主要构造。
二、 原理:
可见分光光度法测定无机离子,通常要经过两个过程,一是显色过程,二是测量过程。
为了使测定结果有较高灵敏度和准确度,必须选择合适的显色条件和测量条件,这些条件主要包括入射波长,显色剂用量,有色溶液稳定性,溶液酸度干扰的排除。
(1) 入射光波长:一般情况下,应选择被测物质的最大吸收波长的光为入射光。
(2) 显色剂用量:显色剂的合适用量可通过实验确定。
(3) 溶液酸度:选择适合的酸度,可以在不同PH缓冲溶液中加入等量的被测离子和显色剂,测其吸光度,作DA-PH曲线,由曲线上选择合适的PH范围。
(4) 有色配合物的稳定性:有色配合物的颜色应当稳定足够的时间。
(5) 干扰的排除:当被测试液中有其他干扰组分共存时,必须争取一定的措施排除干扰。
邻二氮菲与Fe2+ 在PH2.0-9.0溶液中形成稳定橙红色配合物。配合无的ε =1.1 ×104 L· mol ·cm-1 。
配合物配合比为3:1,PH在2-9(一般维持在PH5-6)之间。在还原剂存在下,颜色可保持几个月不变。Fe3+ 与邻二氮菲作用形成淡蓝色配合物稳定性教差,因此在实际应用中加入还原剂使Fe 3+还原为Fe2+ 与显色剂邻二菲作用,在加入显色剂之前,用的还原剂是盐酸羟胺。此方法选择性高Br3+ 、Ca2+ 、Hg 2+、Zn2+ 及Ag+ 等离子与邻二氮菲作用生成沉淀,干扰测定,相当于铁量40倍的Sn2+、Al3+、Ca2+、Mg2+ 、Zn2+ 、Sio32-,20倍的Cr3+、Mn2+、VPO3-45倍的Co2+、Ni2+、Cu2+等离子不干扰测定。
三、 仪器与试剂:
1、 仪器:721型723型分光光度计
500ml容量瓶1个,50 ml 容量瓶7个,10 ml 移液管1支
5ml移液管支,1 ml 移液管1支,滴定管1 支,玻璃棒1 支,烧杯2 个,吸尔球1个, 天平一台。
2﹑试剂:(1)铁标准溶液100ug·ml-1,准确称取0.43107g铁盐NH4Fe(SO4)2·12H2O置于烧杯中,加入0.5ml盐酸羟胺溶液,定量转依入500ml容量瓶中,加蒸馏水稀释至刻度充分摇匀。
(2)铁标准溶液10ug·ml-1.用移液管移取上述铁标准溶液10ml,置于100ml容量瓶中, 并用蒸馏水稀释至刻度,充分摇匀。
(3)盐酸羟胺溶液100g·L-1(用时配制)
(4)邻二氮菲溶液 1.5g·L-1 先用少量乙醇溶液,再加蒸馏水稀释至所需浓度。
(5)醋酸钠溶液1.0mol·L-1μ
四、实验内容与操作步骤:
1.准备工作
(1) 清洗容量瓶,移液官及需用的玻璃器皿。
(2) 配制铁标溶液和其他辅助试剂。
(3) 开机并试至工作状态,操作步骤见附录。
(4) 检查仪器波长的正确性和吸收他的配套性。
2. 铁标溶液的配制
准确称取0.3417g铁盐NH4Fe(SO4)·12H2O置于烧杯中,加入10mlHCL加少量水。溶解入500ml容量瓶中加水稀释到容量瓶刻度。
3 .绘制吸收曲线选择测量波长
取两支50ml干净容量瓶,移取100µ g m l-1铁标准溶液2.50ml容量瓶中,然后在两个容量瓶中各加入0.5ml盐酸羟胺溶液,摇匀,放置2min后各加入1.0ml邻二氮菲溶液,2.5ml醋酸钠溶液,用蒸馏水稀释至刻度线摇匀,用2cm吸收池,试剂空白为参比,在440——540nm间,每隔10nm测量一次吸光度,以波长为横坐标,吸光度为纵坐标,确定最大吸收波长
(1)
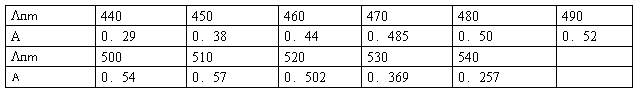
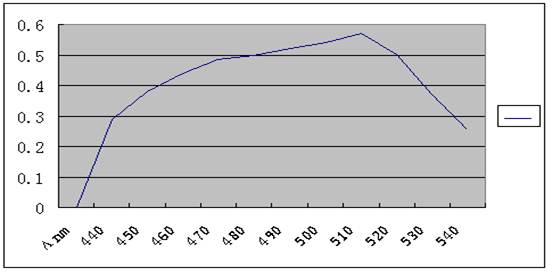
4.工作曲线的绘制
取50ml的容量瓶7个,各加入100.00µɡ ml-1铁标准0.00,0.20,0.40,0.60,0.80,1.00,1.20ml,然后分别加入0.5ml邻二氮菲溶液,2.5ml醋酸钠溶液,用蒸馏水稀释至刻度线摇匀,用2cm吸收池,以试剂空白为参比溶液,在选定波长下测定并记录各溶液光度,记当格式参考下表:
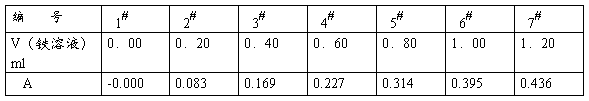
5.铁含量的测定
取1支洁净的50ml容量瓶,加人2.5ml含铁未知试液,按步骤(6 )显色,测量吸光度
并记录.

K=268.1 B= -2.205 R*R=0.9945
CONC. =K *ABS+B
C = 44.55mol ml-1
6.结束工作
测量完毕,关闭电源插头,取出吸收池, 清洗晾干后人盆保存.清理工作台,罩上一
仪器防尘罩,填写仪器使用记录.清洗容量瓶和其他所用的玻璃仪器并放回原处.
五、讨论:
(1) 在选择波长时,在440nm——450nm间每隔10nm 测量一次吸光度,最后得出的λmix=510nm,可能出在试剂未摇匀,提供的λmix=508nm,如果再缩减一点进程,试齐充分摇匀,静置时间充分,结果会更理想一些。
(2) 在测定溶液吸光度时,测出了两个9,实验结果不太理想,可能是在配制溶液过程中的原因:a、配制好的溶液静置的未达到15min;b、药剂方面的问题是否在期限内使用(未知)因从溶液显色的效果看,颜色有点淡,要求在试剂的使用期限内使用;c、移取试剂时操作的标准度是否符合要求,要求一个人移取试剂。(张丽辉)
在配制试样时不是一双手自始至终,因而所观察到的结果因人而异,导致最终结果偏差较大,另外还有实验时的温度,也是造成结果偏差的原因。(崔凤琼)
本次实验阶段由于多人操作,因而致使最终结果不精确。(普杰飞)
(1) 在操作中,我觉得应该一人操作这样才能减少误差。
(2) 在使用分光计时,使用同一标样,测同一溶液但就会得出不同的值。这可能有几个原因:a、温度,b、长时间使用机器,使得性能降低,所以商量得不同值。(李国跃)
在实验的进行当中,因为加试样的量都有精确的规定,但是在操作中由于是手动操作所以会有微小的误码率差量,但综合了所有误差量将成为一个大的误差,这将导致整个实验的结果会产生较大的误码率差。(赵宇)
在配制溶液时,加入拭目以待试剂顺序不能颠倒,特别加显色剂时,以防产生反应后影响操作结果。(刘金旖)
六、结论:
(1) 溶液显色,是由于溶液对不同波长的光的选择的结果,为了使测定的结果有较好的灵敏度和准确度,必须选择合适的测量条件,如:入射波长,溶液酸度,度剂使用期限 。
(2) 吸收波长与溶液浓度无关,不同浓度的溶液吸收都很强烈,吸收程度随浓度的增加而增加,成正比关系,从而可以根据该部分波长的光的吸收的程度来测定溶液的浓度。
(3) 此次试验结果虽不太理想,但让我深有感触,从中找到自己的不足,并且懂得不少试验操作方面的知识。从无知到有知,从不熟练到熟练使用使自己得到了很大的提高。(张丽辉)
附录:
723型操作步骤
1、 插上插座,按后面开关开机
2、 机器自检吸光度和波长,至显示500。
3、 按AλCOTO键,输入测定波长数值按回车键。
4、 将考比溶液(空白溶液)比色皿置于R位以消除仪器配对误码率差,拉动试样架拉杆,按ABS。01键从R、S1、S2、S3,逐一消除然后再检查1~~2次看是否显示0。000否则重新开始。
5、 按T/ARAN按3键,回车,再按1键,回车。
6、 逐一输入标准溶液的浓度值,每输一个按回车,全部输完,再按回车。
7、 固定考比溶液比色皿(第一格为参比溶液)其余三格放标准试样溶液,每测一值,拉杆拉一格,按START/STOP全打印完,按回车
8、 机器会自动打印出标准曲线K、B值以及相关系R。
9、 固定参比溶液比色皿,其余三格放入待测水样,逐一测定。
10完毕后,取出比色皿,从打印机上撕下数据,清扫仪器及台面关机。
721型分光度计操作步骤
1、 开机。
2、 定波长入=700。
3、 打开盖子调零。
4、 关上盖子,调满刻度至100。
5、 参比溶液比色皿放入其中,均合100调满。
6、 第一格不动,二,三,四格换上标液(共计七个点)调换标液时先用蒸馏水清洗后,再用待测液(标液)清洗,再测其分光度(浓度)
第二篇:邻二氮菲分光光度法测定微量铁实验报告
XXXX大学--------------------实验报告 年级:2010级 系:XX医学 班:1班 组:1组 姓名:XXX xxxxxxxxxx
实验一 邻二氮菲分光光度法测定微量铁
实验目的和要求
1.掌握紫外可见分光光度计的基本操作;
2.掌握邻二氮菲分光光度法测定微量铁的原理和方法;
3.掌握吸收曲线绘制及最大吸收波长选择;
4.掌握标准曲线绘制及应用。
实验原理
邻二氮菲(1,10—邻二氮杂菲)是一种有机配位剂,可与Fe2+形成红色配位离子:
2+
Fe2++3
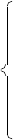
Fe
3
在pH=3~9范围内,该反应能够迅速完成,生成的红色配位离子在510nm波长附近有一吸收峰,摩尔吸收系数为1.1×10-4,反应十分灵敏,Fe2+ 浓度与吸光度符合光吸收定律,适合于微量铁的测定。
实验中,老师我们又见面了采用pH=4.5~5的缓冲溶液保持标准系列溶液及样品溶液的酸度;采用盐酸羟胺还原标准储备液及样品溶液中的Fe3+并防止测定过程中Fe2+被空气氧化。 实验仪器与试剂
1.752S型分光光度计
-32.标准铁储备溶液(1.00×10mol/L)
3.邻二氮菲溶液(0.15%,新鲜配制)
4.盐酸羟胺溶液(10%,新鲜配制)
5.NaAC缓冲溶液
6.50ml容量瓶7个
7.1cm玻璃比色皿2个
8.铁样品溶液
实验步骤
1.标准系列溶液及样品溶液配制,按照下表配制铁标准系列溶液及样品溶液。 教师签名: 日期:2012-13-32
XXXX大学--------------------实验报告
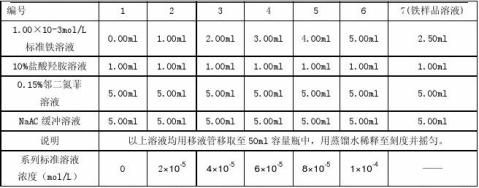
2.吸收曲线绘制 用1cm比色皿,以1号溶液作为参比溶液,测定4号溶液在各个波长处的吸光度,绘制吸收曲线,并找出最大吸收波长。
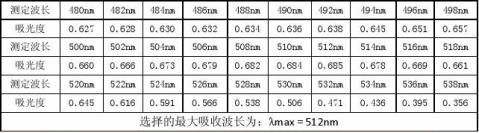
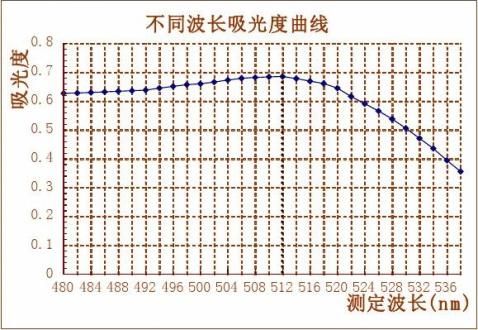
3.标准曲线制作
教师签名: 日期:2012-13-32
XXXX大学--------------------实验报告
年级:2010级 系:XX医学 班:1班 组:1组 姓名:XXX xxxxxxxxxx
在选定最大吸收波长处,用1cm比色皿,以1号溶液作为参比溶液,分别测定2至7号溶液的吸光度,平行测定3次,计算吸光度平均值,绘制标准曲线。

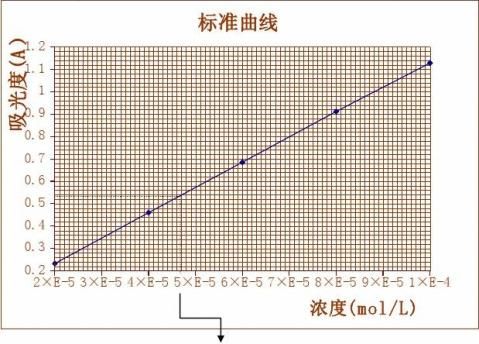
实验数据处理
1、 样品中铁的计算
7 样品溶液
4.65×10-5 mol/ml
CX?C读取值?
-5
50.00
2.50
-4
Cx=4.65×10×50.00/2.50=9.30×10 mol/L
2、 摩尔吸光系数计算
在标准曲线的直线部分选择量两点,读取对应的坐标值,计算邻二氮菲配位物在最大吸收波长出的摩尔吸光系数:
ε?
A2?A1
c2-c1
-5
ε=(0.460-0.233)/(0.00006-0.00004)=2.00×10
教师签名: 日期:2012-13-32
XXXX大学--------------------实验报告 年级:2010级 系:XX医学 班:1班 组:1组 姓名:XXX xxxxxxxxxx 实验注意事项
1、测定系列标准溶液和样品溶液时,必须使用同一只比色皿。
2、比色皿放入分光光度计样品室前,必须使用吸水纸将外表面擦拭干净。
3、比色皿在换装不同浓度溶液时,必须使用待测溶液润洗至少三次。
4、在比色皿未放入分光光度计测定光路时,必须将样品室舱打开。
讨论及思考
1.如果绘制你的标准曲线线性不好或者标准曲线有部分发生偏离,请分析原因。 答:标准曲线部分偏离的原因可能是:
(1)我感觉的数据如果有问题主要是感觉分光光度计不够精确,使用旋钮每次旋出相同的测定数值可能都不一样,有时小范围内甚至可能发生往大旋,波长数值反而变小的情况;
(2)也可能是装溶液时没有进行润洗,影响溶液的浓度。
2.计算的红色配位物摩尔吸光系数与文献是否一致?影响因素有哪些? 答: 一致。
3.如果各个测定溶液的酸度值不同,会给实验结果带来怎么样的影响? 答:
教师签名: 日期:2012-13-32
-
综合实验报告 邻二氮菲分光光度法测定微量铁
邻二氮菲分光光度法测定微量铁一实验目的学习确定实验条件的方法掌握邻二氮菲分光光度法测定微量铁的方法原理掌握721型分光光度计的使用…
-
邻二氮菲分光光度法测定微量铁实验报告
邻二氮菲分光光度法测定微量铁课程名称仪器分析指导教师李志红实验员张丽辉李国跃崔凤琼刘金旖普杰飞赵宇时间20xx年5月12日一实验目…
-
邻二氮菲分光光度法测定微量铁实验报告
实验一邻二氮菲分光光度法测定微量铁20xx级医学检验3组吴茳铃20xx221885实验目的和要求1掌握紫外可见分光光度计的基本操作…
-
邻二氮菲分光光度法测定微量铁实验报告
实验一邻二氮菲分光光度法测定微量铁一实验目的和要求1掌握紫外可见分光光度计的基本操作2掌握邻二氮菲分光光度法测定微量铁的原理和方法…
-
邻二氮菲分光光度法测定微量铁实验报告
实验一邻二氮菲分光光度法测定微量铁实验目的和要求1掌握紫外可见分光光度计的基本操作2掌握邻二氮菲分光光度法测定微量铁的原理和方法3…
-
综合实验报告 邻二氮菲分光光度法测定微量铁
邻二氮菲分光光度法测定微量铁一实验目的学习确定实验条件的方法掌握邻二氮菲分光光度法测定微量铁的方法原理掌握721型分光光度计的使用…
-
邻二氮菲分光光度法测定微量铁实验报告
实验一邻二氮菲分光光度法测定微量铁实验目的和要求1掌握紫外可见分光光度计的基本操作2掌握邻二氮菲分光光度法测定微量铁的原理和方法3…
-
邻二氮菲分光光度法测定微量铁
邻二氮菲分光光度法测定微量铁一实验目的1学习确定实验条件的方法掌握邻二氮菲分光光度法测定微量铁的方法原理2掌握TU19xx分光光度…
-
邻二氮菲分光光度法测定水中微量铁
邻二氮菲分光光度法测定微量铁一实验目的1学会吸收曲线及标准曲线的绘制了解分光光度法的基本原理2掌握用邻二氮菲分光光度法测定微量铁的…
-
邻二氮杂菲分光光度法测定铁 实验报告
分析化学实验报告实验题目邻二氮杂菲分光光度法测定铁学院专业食品科学与工程班级姓名学号同组者姓名一实验目的1了解分光光度法测定物质含…
-
邻二氮菲分光光度法测定微量铁实验报告
邻二氮菲分光光度法测定微量铁日期20xx318实验者曾惜20xx222702合作者曾子夜20xx222702一实验目的和要求1掌握…