紫外-可见分光光度计的检测实验报告
分子光谱实训报告

班 级: ————
学 号:
姓 名:
指导教师:
20##年10月
紫外-可见分光光度计的检测
实训日期______年_____月_____日 教师评定:______________
【仪器概况】
仪器名称:紫外-可见分光光度计
型号:UV1801
厂家:北京瑞利分析仪器公司
编号:090953
 二、【仪器结构】
二、【仪器结构】
三、【实验项目】
波长准确度检查
仪器零点稳定性检查
光电流稳定度检查
吸光度准确度检查
紫外区透色比检查
杂散光合格性检查
吸收池配套性检查
皿差
四、【仪器及试剂准备单】
1、试剂清单(以1个小组6人为例)
H2SO3、K2Cr3O7、HClO4、碘化钠、蒸馏水、亚硝酸钠、无水乙醇、苯、硫酸铜。
2、仪器清单(以1个小组6人为例)
UV1801紫外分光光度计、烧杯14个、容量瓶9个、玻璃棒、滤纸、洗瓶、镨钕滤光片、比色皿、胶头滴管、洗耳球、移液管、表面皿、移液管架。
五、【检测步骤】
开机自检(5个ok)
(一)、波长准确度
可见分光光度(空气)
1、按1、波长扫描;按F1,参数设置(E、波长范围460--680nm、间隔0.1nm、换灯点800nm)按返回键。
2、按F2,根据显示屏提醒,确定键;出现两个峰,分别记录两个峰值的波长和吸光值。(重复3次;参比和样品都是空气)。
镨钕滤光片
1、按F1,参数设置(A、波长范围500--540nm、间隔1nm、换灯点360nm)按返回键。
2、把镨钕滤光片放在第二格,关盖;按F2,根据显示屏提醒,拉入参比,确定键;再拉入样品,确定键;出现一个峰,记录读数。
紫外分光光度
1、按F1,参数设置(A、波长范围200--270nm、间隔0.1nm、换灯点360nm)按返回键。
2、加3滴苯在石英比色皿中,盖上比色皿盖,放在第二格,关盖;按F2,根据显示屏提醒,拉入参比,确定键;再拉入样品,确定键;出现五指峰,分别记录五个不同峰的波长和吸光值。
(二)、透射比的准确度
将参比溶液0.001mol/L高氯酸加入石英比色皿3/4处(润洗3次)放在第一格;将测定液重铬酸钾加入石英比色皿3/4处(润洗3次)放在第二格;调节测量方式T;返回主页面,按2,光度测量;按F1,参数设置(换灯点360nm、波长数4个,入分别调到235nm、257nm、313nm、350nm);按F2,根据显示屏提醒,拉入参比,确定键;再拉入样品,确定键;记录读数。
(三)、吸光度准确度
可见分光光度
将参比溶液1:100硫酸加入石英比色皿3/4处(润洗3次)放在第一格;将测定液硫酸铜加入石英比色皿3/4处(润洗3次)放在第二格;调节测量方式A;返回主页面,按2,光度测量;按F1,参数设置(换灯点360nm、波长数3个,入分别调到650nm、700nm、750nm)按F2,根据显示屏提醒,拉入参比,确定键;再拉入样品,确定键;记录读数。
紫外分光光度
将参比溶液硫酸加入石英比色皿3/4处(润洗3次)放在第一格;将测定液重铬酸钾加入石英比色皿3/4处(润洗3次)放在第二格;调节测量方式A;返回主页面,按2,光度测量;按F1,参数设置(换灯点360nm、波长数4个,入分别调到235nm、257nm、313nm、350nm);按F2,根据显示屏提醒,拉入参比,确定键;再拉入样品,确定键;记录读数。
(四)、杂散光
1、将参比溶液蒸馏水加入石英比色皿3/4处(润洗3次),样品亚硝酸钠加入石英比色皿3/4处(润洗3次)调节测量方式T,返回主页面,按2,光度测量;按F1,参数设置(换灯点360nm、波长数1个,入调成380nm)按F2,根据显示屏提醒,拉入参比,确定键;再拉入样品,确定键;记录读数。
2、将参比溶液蒸馏水加入石英比色皿3/4处(润洗3次),样品碘化钠加入石英比色皿3/4处(润洗3次)调节测量方式T,返回主页面,按2,光度测量;按F1,参数设置(换灯点360nm、波长数1个,入调成220nm);按F2,根据显示屏提醒,拉入参比,确定键;再拉入样品,确定键;记录读数。
(五)、UV1801.零点稳定性的检查
测量方式 A 取样间隔 1nm
波长范围 200nm一780nm A的范围 一0.1一0.1
换灯点 360nm 若所测得的|A|≤0.002为合格
(六)、光电流稳定性
比色皿较正 关 波长数 2
入/nm 370 790 时间:0一3min
若T%在99.9一100.1%之间为合格
(七)、皿差
将上述的T数据从大到小排列(最大的放在第一格);调T0和100,调到A,拉杆一次,记录读数(4个读数)。
六、【数据记录及处理】
1、波长准确度检查
⑴紫外区(苯蒸气)
参数设置
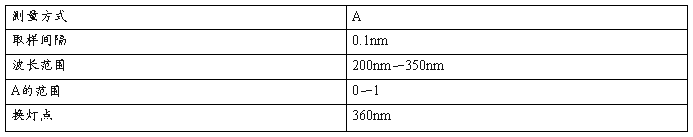
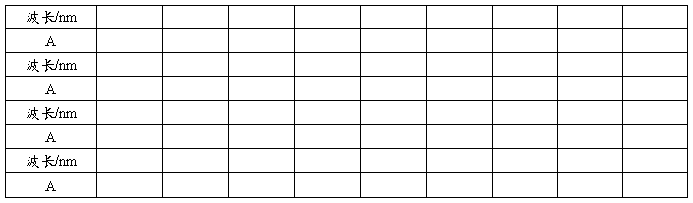
结论:
⑵可见区(镨钕滤光片)△入=|入max一529nm|<3nm为合格
参数设置
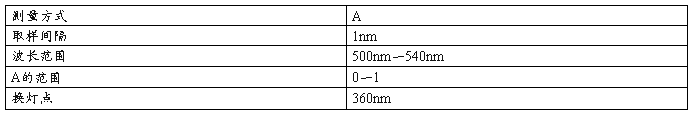
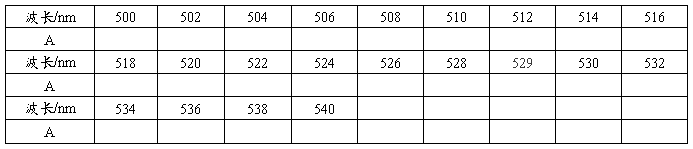
结论:
⑶可见区(空气)
参数设置
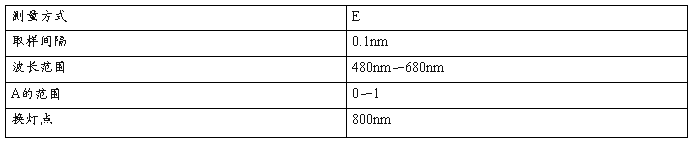
在标准波长入1=486.0nm和入2=656.1nm附近分别寻找峰值最大时所对应的的两个波长,|△入|=|入标一入测1|<0.5nm为合格,|△入|=|入标一入测2|<0.5nm为合格。
重现性:△入=|入测max一入测min|<0.2nm为合格(连测三次)
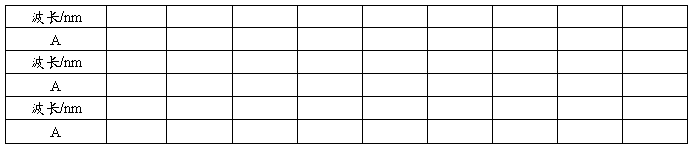
结论:
2、仪器零点稳定性检查
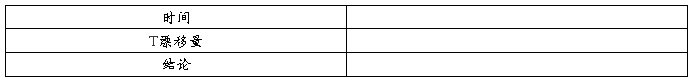
3、光电流稳定度检查

4、吸光度准确度检查
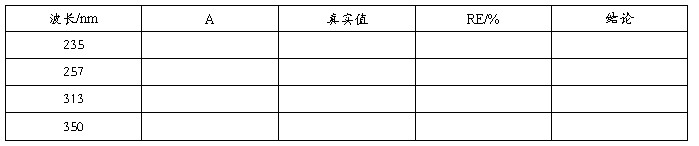
⑴紫外区
⑵可见区(以1:100H2SO4溶液做参比,测2%硫酸铜溶液的吸光度)
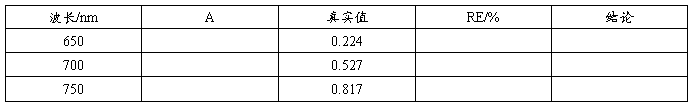
5、紫外区透射比的准确度的检验
以0.001mol/LHCIO4溶液做参比,测0.006000%K2Cr2O7溶液,其差值应在0.8%一2.5%内为合格。
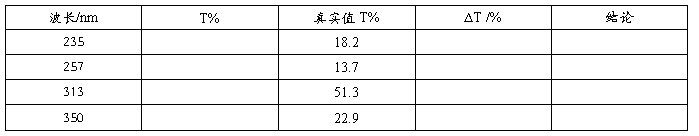
6、杂散光合格性检查
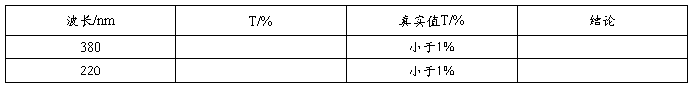
7、吸收池的配套性检查 波长/nm:220
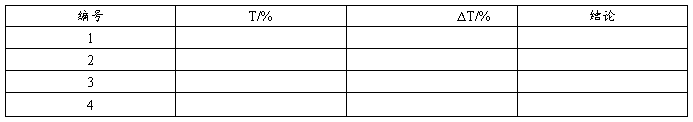
8、皿差 波长/nm:220

七、【结果讨论与实训心得】
第二篇:紫外可见分光光度计的应用
紫外可见分光光度法
摘要 本文介绍了紫外可见分光光度法的发展、原理、特点及应用,并列举多项实例说紫外可见分光光度法在各个领域中的应用。
关键词 有机分析 吸收光谱 紫外可见分光光度法
1.发展
人们在实践中早已总结出不同颜色的物质具有不同的物理和化学性质。根据物质的这些特性可对它进行有效的分析和判别。由于颜色本就惹人注意,根据物质的颜色深浅程度来对物质的含量进行估计,可追溯到古代及中世纪。1852年,比尔(Beer)参考了布给尔(Bouguer)1729年和朗伯(Lambert)在1760年所发表的文章,提出了分光光度的基本定律,即液层厚度相等时,颜色的强度与呈色溶液的浓度成比例,从而奠定了分光光度法的理论基础,这就是著名的比尔朗伯定律。1854年,杜包斯克(Duboscq)和奈斯勒(Nessler)等人将此理论应用于定量分析化学领域,并且设计了第一台比色计。到19xx年,美国国家标准局制成了第一台紫外可见分光光度计。此后,紫外可见分光光度计经不断改进,又出现自动记录、自动打印、数字显示、微机控制等各种类型的仪器,使光度法的灵敏度和准确度也不断提高,其应用范围也不断扩大。
紫外可见分光光度法从问世以来,在应用方面有了很大的发展,尤其是在相关学科发展的基础上,促使分光光度计仪器的不断创新,功能更加齐全,使得光度法的应用更拓宽了范围。目前,分光光度法已为工农业各个部门和科学研究的各个领域所广泛采用,成为人们从事生产和科研的有力测试手段。我国在分析化学领域有着坚实的基础,在分光光度分析方法和仪器的制造方面国际上都已达到一定的水平。
2.原理
物质的吸收光谱本质上就是物质中的分子和原子吸收了入射光中的某些特定波长的光能量,相应地发生了分子振动能级跃迁和电子能级跃迁的结果。由于各种物质具有各自不同的分子、原子和不同的分子空间结构,其吸收光能量的情况也就不会相同,因此,每种物质就有其特有的、固定的吸收光谱曲线,可根据吸收光谱上的某些特征波长处的吸光度的高低判别或测定该物质的含量,这就是分光光度定性和定量分析的基础。分光光度分析就是根据物质的吸收光谱研究物质的成分、结构和物质间相互作用的有效手段。
紫外可见分光光度法的定量分析基础是朗伯-比尔(Lambert-Beer)定律。即物质在一定浓度的吸光度与它的吸收介质的厚度呈正比。
物质的颜色和它的电子结构有密切的关系,当辐射(光子)引起电子跃迁使分子(或离子)从基态上升到激发态时,分子(或离子)就会在可见区或紫外呈现吸光,
颜色的发生或变化是和分子的正常电子结构的变形联系的。当分子中含有一个或更多的生色基因(即具有不饱和键的原子基团),辐射就会引起分子中电子能量的改变。常见的生色团有:
CO, -N=N-, -N=O,-C N,CS
如果两个生色团之间隔一个碳原子,则形成共轭基团,会使吸收带移向较长的波长处(即红移),且吸收带的强度显著增加。当分子中含有助色基团(有未共用电子对的基团)时,也会产生红移效应。常见的助色基团有:-OH -NH2, -SH, -Cl, -Br, -I。
3.特点
分光光度法对于分析人员来说,可以说是最有用的工具之一。几乎每一个分析实验室都离不开紫外可见分光光度计。分光光度法的主要特点为:
(1)应用广泛
由于各种各样的无机物和有机物在紫外可见区都有吸收,因此均可借此法加以测定。到目前为止,几乎化学元素周期表上的所有元素(除少数放射性元素和惰性元素之外)均可采用此法 。在国际上发表的有关分析的论文总数中,光度法约占28%,我国约占所发表论文总数的33% 。
(2)灵敏度高
由于新的显色剂的大量合成,并在应用研究方面取得了可喜的进展,使得对元素测定的灵敏度有所推进,特别是有关多元络合物和各种表面活性剂的应用研究,使许多元素的摩尔吸光系数由原来的几万提高到数十万。
(3)选择性好
目前已有些元素只要利用控制适当的显色条件就可直接进行光度法测定,如钴、铀、镍、铜、银、铁等元素的测定,已有比较满意的方法了。
(4)准确度高
对于一般的分光光度法,其浓度测量的相对误差在1~3%范围内,如采用示差分光光度法进行测量,则误差可减少到更低。
(5) 适用浓度范围广
可从常量(1%~50%)(尤其使用示差法)到痕量(10-8~10-6%)(经预富集后)。
(6) 分析成本低、操作简便、快速
由于分光光度法具有以上优点,因此目前仍广泛地应用于化工、冶金、地质、医学、食品、制药等部门及环境监测系统。单在水质分析中的应用就很广,目前能有直接法和间接法测定的金属和非金属元素就有70多种。
4.应用
4.1 检定物质
根据吸收光谱图上的一些特征吸收,特别是最大吸收波长和摩尔吸收系数是检定物质的常用物理参数。这在药物分析上就有着很广泛的应用。在国内外的药典中,已将众多的药物紫外吸收光谱的最大吸收波长和摩尔吸收系数载入其中,为药物分析提供了很好的手段。
4.2 与标准物及标准图谱对照
将分析样品和标准样品以相同浓度配制在同一溶剂中,在同一条件下分别测定紫外可见吸收光谱。若两者是同一物质,则两者的光谱图应完全一致。如果没有标样,也可以和现成的标准谱图对照进行比较。这种方法要求仪器准确,精密度高,且测定条件要相同。
4.3 比较最大吸收波长吸收系数的一致性
由于紫外吸收光谱只含有2~3个较宽的吸收带,而紫外光谱主要是分子内的发色团在紫外区产生的吸收,与分子和其它部分关系不大。具有相同发色团的不同分子结构,在较大分子中不影响发色团的紫外吸收光谱,不同的分子结构有可能有相同的紫外吸收光谱,但它们的吸收系数是有差别的。如果分析样品和标准样品的吸收波长相同,吸收系数也相同,则可认为分析样品与标准样品为同一物质。
4.4 纯度检验
例1 紫外吸收光谱能测定化合物中含有微量的具有紫外吸收的杂质。如果化合物的紫外可见光区没有明显的吸收峰,而它的杂质在紫外区内有较强的吸收峰,就可以检测出化合物中的杂质。
例2 检测乙醇样品含有的苯的杂质。苯的最大吸收波长在256nm,而乙醇在此波长处没有吸收。在紫外吸收光谱上就能很明显地看出来。
如果化合物在紫外可见有吸收,可用吸收系数检测其纯度。
例3 还可以用差示法来检测样品的纯度。取相同浓度的纯品在同一溶剂中测定作空白对照 ,样品与纯品之间的差示光谱就是样品中含有杂质的光谱。
4.5 推测化合物的分子结构
(1) 推测化合物的共轭体系和部分骨架
如果一个化合物在紫外区是透明的,没有吸收峰,则说明不存在共轭体系 (指不存在多个相间双键)。它可能是脂肪族碳氢化合物、胺、腈、醇等不含双键或环状结构的化合物。
如果在210-250nm有强吸收,则可能有两个双键共轭系统(如共轭二烯或幔-不饱和酮)。
如果在250-300nm有强吸收,则可能具有3-5个不饱和共轭系统。
如果在260-300nm有中强吸收(吸收系数=200-1000),则可能有苯环。
如果在250-300nm有弱吸收,则可能存在羰基基团
(2) 区分化合物的构型和构象
例4 化合物二苯乙烯有顺式和反式两种构型,它们的最大吸收波长和吸收强度都不同,由于反式构型没有空间障碍,偶极矩大,而顺式构型有空间障碍,因此反式的吸收波长和强度都比顺式的来得大。为此就很容易区分顺式和反式构型了。
(3)互变异构体的鉴别。
在有机化学中,会有异构体的互变现象,通过紫外光谱也可鉴别。
4.6 氢键强度的测定
实验证明,不同的极性溶剂产生氢键的强度也不同,这可以利用紫外光谱来判断化合物在不同溶剂中氢键强度,以确定选择哪一种溶剂 。
4.7 络合物组成及稳定常数的测定
金属离子常与有机物形成络合物,多数络合物在紫外可见区是有吸收的,我们可以利用分光光度法来研究其组成。
4.8 反应动力学研究
借助于分光光度法可以得出一些化学反应速度常数,并从两个或两个以上温度条件下得到的速度数据,得出反应活化能。在丙酮的溴化反应的动力学研究中就是一个成功的例子。
4.9 在有机分析中的应用
有机分析是一门研究有机化合物的分离、鉴别及组成结构测定的科学,它是在有机化学和分析化学的基础上发展起来的综合性学科。在国民经济的许多领域都用有机分析。
波长在190-800nm的电磁光谱对于判断有机分子中是否存在共轭体系、芳环结构及C=C、C=O 、N=N之类的发色团是一个很好的手段,具有强烈的吸收,其摩尔吸光系数可达104-105(而红外吸收光谱的摩尔吸光系数一般均小于103),因而检测灵敏度很高。对于一些特列类型的结构,可通过简单的数学运算确定最大吸收。如果发色团之间不以共轭键相连的话,其紫外吸收具有可加性,即总的吸收等于各单独发色团的吸收之和。用此性质曾成功地推导出利血平及氯霉素的部分结构。一个复杂分子的结构,往往可以由比较化合物的紫外光谱性质而推断其含有何种发色团,有时还能提供一些立体结构及分子量的一些信息,为未知物的剖析提供有用的线索。以下通过实例说明分光光度法在有机分析中的应用。
例5 氯霉素分子中的硝基首先是由它的紫外光谱而确定的,在紫外光谱中298nm和278nm处出现芳香硝基的特征吸收。
例6 五圆环酮和羧酸酯的红外特征吸收都在1740cm-1附近,难以区别。但在紫外光谱中只有前者在210nm以上有吸收,从而得以区别。
利用紫外分光光度法进行定量分析时,可将待测试样的纯品配制成一系列标准溶液,事先绘制标准曲线,由待测未知样品吸光度对照标准曲线,就可得到其含量。当未知物样品为几种组分,且这组分的最大吸收峰值互不重叠,则可用联立方程解之。
结语 紫外可见分光光度法仪器价格低廉适用性广泛,尤其是采用微机控制以来,该技术得到了突飞猛进的发展。近年来我国仪器制造厂可以生产出与国外等同水平的紫外分光光度计,成为分析者的最佳选择。
-
分光光度计实验报告
实验六分光光度法测溴酚蓝的电离平衡常数王思雨PB1220xx07中国科学技术大学生命科学院摘要本实验中我们通过使用722型分光光度…
-
分析化学实验报告(分光光度法)(2)
广西师范学院化学系化学实验报告册课程名称分析化学实验班级高分班学号姓名组别20xx年至20xx年第一学年第二学期广西师范学院化学实…
-
紫外分光光度计实验报告
UV2550紫外分光光度计的使用和分光光度法测定对苯二酚姓名XXX专业有机化学学号3120xx303004时间20xx10211目…
-
紫外可见分光光度计实验报告
实验报告一实验题目浓度为01的TiO2水悬浮液的光谱分析二实验日期三实验人员四实验目的本实验目的是掌握TiO2的光学特性特别是在紫…
-
邻二氮菲分光光度法测定微量铁实验报告
邻二氮菲分光光度法测定微量铁课程名称仪器分析指导教师李志红实验员张丽辉李国跃崔凤琼刘金旖普杰飞赵宇时间20xx年5月12日一实验目…
-
分光计的调节与使用实验报告
分光计的调节与使用实验报告实验名称分光计的调节与使用姓名学号班级实验日期20xx1219温度2同组者无一实验目的1掌握分光计的调整…
-
分光光度计实验报告
实验六分光光度法测溴酚蓝的电离平衡常数王思雨PB1220xx07中国科学技术大学生命科学院摘要本实验中我们通过使用722型分光光度…
-
紫外分光光度计实验报告
UV2550紫外分光光度计的使用和分光光度法测定对苯二酚姓名XXX专业有机化学学号3120xx303004时间20xx10211目…
-
分析化学实验报告(分光光度法)(2)
广西师范学院化学系化学实验报告册课程名称分析化学实验班级高分班学号姓名组别20xx年至20xx年第一学年第二学期广西师范学院化学实…
-
紫外可见分光光度计实验报告
实验报告一实验题目浓度为01的TiO2水悬浮液的光谱分析二实验日期三实验人员四实验目的本实验目的是掌握TiO2的光学特性特别是在紫…
-
光谱分析实验报告
仪器分析实验光谱分析实验一光谱分析食质检测20xx级02班钟凯成学号20xx5782一实验目的1了解主要光学仪器AASAFSV2S…