实验1、紫外可见光谱实验报告
一、实验目的
1、 学会使用UV-2550型紫外-可见光分光光度计。
2、 掌握紫外—可见分光光度计的定量分析方法。
3、 学会利用紫外可见光谱技术进行有机化合物特征和定量分析的方法。
二、实验原理
基于物质对200-800nm光谱区辐射的吸收特性建立起来的分析测定方法称为紫外—可见吸收光谱法或紫外—可见分光光度法。紫外—可见吸收光谱是由分子外层电子能级跃迁产生,同时伴随着分子的振动能级和转动能级的跃迁,因此吸收光谱具有带宽。紫外—可见吸收光谱的定量分析采用朗伯-比尔定律,被测物质的紫外吸收的峰强与其浓度成正比,即:
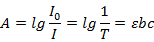
其中A是吸光度,I、I0分别为透过样品后光的强度和测试光的强度,ε为摩尔吸光系数,b为样品厚度,c为浓度。
紫外吸收光谱是由于分子中的电子跃迁产生的。按分子轨道理论,在有机化合物分子中这种吸收光谱取决于分子中成键电子的种类、电子分布情况,根据其性质不同可分为3种电子:(1)形成单键的σ电子 ;(2)形成不饱和键的π电子 ;(3)氧、氮、硫、卤素等杂原子上的未成键的n电子 。

图1. 基团中的σ,π,n成键电子
当它们吸收一定能量ΔE后,将跃迁到较高的能级,占据反键轨道。分子内部结构与这种特定的跃迁是有着密切关系的,使得分子轨道分为成键σ轨道、反键σ*轨道、成键π轨道、反键 π* 轨道和n轨道,其能量由低到高的顺序为:σ<π<n<π*<σ*。
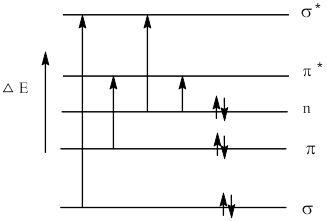
图2.分子轨道中的能量跃迁示意图
仪器原理是光源发出光谱,经单色器分光,然后单色光通过样品池,达到检测器,把光信号转变成电信号,再经过信号放大、模/数转换,数据传输给计算机,由计算机软件处理。
三、仪器与溶液准备
1、 UV-2550型紫外—可见分光光度计
2、 1cm石英比色皿一套
3、 UVprobe电脑软件
4、 配置好的10μg/mL、15μg/mL、20μg/mL以及未知浓度的甲基紫溶液,甲基红溶液
5、 仪器的基本构成:
紫外可见分光光度计的基本结构如下:
 光源→单色器→吸收池→检测器→信息处理与显示系统
光源→单色器→吸收池→检测器→信息处理与显示系统

四、实验步骤
1、打开电源,开启紫外—可见分光光度计上的开关,打开电脑上的UVprobe软件,让其自检,约5min后,对仪器相关参数设置。设置波长范围为400-200nm,高速检测,间隔为0.5nm。
2、空白对比实验。取一定量的蒸馏水装进1cm石英比色皿至2/3,在Win-UV 主显示窗口下,单击所选图标“基线”以扫描蒸馏水的测定吸收曲线。
3、取一定浓度的的水杨酸溶液,装进石英比色皿中放到紫外—可见分光光度计中,获得波长-吸收曲线,读取最大吸收的波长数据和吸光度。得到其标准图谱。
4、同样的方法测定一定浓度的水杨醛溶液,获得波长-吸收曲线,读取最大吸收的波长数据和吸光度。得到其标准图谱。
5、同样的方法测定未知溶液,获得波长-吸收曲线,读取最大吸收的波长数据和吸光度。得到其图谱。
6、数据处理和分析。
7、结果与讨论。
五、实验数据处理
1.实验数据记录
将实验数据用excel作图可得到水杨酸和水杨醛的紫外可见分光波谱图,分别如图3和图4.

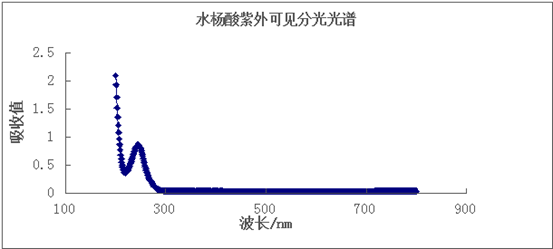
图3 实验1水杨酸的紫外可见分光波谱图
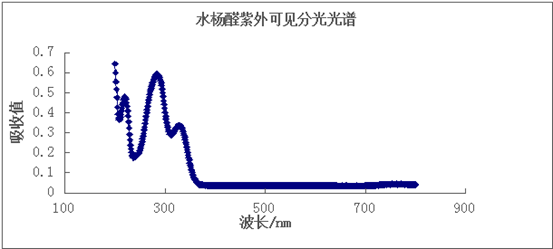
图4 实验2 水杨醛的紫外可见分光波谱图
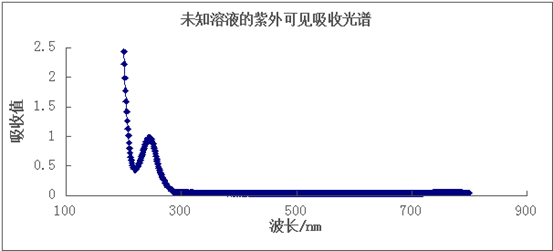
图5 实验3 未知溶液的紫外可见分光波谱图
2.实验数据处理
由实验3所得的可见分光波谱图可知,该溶液的最大吸收波长为245nm,对比图3、图4,该溶液为水杨酸溶液。,
将波长为580nm时不同浓度的甲基紫溶液的吸光度列出如表1。
表1,所测溶液最大吸光度数据
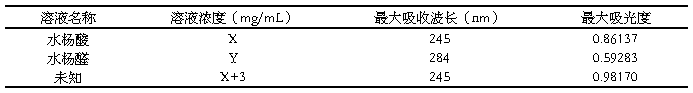
通过公式 Lamber-Beer(朗伯-比耳)定律:A=εbc可知,同一物质吸收值与浓度呈正比,又已知未知物质浓度比已知物质浓度大3.0mg/ml ,得:X/(X+3)=0.86137/0.98170
算得X=21.634mg/ml
六、分析与讨论
1、从实验结果中可得,所测的未知样品为水杨酸溶液,且其浓度为21.634mg/mL。
2、从水杨酸及水杨醛的结构中可看出,在λmax处的吸收峰为共轭体系的吸收,由于水杨醛的共轭体系较大,所以甲基紫的λmax比甲基红的λmax要大。
七、思考题
根据物质吸收曲线,思考如何利用紫外吸收光谱做定性分析?
答:紫外吸收光谱为有机化合物的定性分析提供了有用的信息。其方法是将未知试样和标准品以相同浓度配制在相同的溶剂中,在分别测绘吸收光谱,比较二者是否一致也可将未知试样的吸收光谱与标准图谱,如萨特勒紫外吸收光谱图相比较,如果吸收光谱完全相同,则一般可以认为两者是同一种化合物。但是,有机化合物在紫外区的吸收峰较少,有时会出现不同的结构,只要具有相同的生色团,它们的最大吸收波长lmax相同,然而其摩尔吸光系数e或比吸光系数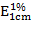 值是有差别的因此需利用lmax和lmax处的e或
值是有差别的因此需利用lmax和lmax处的e或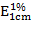 等数据作进一步比较。
等数据作进一步比较。
在没有紫外吸收光谱峰的物质中检查含高吸光系数的杂质是紫外吸收光谱的重要用途之一。如乙醇中杂质苯的检查,只需测定256 nm处有无苯的吸收峰即可。因为在这一波段,主成分乙醇无吸收峰。
在测绘比较用的紫外吸收光谱图时,应首先对仪器的波长准确性进行检查和校正。还必须采用相同的溶剂,以排除溶剂的极性对吸收光谱的影响。同时还应注意pH值、温度等因素的影响。在实际应用时,应注意溶剂的纯度。
但应注意紫外—可见吸收光谱对无机元素的定性分析应用较少。它主要适用于不饱和有机化合物,尤其是共轭体系的鉴定,以此推断未知物的骨架结构。在配合红外光谱、核磁共振谱、质谱等进行定性鉴定和结构分析中,是一个十分有用的辅助方法。
第二篇:紫外光谱实验报告
紫外-可见吸收光谱实验报告
一、实验目的
学习测定有机化合物或生物大分子的测定方法;掌握分光光度计的基本操作及数据处理方法。
二、实验内容
用双光路紫外分光光度计测量已知化合物在某未知浓度时的吸光度,同时,根据实验数据用origin做出紫外光谱图,并根据朗伯-比尔 (Lamber-Beer)定律,计算所测物质的浓度。
三、实验仪器及试剂:
UV2550紫外-可见分光光度仪;
本组所测溶剂为苯甲酸。
四、实验原理
根据朗伯-比耳 (Lamber-Beer)定律:A=εbc,通过紫外分光光度计测量出最大吸收峰A,而b与ε已知,故可求得苯甲酸的浓度。
五、实验结果与讨论
1、根据图一可知,苯甲酸在λ=226nm处有最大吸收峰,此时,A=0.77525;
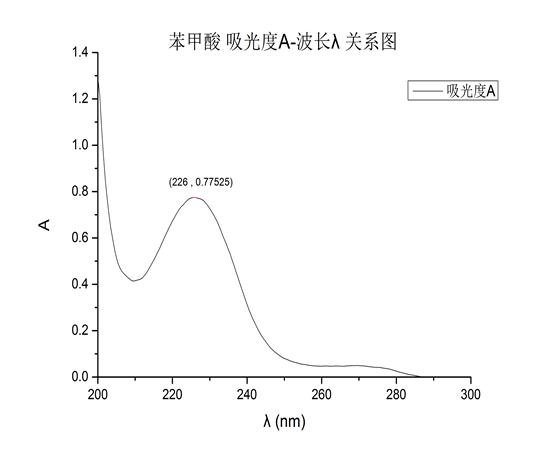
苯甲酸吸光度与波长关系图(图一)
2、苯甲酸在λ=226nm时的摩尔吸光系数ε=1000L/(mol·cm);
3、已知b=1cm,因此,根据据朗伯-比尔 (Lamber-Beer)定律,可求得苯甲酸的浓度c=7.75*10-4mol/L。
-
紫外吸收光谱实验报告
利用紫外吸收光谱检查物质纯度紫外-可见分光光度法测定水中苯酚含量一、实验目的1.学会使用Cary50型紫外-可见分光光度计2.掌握…
-
紫外光谱实验报告
紫外吸收光谱分析的应用实验报告班级环科10姓名王强学号20xx012127一实验目的1掌握紫外吸收光谱仪的使用方法2学会利用紫外光…
-
1紫外可见光谱实验报告
紫外可见光谱实验报告一、实验目的1、学会使用UV-2550型紫外-可见光分光光度计。2、掌握紫外可见分光光度计的定量分析方法。3、…
-
实验1紫外-可见吸收光谱实验报告
实验一紫外可见吸收光谱一实验目的1熟悉和掌握紫外可见吸收光谱的使用方法2用紫外可见吸收光谱测定某一位置样品浓度3定性判断和分析溶液…
-
实验1、紫外可见光谱实验报告
一实验目的1学会使用UV2550型紫外可见光分光光度计2掌握紫外可见分光光度计的定量分析方法3学会利用紫外可见光谱技术进行有机化合…
-
激光拉曼光谱实验报告---近代物理实验
激光拉曼光谱实验报告学号20xx11141054姓名牟蓉实验日期20xx328指导老师杨国建摘要本实验研究了用半导体激光器泵浦的N…
-
实验31 原子发射光谱观测分析(实验报告)
实验31A原子发射光谱观测分析实验目的1学会使用光学多通道分析器的方法2通过对钠原子光谱的研究了解碱金属原子光谱的一般规律3加深对…
-
圆二色光谱实验报告
圆二色光谱实验一实验目的1了解圆二色CD光谱的原理和使用方法2学会用圆二色光谱检测蛋白质二级构象的基本原理和方法并学会分析物质的手…
-
氢原子光谱实验报告
氢原子光谱摘要本实验用光栅光谱仪对氢原子光谱进行测量测得了氢原子光谱巴尔末线系的波长求出了里德伯常数最后对本实验进行了讨论关键词氢…
-
氢、氘光谱实验报告
实验一A氢氘光谱实验目的要求1测定氢原子与氘原子的巴耳末系发射光谱的波长和氢原子与氘原子的里德伯常数2了解WGD8A型组合式多功能…
-
光谱分析实验报告
仪器分析实验光谱分析实验一光谱分析食质检测20xx级02班钟凯成学号20xx5782一实验目的1了解主要光学仪器AASAFSV2S…