乙酸乙酯的制备
乙酸乙酯的制备
一、 实验目的
1. 掌握乙酸乙酯的制备原理及方法,掌握可逆反应提高产率的措施。 2. 掌握分馏的原理及分馏柱的作用。
3. 进一步练习并熟练掌握液体产品的纯化方法。
二、 实验原理
乙酸乙酯的合成方法很多,例如:可由乙酸或其衍生物与乙醇反应制取,也可由乙酸钠与卤乙烷反应来合成等。其中最常用的方法是在酸催化下由乙酸和乙醇直接酯化法。常用浓硫酸、氯化氢、对甲苯磺酸或强酸性阳离子交换树脂等作催化剂。若用浓硫酸作催化剂,其用量是醇的0.3%即可。其反应为:
CH3COOCH2CH3+H2O

主反应:CH3COOH+CH3CH2OH

3CH2OCH2CH3+H2O副反应:2CH3CH2CH3CH2OHCH2CH2+H2O
酯化反应为可逆反应,提高产率的措施为:一方面加入过量的乙醇,另一方面在反应过
程中不断蒸出生成的产物和水,促进平衡向生成酯的方向移动。但是,酯和水或乙醇的共沸物沸点与乙醇接近,为了能蒸出生成的酯和水,又尽量使乙醇少蒸出来,本实验采用了较长的分馏柱进行分馏。
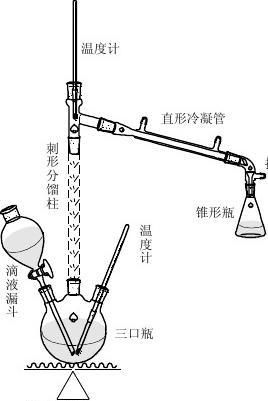
四、 实验装置图
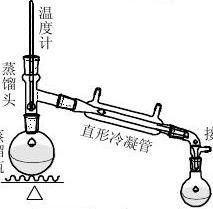

蒸馏装置
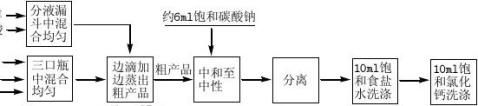
五、 实验流程图
10ml8ml4ml乙醇5ml浓硫酸2粒沸石
73-80℃ 的馏分,
六、 实验步骤
在100ml三颈瓶中,加入4ml乙醇,摇动下慢慢加入5ml浓硫酸,使其混合均匀,并加入几粒沸石。三颈瓶一侧口插入温度计,另一侧口插入滴液漏斗,漏斗末端应浸入液面以下,中间口安一长的刺形分馏柱(整个装置如上图)。
仪器装好后,在滴液漏斗内加入10ml乙醇和8ml冰醋酸,混合均匀,先向瓶内滴入约2ml的混合液,然后,将三颈瓶在石棉网上小火加热到110-120℃左右,这时蒸馏管口应有液体流出,再自滴液漏斗慢慢滴入其余的混合液,控制滴加速度和馏出速度大致相等,并维持反应温度在110-125℃之间,滴加完毕后,继续加热10分钟,直至温度升高到130℃不再有馏出液为止。
馏出液中含有乙酸乙酯及少量乙醇、乙醚、水和醋酸等,在摇动下,慢慢向粗产品中加
入饱和的碳酸钠溶液(约6ml)至无二氧化碳气体放出,酯层用PH试纸检验呈中性。移入分液漏斗中,充分振摇(注意及时放气!)后静置,分去下层水相。酯层用10ml饱和食盐水洗涤后,再每次用10ml饱和氯化钙溶液洗涤两次,弃去下层水相,酯层自漏斗上口倒入干燥的锥形瓶中,用无水碳酸钾干燥。
将干燥好的粗乙酸乙酯小心倾入60ml的梨形蒸馏瓶中(不要让干燥剂进入瓶中),加入沸石后在水浴上进行蒸馏,收集73-80℃的馏分。产品5-8g。
七、 操作要点及说明
1、本实验一方面加入过量乙醇,另一方面在反应过程中不断蒸出产物,促进平衡向生成酯的方向移动。乙酸乙酯和水、乙醇形成二元或三元共沸混合物,共沸点都比原料的沸点低,故可在反应过程中不断将其蒸出。这些共沸物的组成和沸点如下:
共沸物组成 共沸点
(1)乙酸乙酯91.9%,水8.1% 70.4℃
(2)乙酸乙酯69.0%,乙醇31.0% 71.8℃
(3)乙酸乙酯82.6%,乙醇8.4%,水9.0% 70.2℃
最低共沸物是三元共沸物,其共沸点为70.2℃,二元共沸物的共沸点为70.4℃和71.8℃,三者很接近。蒸出来的可能是二元组成和三元组成的混合物。加过量48%的乙醇,一方面使乙酸转化率提高,另一方面可使产物乙酸乙酯大部分蒸出或全部蒸出反应体系,进一步促进乙酸的转化,即在保证产物以共沸物蒸出时,反应瓶中,仍然是乙醇过量。
2、本实验的关键问题是控制酯化反应的温度和滴加速度。控制反应温度在120℃左右。温度过低,酯化反应不完全;温度过高(>140℃),易发生醇脱水和氧化等副反应:
2CH3CH23CH2OCH2CH3+H2O
CH3CH2OH33COOH
故要严格控制反应温度。
要正确控制滴加速度,滴加速度过快,会使大量乙醇来不及发生反应而被蒸出,同时也造成反应混合物温度下降,导致反应速度减慢,从而影响产率;滴加速度过慢,又会浪费时间,影响实验进程。
3、用饱和氯化钙溶液洗涤之前,要用饱和氯化钠溶液洗涤,不可用水代替饱和氯化钠溶液。粗制乙酸乙酯用饱和碳酸钠溶液洗涤之后,酯层中残留少量碳酸钠,若立即用饱和氯化钙溶液洗涤会生成不溶性碳酸钙,往往呈絮状物存在于溶液中,使分液漏斗堵塞,所以在用饱和氯化钙溶液洗涤之前,必须用饱和氯化钠溶液洗涤,以便除去残留的碳酸钠。乙酸乙酯在水中的溶解度较大,15℃时100g水中能溶解8.5g,若用水洗涤,必然会有一定量的酯溶解在水中而造成损失。此外,乙酸乙酯的相对密度(0.9005)与水接近,在水洗后很难立即分层。因此,用水洗涤是不可取的。饱和氯化钠溶液既具有不的性质,又具有盐的性质,一方面它能溶解碳酸钠,从而将其双酯中除去;另一方面它对有机物起盐析作用,使乙酸乙酯在水中的溶解度大降低。除此之外,饱和氯化钠溶液的相对密度较大,在洗涤之后,静置便可分离。因此,用饱和氯化钠溶液洗涤既可减少酯的损失,又可缩短洗涤时间。
4、注意事项
(1) 加料滴管和温度计必须插入反应混合液中,加料滴管的下端离瓶底约5mm为宜。
(2) 加浓硫酸时,必须慢慢加入并充分振荡烧瓶,使其与乙醇均匀混合,以免在加热时
因局部酸过浓引起有机物碳化等副反应。
(3) 反应瓶里的反应温度可用滴加速度来控制。温度接近125℃,适当滴加快点;温度
落到接近110℃,可滴加慢点;落到110℃停止滴加;待温度升到110℃以上时,再
滴加。
(4) 本实验酯的干燥用无水碳酸钾,通常只少干燥半个小时以上,最好放置过夜。但在
本实验中,为了节省时间,可放置10分钟左右。由于干燥不完全,可能前馏分多些。
八、 教学方法
1、合成乙酸乙酯的反应是典型的可逆平衡反应,本实验应重点分析、总结提高可逆平衡反应产率的实验方法。
2、组织讨论以下问题:
(1) 为什么使用过量的乙醇?
(2) 蒸出的粗乙酸乙酯中主要含有哪些杂质?如何逐一除去?
(3) 能否用浓的氢氧化钠溶液代替饱和碳酸钠溶液来洗涤蒸馏液?为什么?
(4) 用饱和氯化钙溶液洗涤的目的是什么?为什么先用饱和氯化钠溶液洗涤?是否可用
水代替?
(5) 如果在洗涤过程中出现了碳酸钙沉淀,如何处理?
第三章 生理学实验报告的书写
? 实验报告是对实验的全面总结,是综合评定实验课成绩的重要依据之
一。实验报告的书写也是一项重要的基本技能训练,是今后撰写科学论文的初始演练。
一、实验报告的写作要求
1.按照每个实验的具体要求,实事求是,认真独立地按时完成实验报告。注意,要根据实验记录写实验报告,不可凭记忆或想象,否则容易发生错误或遗漏。
2.书写实验报告应使用统一的实验报告册和规范的撰写格式。
3.实验报告的书写应文笔简练、语句通顺、条理清晰、观点明确、字迹工整,并正确使用标点符号。
二、实验报告的具体内容
1.一般项目姓名、班级、组别、日期、室温、合作者、指导教师等。
2.实验序号和题目。
3.实验目的。
4.实验对象如为动物,要写明种属、性别和体重。
5.实验方法和步骤对实验指导书中已有的部分,可简写或省略。如实验操作改动较大,应详加记述。
6.实验结果这是实验报告中最重要的部分。应将实验过程中所观察到的现象忠实、正确、全面详细地加以记述。有曲线记录的实验,应尽量用原始曲线表示实验结果,以保证结果的真实性。实验结果的表达方式有以下几种形式。
(1) 描述法:是用文字将观察到的有关现象客观地加以描述。描述时需要有时间概念和顺序。凡属于定量的资料,例如高低、长短、快慢、轻重、多少等,均应以正确的计量单位及数值表达。必要时可进行统计学处理,以保证结论的可靠性。不能简单、笼统地描述,如心跳的变化不能只写心跳“加快”或“减慢”,而要写出心跳加快或减慢的具体数值。
(2) 波形法:指实验中描记的波形或曲线,经过编辑,剪贴在实验报告纸上,以显示实验结果。如记录到的呼吸、血压、肌肉收缩曲线等。在曲线上应有刺激记号、时间记号并加以必要的标注或文字说明。此外,还要就曲线频率、节律、幅度和基线做出定量分析。
(3) 表格法和简图法:对计量或记数性资料也可用列表或画图的方式表示,使结果更简明、突出,便于比较分析。制表时,一般将观察项目列在表内左侧,由上而下逐项填写;实验结果等则按顺序由左而右填写。绘图时,在坐标上应标明数字和单位。一般以横坐标表示各种刺激条件,纵坐标表示发生的各种反应,并在图的下方标注实验条件。
以上三种形式也可以并用,以达到最佳效果。
7.实验讨论是围绕实验目的,根据已知的理论知识,通过分析和思考,尝试对实验中出现的现象及结果做出客观、深入地解释,指出实验结果的生理意义。如果出现非预期结果,应分析其可能原因。
8.实验结论实验结论是从实验结果中归纳出的一般性、概括性的判断,也就是对该实验所能验证的概念或理论的简明总结。结论应简明扼要,切合实际,不应罗列和重复具体的结果,在实验中没有得到充分证明的问题不应写入结论中。
实验讨论和结论的书写是富有创造性的工作,应开动脑筋,积极思考,不能盲目抄袭书本。可适当开展同学间的讨论,加深对实验的理解。
【附】生理学实验报告的基本格式
姓名 班级 学号 实验室 (小组)
日期 室温 合作者
指导老师
实验名称 (题目) 实验目的 实验对象
实验步骤与方法 实验结果 讨论
实验结论
第二篇:深度解读乙酸乙酯的制备原理
深度解读乙酸乙酯的制备原理
绍兴一中分校吴文中
1、乙酸和乙醇反应速率很慢,常温下,需要15年以上达到化学平衡。
2、使用催化剂,如浓硫酸、弄磷酸,作用为了加快反应速率。
3、把产物及时分离出去,提高产率,假如酯难以被蒸馏出去,这把水蒸馏出去。
4、使用乙酸酐,则可以促进平衡往得到酯的方向移动,如阿司匹林的制备
5、加热的目的:加快反应速率,把产物及时带离反应体系。
6、把产物(酯)带离了反应体系,就少了催化剂,酯的水解速率大大降低。可以看作酯和水不反应了。
7、假如产物(酯)难以被蒸发出去,则把水蒸发出去。(分水器的作用)
8、教材中,用饱和的碳酸钠溶液来收集乙酸乙酯(饱和的碳酸钠降低了乙酸乙酯的溶解性,溶剂极性发生了改变),实际上,饱和的NaCl也可以使用,只是饱和氯化钠不能除乙酸)
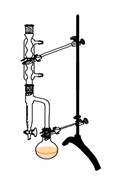
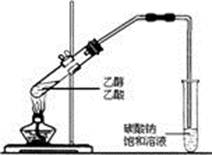
把该装置应用于乙酸乙酯的制备也是可以考虑的。
实验操作
在25mL刻度试管里加入1滴1%酚酞试液和15mL饱和碳酸钠溶液,将其固定在铁架台上,把球形干燥管插在刻度试管管口上,在硬质试管里先加入2mL灯用酒精,然后一边摇动一边缓慢地加入2mL浓硫酸、5mL37%醋酸和2粒小沸石,按图装置好。
用酒精灯加热试管底部的石棉网,1.5min后,可见到刻度试管中有无色透明的油珠上浮到饱和碳酸钠溶液面上,约5min后,当饱和碳酸钠溶液由玻璃管逆流上升时,证明乙酸乙酯已基本蒸馏完毕,即拔去干燥管上单孔塞,停止加热,拿走干燥管,刻度试管中呈现两层颜色不同的液体,即上层是无色透明具有果香味的油状液体乙酸乙酯,其体积为2.3mL,下层是玫瑰红色的水溶液。
几点说明
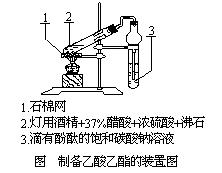 1.该实验装置气密性要良好。
1.该实验装置气密性要良好。
2.在球形干燥管下,端连接一玻璃管,将其插入饱和碳酸钠溶液面下3~4cm处,这样既可增加冷凝效果,又可洗涤乙酸乙酯,除去乙酸、亚硫酸等杂质,同时又能防止硬质试管内因低沸点混合物大量蒸出,蒸气压大幅度下降,引起饱和碳酸钠溶液倒吸流入管内,即使操作不小心,饱和碳酸钠溶液只会倒吸到干燥管中,液面即与玻管下端脱离,不会发生事故。
3.在该实验装置中,使用石棉网和沸石的目的在于有效的控制温度,使酯化反应受热均匀,防止反应液爆沸、冲塞和碳化、确保实验安全,同时能减少醋酸大量蒸出和亚硫酸生成。
?
-
实验二 乙酰乙酸乙酯的制备
实验二乙酰乙酸乙酯的制备一实验目的1学习制备乙酰乙酸乙酯的原理和方法加深对Claisen酯缩合反应原理的理解和认识2熟悉在酯缩合反…
-
乙酰乙酸乙酯的制备 实验报告
乙酰乙酸乙酯的制备前言乙酰乙酸乙酯无色至淡黄色的澄清液体微溶于水易溶于乙醚乙醇有刺激性和麻醉性可燃遇明火高热或接触氧化剂有发生燃烧…
-
乙酰乙酸乙酯的制备
理论产量0041301452g产率八问题和讨论1本实验所用仪器未经干燥处理对反应有何影响答一开始要用到纯的金属钠有水会发生局部过热…
-
乙酰乙酸乙酯的制备
乙酰乙酸乙酯的制备实验目的1了解通过Claisen缩合反应由乙酸乙酯制备三乙的基本原理和方法2了解和掌握减压蒸馏装置的原理和作用实…
-
乙酰乙酸乙酯的制备.doc1.
乙酰乙酸乙酯的制备作者化工106程鹏摘要含有a氢的酯在碱性催化剂存在下能和另一份子酯发生克莱森酯缩合反应生成酮酸酯乙酰乙酸乙酯就是…
-
二年级数学教学总结
二年级数学教学总结本学期我担任二年级2班的数学教学工作。一学期以来我根据学生的实际情况,努力地去激发学生的学习兴趣,培养学生良好的…
-
20xx大学生预备党员半年总结
20xx年大学生预备党员半年总结入大学以来,接受了系统的中国共产党的知识了。递交入党申请书,成为入党积极分子也将近一年了,在这时候…
-
基层党支部工作总结
XX年,******党委认真贯彻落实****党委的工作指导思想、工作部署和工作要求,坚持以三个代表重要思想和党的十六届三中、四中全…
-
二年级数学教学总结
二年级上册数学教学总结总堡学校汪元德20xx.1.18本学期我担任二年级的数学教学工作。一学期来,我努力根据学生的实际情况,采取有…
-
单片机重点总结
第1章1、微型计算机通常由哪些部分组成?各有哪些功能?答:微型计算机通常由控制器、运算器、存储器、输入/输出接口电路、输入设备和输…