GSP认证现场检查缺陷项目整改报告
XXXX医药有限公司
GSP认证现场检查缺陷项目整改报告
XX省食品药品监督管理局:
XX市食品药品监督管理局:
受XX省药品认证管理中心委派的检查组于20##年X月X日依据《药品经营质量管理规范认证管理办法》对我公司的各项情况进行了全面的检查。检查情况如下:
严重缺陷:0项
一般缺陷:8项
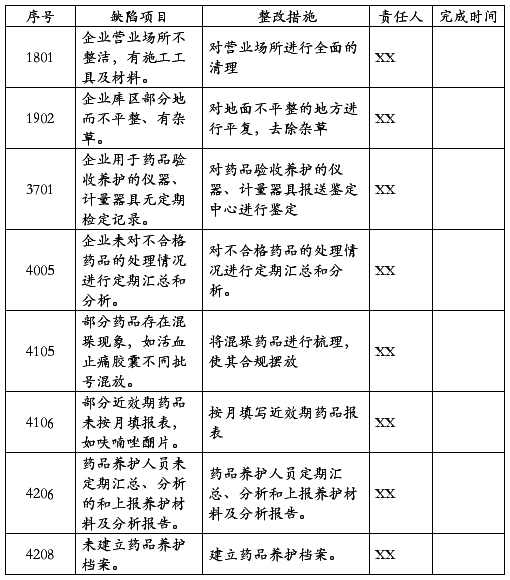
1801 企业营业场所不整洁,有施工工具及材料。
1902 企业库区部分地而不平整、有杂草。
3701 企业用于药品验收养护的仪器、计量器具无定期检定记录。
4005 企业未对不合格药品的处理情况进行定期汇总和分析。
4105 部分药品存在混垛现象,如活血止痛胶囊不同批号混放。.
4106 部分近效期药品未按月填报表,如呋喃唑酮片。
4206 药品养护人员未定期汇总、分析的和上报养护材料及分析报告。
4208 未建立药品养护档案。
针对以上GSP认证现场检查缺陷项目情况,本公司及时组织全体员工认真学习《药品管理法》、药品“GSP"管理规范和其他有关法律法规。认真进行整改,提出整改措施,责任到人。为此,本公司就GSP认证现场检查缺陷项目整改情况向XX省食品药品监督管理局、XX省食品药品监督管理局报告。
XXXX医药有限公司
GSP认证现场检查不合格项目的整改
第二篇:GSP整改报告
湖北省*************药店 关于GSP认证检查一般缺陷项目
整
改
报
告
年 月 日
湖北省***********药店
关于GSP认证检查缺陷项目
食品药品监督管理局:
我药店于***年*月*日接受了市食品药品监督管理局GSP认证检查验收组的细致、全面的现场检查。通过这次检查,我店深刻的领会了GSP的精神,进一步提高了药店人员对GSP的认识。在质管员的指导下,我店人员迅速、认真的对查出的缺陷项目进行了整改,现将整改回报如下:
一、现场检查缺陷项目
验收组的检查结果为:严重项目为0项,一般项目3项 6006 企业专职质量管理人员收集药品质量档案不全; 6807 企业未配置中药饮片临方炮制设备 7102 药品购进记录保存不全;
二、缺陷项目的整改情况
检查结束后,药店负责人立即组织全体人员针对此次检查开会,讨论对出现的3项缺陷进行细致的分析,并讨论问题存在的原因,针对缺陷项目制定出切实可行的整改措施并责任到人。
6006 企业专职质量管理人员收集药品质量档案不全 责任人:****
整改措施
立即向供货方索要购进药品的质量档案,并归纳存档。 6802 企业未配置中药饮片临方炮制设备
责任人:*****
整改措施
按规定立即添置重要饮片临方炮制设备
7102 药品购进记录保存不全;
责任人:****
整改措施
今后一律按规定做每次的药品购进工作,并按规定记录,质管部人员进行监督并抽查。
以上是我店根据这次GSP认证检查出现一般项目的整改报告,我店会在以后的工作中严格按照《GSP》、《药品管理法》等法律、法规来做,将工作落到实到人、责任到岗、诚信经营,确保人民群众的用药安全。敬请市领导有关人员经常来我店进行监督、指导和检查。
附:整改完成情况报表
湖北省*******药店 年 月 日
湖北省***********药店
GSP认证检查一般缺陷项目整改完成情况报表

-
GSP认证现场检查缺陷项目整改报告
XX医药有限公司文件20xx015号GSP认证现场检查缺陷项目整改报告XXX食品药品监督管理局药品流通监管处审评认证中心受省局审评…
-
GSP认证现场检查缺陷项目整改报告
药店文件20xx5号GSP认证现场检查缺陷项目整改报告药品监督管理局药店于20xx年月日接受了GSP认证检查组的现场检查检查发现有…
-
总部GSP认证现场检查缺陷项目整改报告 (1)
药业零售连锁有限公司GSP认证现场检查缺陷项目整改报告食品药品监督管理局受贵局委派的三人专家检查组于20xx年月日依据药品经营质量…
-
关于GSP认证现场检查不合格项目的整改报告
XXXX关于GSP认证现场检查不合格项目的整改报告XX食品药品监督管理局按照XX食品药品监督管理局药品评审认证中心的安排GSP认证…
-
GSP认证现场检查缺陷项目整改报告
XXXX医药有限公司GSP认证现场检查缺陷项目整改报告XX省食品药品监督管理局XX市食品药品监督管理局受XX省药品认证管理中心委派…
-
药店gsp认证现场检查不合格项目整改
山西药店GSP认证现场检查不合格项目整改报告省市食品药品监督管理局20xx年10月12日贵局对河南东森医药有限公司第二平价药店进行…
-
GSP认证现场检查缺陷项目整改报告
药店文件20xx5号GSP认证现场检查缺陷项目整改报告药品监督管理局药店于20xx年月日接受了GSP认证检查组的现场检查检查发现有…
-
XXX大药房GSP认证现场检查缺陷项目整改报告2
xxxx大药房GSP认证现场检查不合格项目整改报告xxx食品药品监督管理局xxxx大药房于20xx年月日xxx食品药品管理局提交G…
-
GSP认证现场检查缺陷项目整改报告
XX医药有限公司文件20xx015号GSP认证现场检查缺陷项目整改报告XXX食品药品监督管理局药品流通监管处审评认证中心受省局审评…
-
关于GSP认证现场检查不合格项目的整改报告
XXXX关于GSP认证现场检查不合格项目的整改报告XX食品药品监督管理局按照XX食品药品监督管理局药品评审认证中心的安排GSP认证…
-
20xx年度GSP认证整改报告
XXXX大药房XXX【20xx】07号整改报告六安市食品药品监督管理局:六安市食品药品监督管理局GSP认证检查组于20xx年x月x…