EDTA标准溶液的配制与标定实验报告
EDTA标准溶液的配制与标定实验报告
EDTA标准溶液的配制与标定
一、实验目的
(1)、掌握EDTA标准溶液的配制与标定方法。
(2)、掌握铬黑T指示剂的应用条件和终点颜色变化。
二、实验原理
EDTA(Na2H2Y)标准溶液可用直接法配制,也可以先配制粗略浓度,再用金属Zn、ZnO、CaCO3或MgSO4· 7H2O等标准物质来标定。当用金属锌标定时,用铬黑T(H3In)做指示剂,在pH=10的款冲溶液中进行,滴定到溶液呈蓝色时为止。滴定反应式:
指示剂反应 Hln2- + Zn2+ = Znln- + H+
滴定反应 H2Y2- + Zn2+ = ZnY2- + 2H+
终点反应 Znln- + H2Y2- ↔ ZnY2- + Hln2- + H+
二、实验注意事项
(1)、称取EDTA和金属时,保留四位有效数;
(2)、控制好滴定速度;
(3)、加热锌溶解时,用表面皿盖住以免蒸发掉。
三、主要仪器与药品
仪器:酸式滴定管、25ml移液管、250ml容量瓶、250ml锥形瓶、250ml烧杯、表面皿。
药品:EDTA二钠盐、金属锌、1:1的氨水、1:1的HCl 、铬黑T指示剂、氨水—NH4Cl缓冲液(PH=10)
四、实验过程及原始数据记录
(1)、称取分析纯EDTA二钠盐1.9g左右,配制成500ml溶液。
(2)、称取0.15~0.2g金属Zn,加入1:1 HCl 5ml,盖好表面皿,使锌完全溶解,用水冲洗表面皿及烧杯内壁,然后将溶液移入250ml容量瓶中,再加水至刻度摇均,用25ml移液管吸此溶液置于250ml锥形瓶中,滴加1:1 氨水至开始出现Zn(OH)2白色沉淀,再加PH=10的缓冲溶液10ml ,加水稀释至100ml ,加入少许(约0.1g)铬黑T指示剂,用待标定的EDTA溶液滴定至溶液由酒红色变为纯蓝色,即为滴定终点。
EDTA的标定[ m(Zn) = 0.1815g ]
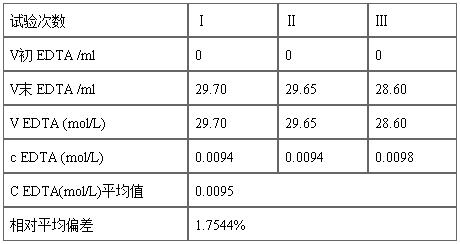
计算过程
c EDTA(mol/L)= m(Zn)/[M(Zn)* V] *1000*25/250
式中m(Zn)为称取分析纯Zn的质量(g);M(Zn)为Zn的摩尔质量(g/mol);V为标定时所用EDTA的体积(ml)。
第一次:
c (EDTA) =0.185/(65*29.7)* 1000 * 25/250=0.0094 mol/L
第二次:
c (EDTA) =0.1815/ (65 * 29.65) * 1000 * 25/250=0.0094 mol/L
第三次:
c (EDTA) =0.1815/ (65 * 28.6) * 1000 * 25/250=0.0098 mol/L
c EDTA(mol/L)平均值=(0.0094+0.0094+0.0098)/3=0.0095
c EDTA(mol/L)平均偏差= (|0.0094-0.0095 | + |0.0094-0.0095 |+ |0.0098-0.0095 |)/ 3 =0.0001667
c EDTA(mol/L)相对平均偏差=平均偏差/平均值*100%=0.0001667/0.0095 *100%=1.7544%
实验日期:20XX.10.25
第二篇:EDTA标准溶液的配制与标定
实验3 EDTA标准溶液的配制与标定
一、实验目的
1.掌握EDTA标准溶液配制和标定的方法;
2.了解金属指示剂变色原理及使用注意事项。
二、实验原理
EDTA标准溶液常用乙二酸四乙酸二钠(EDTA-2Na·2H2O)配制。EDTA-2Na·2H2O为白色结晶粉末,因不易制得纯品,标准溶液常用间接法配制,以ZnO为基准物质标定其浓度。滴定条件:pH=10,以铬黑T为指示剂,终点由酒红色变为纯蓝色。滴定过程中的反应为:
滴定前: 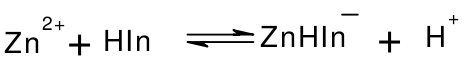
终点时: 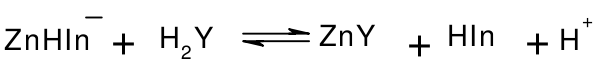
纯蓝色
三、试 剂
EDTA-2Na·2H2O :A.R.
ZnO:基准试剂
铬黑T指示剂:称取铬黑T 0.5g和盐酸羟胺,溶于乙醇,用乙醇稀释至100mL,摇匀。
氨-氯化铵缓冲溶液(pH=10):取20gNH4Cl溶于少量水中,加入100mL浓氨水,用水稀释至1000mL。
氨试液:取浓氨水400mL,加水使成1000mL。
四、实验步骤
(一) 0.05mol/LEDTA溶液的配制 取EDTA-2Na·2H2O9.5g,加100mL蒸馏水温热使溶液,稀释至500mL,摇匀,贮存于聚乙烯瓶中。
(二) 0.05mol/LEDTA溶液的标定 精密称取已在800℃灼烧至恒重的基准ZnO约0.12g,加稀HCl3mL使之溶解,加蒸馏水25mL,滴加氨试液至溶液呈微黄色。再加蒸馏水25mL,氨-氯化铵缓冲溶液10mL,铬黑T指示剂3—4滴,用EDTA溶液滴定至溶液由酒红色变为纯蓝色即为滴定终点。作三次平行测定。
实验流程
五、数据记录与处理
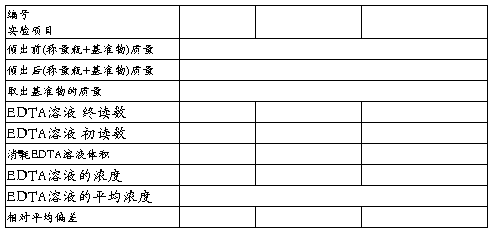
六、注意事项
1.滴加氨试液至溶液呈微黄色,应边加边摇,若出现Zn(OH)2↓。遇此情况,可用稀HCl调回,使沉淀溶解。
2.配位反应为分子反应,反应速度不如离子反应快,近终点时,滴定速度不宜太快。
七、思考题
1.酸度对配位反应有何影响?为什么要加氨-氯化铵缓冲溶液?
2.选择金属指示剂的原则是什么?
参考文献:张龙、潘亚芬 《化学分析技术》
邢文卫、李炜 《分析化学实验》
-
实验报告_酸碱标准溶液的配制和标定
大学化学实验实验一酸碱标准溶液的配制和标定实验目的1掌握标准溶液的配制方法2掌握滴定法定量测定溶液浓度的原理熟悉滴定管移液管的准备…
-
化学实验报告 实验__氢氧化钠标准溶液的配制与标定1
实验报告姓名班级同组人自评成绩项目氢氧化钠标准溶液的配制与标定课程学号一实验目的1掌握氢氧化钠溶液的配制和标定方法2熟悉滴定操作和…
-
EDTA标准溶液的配制与标定实验报告
EDTA标准溶液的配制与标定EDTA标准溶液的配制与标定一实验目的1掌握EDTA标准溶液的配制与标定方法2掌握铬黑T指示剂的应用条…
-
实验5 盐酸标准溶液的配制和标定
实验五盐酸标准溶液的配制和标定一实验目的1掌握减量法准确称取基准物的方法2掌握滴定操作并学会正确判断滴定终点的方法3学会配制和标定…
-
EDTA标准溶液的标定和水的硬度测定(实验报告)
EDTA标准溶液的标定和水的硬度测定四川农业大学生命科学与理学院625014应用化学092王雨20xx6824摘要本实验利用络合滴…
-
实验九 EDTA标准溶液的配制与标定
实验七EDTA标准溶液的配制与标定一实验目的1掌握EDTA标准溶液的配制与标定2掌握使用铬黑T指示剂的条件和正确判断终点的方法二实…
-
实验:EDTA标准溶液的配制与标定
配位滴定法EDTA005molL标准溶液的配制与标定一实验目的1了解EDTA标准溶液的配制和标定原理2掌握常用的标定EDTA的方法…
-
实验六 EDTA标准溶液的配制与标定(上课)
实验六EDTA标准溶液的配制与标定一实验目的1掌握配位滴定的原理了解配位滴定的特点2学会EDTA标准溶液的配制标定及稀释3学会铬黑…
-
下周实验 EDTA标准溶液的配制与标定
EDTA标准溶液的配制与标定实验目的1掌握EDTA标准溶液的配制与标定方法2学会判断配位络合滴定的终点3了解缓冲溶液的应用4进一步…
-
实验七:缓冲溶液的配制与性能
实验七缓冲溶液的配制与性能一实验目的1学习缓冲溶液的配制方法加深对缓冲溶液性质的理解2了解缓冲容量与缓冲剂浓度和缓冲组分的比值关系…
-
实验报告_酸碱标准溶液的配制和标定
大学化学实验实验一酸碱标准溶液的配制和标定实验目的1掌握标准溶液的配制方法2掌握滴定法定量测定溶液浓度的原理熟悉滴定管移液管的准备…