1-溴丁烷的制备(实验报告)
1- 溴丁烷的制备(实验报告)
一、实验目的
1. 学习用溴化钠,浓硫酸和正丁醇制备1-溴丁烷的原理和方法
2. 学习有害气体吸收装置的安装,巩固加热回流的操作
二、实验原理
主要反应: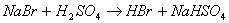


 副反应
副反应 

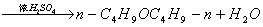
三、实验方法
1.100ml三口瓶加入13.67g溴化钠加10ml正丁醇烧瓶上装可吸收有害气体的回流冷凝管。
2.锥形瓶加10ml水,边振摇边加16ml弄硫酸。用冷水冷却,将混合液从三口瓶一口加入,沸石,小火回流59min,冷却、
3.取下废气装置,30ml冰水于三口瓶一口加入,溶解固体,倒入分液漏斗,有机层加入5ml冷却浓硫酸,震荡,静置分层,放出下层,上层1-溴丁烷依次用8ml饱和碳酸钠,收集下层,然后,10ml水洗涤,收集下层,之后将其加入小锥形瓶,无水氯化钙干燥。
4.然后将粗品滤入50ml蒸馏烧瓶,小火蒸馏,收集馏分,最后温度基本稳定在100‘C、
四、实验药品
1.正丁醇:天津风船化学试剂科技有限公司 (AR 20100918)
2.溴化钠:天津市化学试剂三厂 (AR 20050310)
3.NAOH:天津风船化学试剂科技有限公司 (AR 20100508)
4.无水CaCl2: 天津市光复精细化工研究所 (AR 20101025)
5. 浓硫酸:北京化工厂 (AR 20100304)
6.碳酸钠:天津风船化学试剂科技有限公司 (AR 20100308)
五、注意事项
分液漏斗分液时,粗产物倒入分液漏斗后(第一次分液)弃去下层;加浓硫酸后(第二次分液)弃去下层;饱和碳酸钠和水洗涤时(第三、第四次分液)弃去上层。
六、数据处理
1.溴化钠质量:13.67g
2.反应开始时间:14:39 结束时间:15:38
3.蒸馏开始时间:16.10 结束时间:16.28
4.沸程:99-100‘C
5.空瓶重:17.08g 瓶+产物:24.09g
七、实验装置


八、思考题
1.制备1-溴丁烷除本方法外,还有哪些方法?
答:可用三口瓶装置,用恒压滴液漏斗滴加稀释后的硫酸以增加氢溴酸的利用率
2.反应混合液中可能含有那些杂质?如何除去?
① 粗1-溴丁烷中含有小量未反应的正丁醇和正丁醚以及1-丁烯等杂质,他们都能溶解于冷浓硫酸除去
② 粗1-溴丁烷中有事因含有少量游离的溴而显粉红色或红棕色,可用少量亚硫酸氢钠的水溶液除去
3. 用无水氯化钙干燥脱水,蒸馏时为什么要将氯化钙除去?
无水氯化钙的吸水原因是生成了结晶水,加热条件下,结晶水会失去,回到1-溴丁烷中,就失去了干燥的意义。
------------------
第二篇:1-溴丁烷的制备
1-溴丁烷的制备
思考题
1. 溴丁烷制备实验为什么用回流反应装置?
答:此反应较慢,需要在较高的温度下、长时间反应,而玻璃反应装置可达到的最高反应温度是回流温度,所以采用回流反应装置。
2. 溴丁烷制备实验为什么用球型而不用直型冷凝管做回流冷凝管?
答:因为球型冷凝管冷凝面积大,各处截面积不同,冷凝物易回流下来。
3. 溴丁烷制备实验采用1﹕1的硫酸有什么好处?
答:减少硫酸的氧化性,减少有机物碳化;水的存在增加HBr溶解量,不易逃出反应体系,减少HBr损失和环境污染。
4. 什么时候用气体吸收装置?怎样选择吸收剂?
答:有污染环境的气体放出时或产物为气体时,常用气体吸收装置。吸收剂应该是价格便宜、本身不污染环境,对被吸收的气体有大的溶解度。如果气体为产物,吸收剂还应容易与产物分离。
5. 1—溴丁烷制备实验中,加入浓硫酸到粗产物中的目的是什么?
答:除去粗产物中未反应的原料丁醇或溶解的副产物丁烯等。
6. 1—溴丁烷制备实验中,粗产物用75度弯管连接冷凝管和蒸馏瓶进行蒸馏,能否改成一般蒸馏装置进行粗蒸馏?这时如何控制蒸馏终点?
答:可用一般蒸馏装置进行粗蒸馏,馏出物的温度达到100℃时,即为蒸馏的终点,因为1-溴丁烷/水共沸点低于100℃,而粗产物中有大量水,只要共沸物都蒸出后即可停止蒸馏。
7. 在1—溴丁烷制备实验中,硫酸浓度太高或太低会带来什么结果?
答:硫酸浓度太高:
(1)会使NaBr氧化成Br2,而Br2不是亲核试剂。
2 NaBr + 3 H2SO4(浓) →Br2 + SO2 + 2 H2O +2 NaHSO4
(2)加热回流时可能有大量HBr气体从冷凝管顶端逸出形成酸雾。
硫酸浓度太低:生成的HBr量不足,使反应难以进行。
注意事项
1、 加料时,不要让溴化钠粘附在液面以上的烧瓶壁上,加完物料后要充分摇匀,防止硫酸局部过浓,一加热就会产生氧化副反应,使产品颜色加深。
2、 加热时,一开始不要加热过猛,否则,反应生成的HBr来不及反应就会逸出,另外反应混合物的颜色也会很快变深。操作情况良好时,油层仅呈浅黄色,冷凝管顶端应无明显的HBr逸出。
3、 粗蒸正溴丁烷时,黄色的油层会逐渐被蒸出,应蒸至油层消失后,馏出液无油滴蒸出为止。检验的方法是用一个小锥形瓶,里面事先装一定的水,用其接一两滴馏出液,观察其滴入水中的情况,如果滴入水中后,扩散开来,说明已无产品蒸出;如果滴入水中后,呈油珠下沉,说明仍有产品蒸出。当无产品蒸出后,若继续蒸馏,馏出液又会逐渐变黄,呈强酸性。这是由于蒸出的是HBr水溶液和HBr被硫酸氧化生成的Br2,不利于后续的纯化。
4、 如果用磨口仪器,粗蒸时,也可将75°弯管换成蒸馏头进行蒸馏,用温度计观察蒸气出口的温度,当蒸气温度持续上升到105℃以上而馏出液增加甚慢时即可停止蒸馏,这样判断蒸馏终点比观察馏出液有无油滴更为方便准确。用浓硫酸洗涤粗产品时,一定要事先将油层与水层彻底分开,否则浓硫酸被稀释而降低洗涤的效果。如果粗蒸时蒸出的HBr洗涤前未分离除尽,加入浓硫酸后就被氧化生成Br2,而使油层和酸层都变为橙黄色或橙红色。
5、 酸洗后,如果油层有颜色,是由于氧化生成的Br2造成的,在随后水洗时,可加入少量NaHSO3,充分振摇而除去。
6、 用无水氯化钙干燥时,一般用块状的,粉沫的容易造成悬浮而不好分离。氯化钙的用量视粗产品中含水量而定。一般加2-3块,摇动后,如果溶液变澄清,氯化钙表面没有变化就可以了。如果粗产品中含水量较多,摇动后,氯化钙表面会变湿润,这时应再补加适量的氯化钙。用氯化钙干燥产品,一般至少放置半个小时,最好放置过夜,才能干燥完全,但实验中由于时间关系,只能干燥5-10分钟。有时干燥前溶液呈混浊,经干燥后溶液变澄清,但这并不一定说明它已不含水分。干燥后,干燥剂可通过过滤而除去,但本实验为了省事,可用倾倒的方法,用玻璃棒挡住别让干燥剂进入蒸馏瓶中就可以了。
7、 本实验最后蒸馏收集99-103℃的馏分,但是,由于干燥时间较短,水一般除不尽,因此,水和产品形成的共沸物会在99℃以前就被蒸出来,这称为前馏分,不能做为产品收集,要另用瓶接收,等到99℃后,再用事先称重的干燥的锥形瓶接收产品。
有害气体吸收
在某些有机化学实验中会产生和逸出有刺激性的、水溶性的气体(例如,在制对甲苯乙酮时会产生大量氯化氢,在制正溴丁烷时会逸出溴化氢),这时,必须使用气体吸收装置来吸收这些气体,以免污染实验室空气。常见的气体吸收装置见图1-6 ,其中图1-6(1)和图1-6(2)是用于吸收少量气体的装置。图1-6(1)中的漏斗口应略为倾斜,使一半在水中,一半露出水面,这样既能防止气体逸出,又可防止水被倒吸至反应瓶中。图1-6(2)的玻璃管应略微离开水面,以防倒吸。有时为了使卤化氢、二氧化硫等气体能较完全地被吸收,可在水中加少些氢氧化钠。若反应过程中会生成或逸出大量有害气体,特别当气体逸出速度很快时,应使用图1-6(3)的装置。在图1-6(3)中,水自上端流下(可利用冷凝管流出的水),并在恒定的平面上从吸滤瓶支管溢出,引入水槽。粗玻璃管应恰好伸入水面,被水封住,吸收效果较好。
1、反应装置的密封性要好。吸收液用水即可,气体导管出口处要接近但不能接触吸收液面。
2、实验中采用1:1硫酸,一方面减少副反应,另一方面吸收未反应的溴化氢气体,因此,不能用浓硫酸。
3、蒸出粗产品时,可以不加温度计。检验油滴的方法可用盛少清水的小烧杯接收几滴馏出液,观察烧杯底部有无小油珠。
4、蒸馏时所用的各仪器必须预先烘干,否则产品易浑浊。
5、接受瓶应预先称重,采用减量法可测得产品的重量。
-
实验三 1-溴丁烷的制备
实验三1溴丁烷的制备一实验目的1掌握在实验室以溴化钠浓硫酸和正丁醇制备1溴丁烷的原理和方法2练习带有有害气体吸收装置的回流操作3熟…
-
1-溴丁烷的制备实验报告
1溴丁烷的制备课程名称化学化工软件应用与操作姓名学号班级指导教师化学工程系目录一实验目的1二实验原理121主反应122副反应1三实…
-
有机化学实验报告--1-溴丁烷的制备
1溴丁烷的制备一实验目的1学习由醇制备溴代烃的原理及方法2练习回流及有害气体吸收装置的安装与操作3进一步练习液体产品的纯化方法洗涤…
-
1-溴丁烷的制备 实验报告
广东工业大学学院专业班组学号姓名协作者教师评定实验题目1溴丁烷的制备一实验目的学习由丁醇溴代制1溴丁烷的原理和方法练习带有吸收有害…
-
1-溴丁烷的制备(实验报告)
1溴丁烷的制备实验报告一实验目的1学习用溴化钠浓硫酸和正丁醇制备1溴丁烷的原理和方法2学习有害气体吸收装置的安装巩固加热回流的操作…
- 正溴丁烷的制备实验报告
-
实验七_正溴丁烷的制备
正溴丁烷的制备实验目的1了解以正丁醇溴化钠和浓硫酸为原料制备正溴丁烷的基本原理和方法2掌握带有害气体吸收装臵的加热回流操作3进一步…
-
有机化学实验报告--1-溴丁烷的制备
1溴丁烷的制备一实验目的1学习由醇制备溴代烃的原理及方法2练习回流及有害气体吸收装置的安装与操作3进一步练习液体产品的纯化方法洗涤…
-
1-溴丁烷的制备 实验报告
广东工业大学学院专业班组学号姓名协作者教师评定实验题目1溴丁烷的制备一实验目的学习由丁醇溴代制1溴丁烷的原理和方法练习带有吸收有害…
-
实验七 正溴丁烷的制备
实验十正溴丁烷的制备实验目的1了解以正丁醇溴化钠和浓硫酸为原料制备正溴丁烷的基本原理和方法2掌握带有害气体吸收装置的加热回流操作3…
-
1-溴丁烷的制备实验报告
1溴丁烷的制备课程名称化学化工软件应用与操作姓名学号班级指导教师化学工程系目录一实验目的1二实验原理121主反应122副反应1三实…