1-溴丁烷的制备实验报告

1-溴丁烷的制备
课程名称:《化学化工软件应用与操作》
姓 名:
学 号:
班 级:
指导教师:
化学工程系
2014 年 12 月 7 日
目录
一、 实验目的............................................................................................................ 1
二、 实验原理............................................................................................................ 1
2.1 主反应............................................................................................................ 1
2.2 副反应............................................................................................................ 1
三、 实验仪器与药品................................................................................................. 1
3.1 实验仪器........................................................................................................ 1
3.2 实验药品........................................................................................................ 1
四、 物理常数............................................................................................................ 2
五、 仪器装置图........................................................................................................ 3
六、 实验步骤............................................................................................................ 3
6.1 加料............................................................................................................... 3
6.2 加热溶解........................................................................................................ 3
6.3 冷却及蒸馏..................................................................................................... 3
6.4 除杂............................................................................................................... 3
6.5 重蒸............................................................................................................... 4
6.6 称量及计算产率.............................................................................................. 4
6.7 探讨浓硫酸用量对产率的影响......................................................................... 4
七、 数据处理............................................................................................................ 5
八、 数据分析............................................................................................................ 6
九、 实验注意事项..................................................................................................... 6
一、 实验目的
1.1 学习以丁醇、溴化钠和浓硫酸制备1-溴丁烷的原理和方法。
1.2 练习连有气体吸收装置的加热回流操作和液体干燥操作。
1.3 学习使用分液漏斗洗涤液体的方法。
1.4 基本掌握蒸馏操作。
二、 实验原理
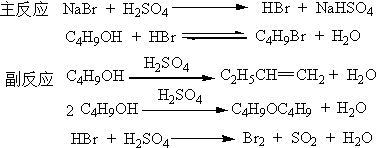
2.1 主反应


2.2 副反应
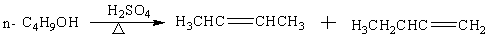
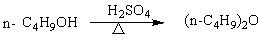
三、 实验仪器与药品
3.1 实验仪器
蒸馏烧瓶、直形冷凝管、带塞子的导气管、长颈漏斗、蒸馏头、温度计、锥形瓶、分液漏斗、小烧杯、洗瓶、铁圈。
3.2 实验药品
正丁醇 :7.4g或9.1mL(0.1mol)
溴化钠(无水):12.4g(0.12mol)
浓硫酸(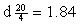 ):14mL(0.26mol)
):14mL(0.26mol)
四、 物理常数
表1 正丁烷、正溴丁烷、正丁醚的物理常数

五、 仪器装置图
Chemoffice绘制:


图1 溴丁烷的制备装置图和蒸馏装置图
六、 实验步骤
6.1 加料
在100mL圆底烧瓶中加入12ml水,置烧瓶于冰水浴中,小心地分多次加入14mL浓硫酸,充分混合。继续冷却,加入9.1mL正丁醇,混合均匀,然后将12.4g研细的溴化钠分多次加入烧瓶,每加一次必须充分旋动烧瓶以免结块。撤去冰浴,擦干烧瓶外壁,加入几粒沸石,装上回流冷凝管,并在其上口用弯玻璃管连一气体吸收装置,以吸收反应时逸出的溴化氢气体。
6.2 加热溶解
在烧瓶下置一石棉网,用小火加热,经常摇动烧瓶直至大部分溴化钠溶解,调节火焰,使混合物平稳沸腾,缓缓回流30min,期间要间歇摇动烧瓶。
6.3 冷却及蒸馏
反应完成后,将反应物冷却5min,拆去回流冷凝管,补加1~2粒沸石,用75°弯管连接直形冷凝管,以50mL锥形瓶作为接受器,在石棉网上加热蒸馏,蒸出粗产物1-溴丁烷,直至馏出液中无液滴生成为止。
6.4 除杂
将馏液倒入分液漏斗中,用8~10ml水洗涤,小心地将下层粗产物放入一干燥的锥形瓶中,从漏斗上口倒出水层。为了除去未反应的正丁醇及副产物正丁醚,用4mL浓硫酸分两次加入锥形瓶内,每加入一次都要充分旋动锥形瓶并用冷水浴冷却,然后将混合物慢慢地倒入分液漏斗,静置分层,小心地尽量分去下层浓硫酸。油层依次用12mL水、6mL10%碳酸钠溶液、12mL水洗涤使呈中性。将下层1-溴丁烷粗产物放入干燥洁净的50mL锥形瓶中,加入约1g粒状无水氯化钙,塞紧瓶塞,间歇振摇,直至液体澄清为止。
6.5 重蒸
将干燥后的液体小心倒入50mL干燥洁净的蒸馏烧瓶中(切勿使氯化钙落入烧瓶),加入1~2粒沸石,在石棉网上加热蒸馏,收集99~102℃馏分于已知质量的样品瓶中。
6.6 称量及计算产率
用一干燥的小烧杯称产品重量(或用量筒量取产品体积)。
6.7 探讨浓硫酸用量对产率的影响
用不同浓硫酸参加反应,重复以上步骤。记录数据。
七、 数据处理
表2 浓硫酸对产量的影响

OriginPro7.0绘制:
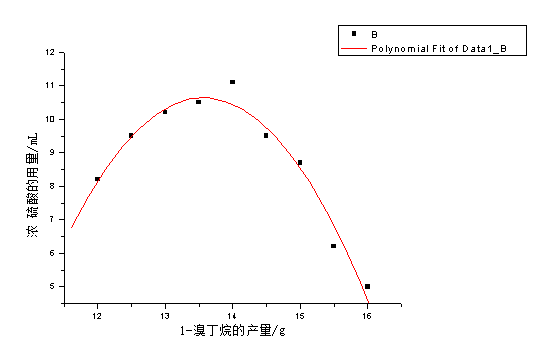
图2 浓硫酸用量对1-溴丁烷产量的影响
八、 数据分析
[2014/12/10 13:13 "/Graph1" (2457001)]
Polynomial Regression for Data1_B:
Y = A + B1*X + B2*X^2
Parameter Value Error
------------------------------------------------------------
A -175.3781 18.99282
B1 27.43727 2.72962
B2 -1.01169 0.09741
------------------------------------------------------------
R-Square(COD) SD N P
------------------------------------------------------------
0.96647 0.42737 9 <0.0001
------------------------------------------------------------
OriginPro7.0数据处理的方程式: Y = -1.0117*X^2 + 27.437*X – 175.38
当浓硫酸用量在13.5mL时,1-溴丁烷的产量最大。
当浓硫酸用量小于13.5时,氢溴酸的生成受阻,所以1-溴丁烷的产量下降。
当浓硫酸用量大于13.5时,副产物(正丁醚 )的生成增加,导致1-溴丁烷的产量下降。
当浓硫酸的浓度一定下,浓硫酸的用量过大,加大副反应的进行;浓硫酸的用量过小,则达不到反应所需。
九、 实验注意事项
9.1 注意浓H2SO4的稀释,混合均匀;
9.2 溴化钠先研碎再称量;
9.3 小火加热回流、否则易炭化;
9.4 注意粗产物的洗涤分离,产物属于哪一层?以及每步洗涤的作用是什么?
9.5 蒸出粗产物后,应趁热倒出残馏液,否则结块很难倒出。(倒出时有大量HBr气体放出,应在通风橱内进行磁搅子回收。)
第二篇:有机化学实验报告--1-溴丁烷的制备
1-溴丁烷的制备
一、实验目的
1.学习由醇制备溴代烃的原理及方法。
2.练习回流及有害气体吸收装置的安装与操作。
3.进一步练习液体产品的纯化方法、洗涤、干燥、蒸馏等操作。
二、实验原理
卤代烃是一类重要的有机合成中间体。由醇和氢卤酸反应制备卤代烷,是卤代制备中的一个重要方法,正溴丁烷是通过正丁醇与氢溴酸制备而成的,HBr是一种极易挥发的无机酸,无论是液体还是气体刺激性都很强。因此,在本实验中采用NaBr与硫酸作用产生HBr的方法,并在反应装置中加入气体吸收装置,将外逸的HBr气体吸收,以免造成对环境的污染。在反应中,过量的硫酸还可以起到移动平衡的作用,通过产生更高浓度的HBr促使反应加速,还可以将反应中生成的水质子化,阻止卤代烷通过水的亲核进攻返回到醇。
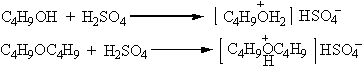
醇类、醚类可与浓硫酸作用生佯盐溶于浓硫酸中,故用浓硫酸洗涤的目的是除录像机,又佯盐遇水分解,必须用干燥漏斗进行此步洗涤(1):
三、实验药品及物理常数

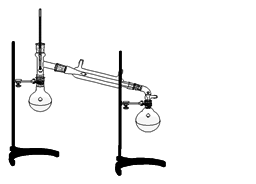
四、实验装置图
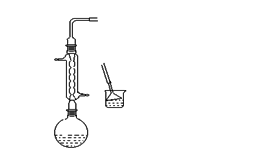
回流冷凝装置 蒸馏装置
五、实验步骤
(1)在100ml圆底烧瓶中加入15ml水,然后加入18ml浓硫酸(分3-4次加),摇匀后,冷却至室温,再加入11.2ml正丁醇,混合后加入15g溴化钠(小心加入,节不可在磨口处留有固体),充分振荡,加入几粒沸石,在烧瓶上装上球形冷凝管回流(因为球型冷凝管冷凝面积大,各处截面积不同,冷凝物易回流下来),在冷凝管的上口用软管连接一个漏斗,置于盛水的烧杯中。
(2)在石棉网上用小火加热回流半小时(在此过程中,要经常摇动)。冷却后,改作蒸馏装置,在石棉网上加热蒸中所有的溴丁烷。
(3)将馏出液小心地转入分液漏斗,用10ml水洗涤,小心地将粗品转入到另一干燥的分液漏斗中,用5ml浓硫酸洗涤。尽量分去硫酸层,有机层依次分别用水、饱和碳酸氢钠溶液和水各10ml洗涤。产物移入干燥的小三角烧瓶中,加入无水气温化钙干燥,间歇摇动,直至液体透明 。将干燥后的产物小心地转入到蒸馏烧瓶中。在石棉网上加热蒸馏,收集99-103度的馏分,产量约为6-7g(产率约为52%)。
六、实验纯化过程与现象
混合物(馏液)(呈淡白色浑浊状)
(丁醇、溴丁烷、丁醚、水、溴化氢、溴)

上层 下层
(理论:水、HBr、Br2) (理论:丁烷、溴丁烷、丁醚)
(实际:呈棕黄色,为有机层) (实际:呈淡白色,为无机层)
 5ml浓硫酸
5ml浓硫酸

上层 下层
(理论:溴丁烷) (理论:丁醇、丁醚、浓硫酸)
(实际:呈淡黄色) (实际:呈深黄色)
 10ml水
10ml水

上层 下层
(硫酸、水,呈淡黄色) (溴丁烷)
 10ml碳酸钠
10ml碳酸钠

上层 下层
(理论:硫酸、水) (理论:溴丁烷)
(实际:呈淡白色) (实际:呈纯白色浑浊)
 无水氯化钙干燥
无水氯化钙干燥

滤渣 滤液
(水合氯化钙 ) (溴丁烷、无色透明)
 蒸馏
蒸馏
正溴丁烷
产品产量:4.2g 理论产量:0.12*137=16.44 产率4.2/16.44=25%
七、讨论
理论与实验现象不同的原因及解决措施
1、 馏出液分两层,通常下层为粗正溴丁烷,上层为水,若反应的正丁醇较多,或因蒸馏过久蒸出一些溴化氢恒沸物,则液层的相对密度发生变化,油层可能悬浮或变为上层,遇此现象,可加清水稀释使油层下沉(2).
3、 加料用浓硫酸洗涤粗产品时,一定要事先将油层与水层彻底分开,否则浓硫酸被稀释而降低洗涤的效果。如果粗蒸时蒸出的HBr洗涤前未分离除尽,加入浓硫酸后就被氧化生成Br2,而使油层和酸层都变为橙黄色或橙红色。在随后水洗时,可加入少量NaHSO3,充分振摇而除去。
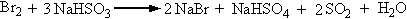
4、加料时,不要让溴化钠粘附在液面以上的烧瓶壁上,加完物料后要充分摇匀,防止硫酸局部过浓,一加热就会产生氧化副反应,使产品颜色加深。
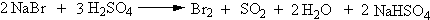
扩展
5、若不用浓硫酸洗涤粗产物,则在下一步蒸馏中,正丁醇与1-溴丁烷由于可形成共沸物(b.p. 98.6 0C, 含正丁醇13%),难以除去,使产品中仍然含有正丁醇杂质。
6、本实验最后蒸馏收集99-103℃的馏分,但是,由于干燥时间较短,水一般除不尽,因此,水和产品形成的共沸物会在99℃以前就被蒸出来,这称为前馏分,不能做为产品收集,要另用瓶接收,等到99℃后,再用事先称重的干燥的锥形瓶接收产品。
7、粗产品用浓硫酸洗涤后,不直接用饱和碳酸氢钠洗涤而要用水洗,然后加饱和碳酸氢钠洗涤的原因:因为刚用浓硫酸洗过的产品还含有不少浓硫酸(包括漏斗壁),若直接用饱和碳酸氢钠中和,则由于酸的量太多,酸碱中和产生大量的热,同时有大量的二氧化碳产生,极易在洗涤时溅出甚至冲出液体,不易操作,也造成产品的损失。为了使该中和反应不致于这么剧烈,故在加饱和碳酸氢钠之前,用水洗涤产品及其漏斗壁上的大部分浓硫酸。
-
实验三 1-溴丁烷的制备
实验三1溴丁烷的制备一实验目的1掌握在实验室以溴化钠浓硫酸和正丁醇制备1溴丁烷的原理和方法2练习带有有害气体吸收装置的回流操作3熟…
-
1-溴丁烷的制备实验报告
1溴丁烷的制备课程名称化学化工软件应用与操作姓名学号班级指导教师化学工程系目录一实验目的1二实验原理121主反应122副反应1三实…
-
1-溴丁烷的制备 实验报告
广东工业大学学院专业班组学号姓名协作者教师评定实验题目1溴丁烷的制备一实验目的学习由丁醇溴代制1溴丁烷的原理和方法练习带有吸收有害…
-
1-溴丁烷的制备(实验报告)
1溴丁烷的制备实验报告一实验目的1学习用溴化钠浓硫酸和正丁醇制备1溴丁烷的原理和方法2学习有害气体吸收装置的安装巩固加热回流的操作…
- 正溴丁烷的制备实验报告
- 正溴丁烷的制备实验报告
-
实验七_正溴丁烷的制备
正溴丁烷的制备实验目的1了解以正丁醇溴化钠和浓硫酸为原料制备正溴丁烷的基本原理和方法2掌握带有害气体吸收装臵的加热回流操作3进一步…
-
有机化学实验报告--1-溴丁烷的制备
1溴丁烷的制备一实验目的1学习由醇制备溴代烃的原理及方法2练习回流及有害气体吸收装置的安装与操作3进一步练习液体产品的纯化方法洗涤…
-
1-溴丁烷的制备 实验报告
广东工业大学学院专业班组学号姓名协作者教师评定实验题目1溴丁烷的制备一实验目的学习由丁醇溴代制1溴丁烷的原理和方法练习带有吸收有害…
-
实验七 正溴丁烷的制备
实验十正溴丁烷的制备实验目的1了解以正丁醇溴化钠和浓硫酸为原料制备正溴丁烷的基本原理和方法2掌握带有害气体吸收装置的加热回流操作3…
-
1-溴丁烷的制备(实验报告)
1溴丁烷的制备实验报告一实验目的1学习用溴化钠浓硫酸和正丁醇制备1溴丁烷的原理和方法2学习有害气体吸收装置的安装巩固加热回流的操作…