有机化学实验
有机化学实验
Organic Chemistry Experiment
(128学时)
一、教学目的
有机化学实验是化学化工学院各专业必修的一门独立的基础实验。它是训练学生牢固掌握有机实验的基本操作、技能和基础知识,通过有机化学实验加强学生对有机化学基础理论与基本概念的理解,培养学生正确选择有机化合物的合成、分离、提纯与分析、鉴定的方法以及分析解决问题和独立思考、独立工作的能力,并让学生及时掌握现代有机合成、分离、鉴定的手段。同时也是培养学生理论联系实际的作风、实事求是、严格认真的科学态度和良好的工作习惯的重要环节。
二、适用专业
本实验课程适合于化学类专业学生。
三、教学要求
1. 通过实验,培养学生掌握基本操作技术和技能
2. 正确记录,培养学生处理数据和表达实验结果的能力
3. 正确观测实验现象,提高分析判断、逻辑推理作出结论的能力
4. 正确选择实验方案,掌握解决实际问题的能力
5. 通过阅读文献及各种信息源,提高学生严谨的科学态度和开拓创新精神的能力
四、教学环节
(一)掌握基本操作技术和技能
1. 有机化学实验的一般知识
① 安全基本知识
② 常用玻璃仪器的清洗和干燥
③ 标准玻璃磨口仪器的清洗和干燥
④ 加热及热源的选择
⑤ 冷却及冷却剂的选择
⑥ 实验预习、记录和实验数据处理
⑦ 手册、词典及有关化学文献的查询
⑧ 有机化学实验的常用仪器
⑨ 有机化学实验的常用反应装置及应用(蒸馏、分馏、水蒸气蒸馏、减压蒸馏、分水器、索氏提取器、电动搅拌器、磁力搅拌器、气体吸收、无水操作等)
2. 有机化合物物理性质的测定
① 熔点的测定:正确掌握毛细管熔点测定法和熔点测定仪的使用
② 微量法和常量法测定沸点
③ 折光率的测定
④ 旋光度测定及旋光仪使用
3.有机化合物的分离及提纯
① 普通蒸馏
② 简单分离
③ 水蒸气蒸馏
④ 减压蒸馏
⑤ 重结晶(水溶剂、有机溶剂、混合溶剂)
⑥ 升华
⑦ 萃取和洗涤
⑧ 干燥和干燥剂
⑨ 色谱法(柱色谱、薄层色谱、气相色谱)
(二)应该了解的实验操作和技能
1. 使用近代物理仪器检测手段:红外光谱仪、核磁共振仪、紫外光谱仪、测试样品的制备、处理及仪器的使用、并能解析图谱。
2. 分步重结晶、气体反应、高温反应、低温反应、无水无氧反应、旋光异构体的分析、电合成等实验技术。
3. 旋转蒸发仪的使用
(三)官能团性质实验作为开放和综合实验进行
五、实验内容和学时安排
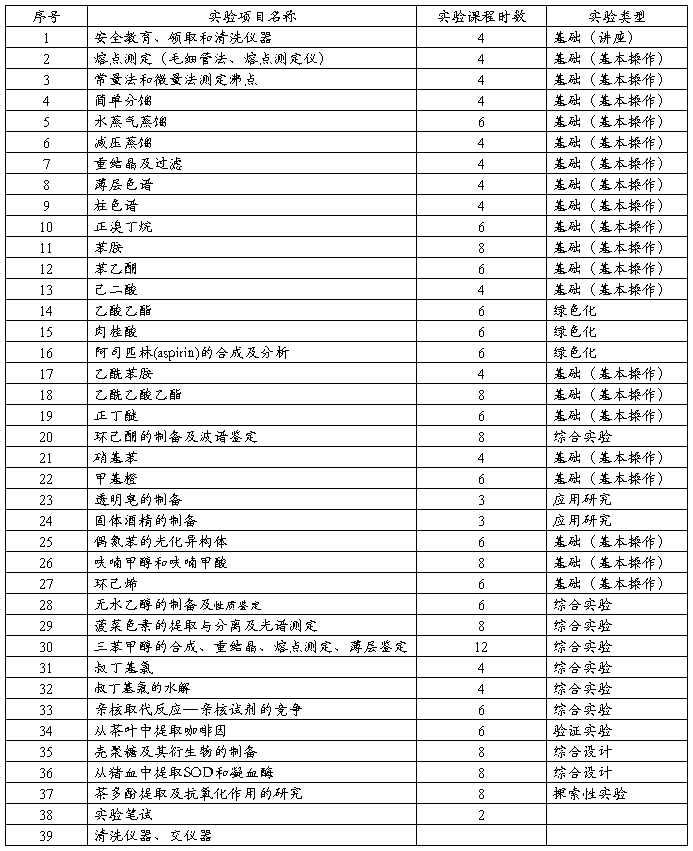
化学专业实验内容和学时安排(128学时)
药学专业实验内容和学时安排(64学时)

六、教材及参考书
《有机化学实验》第二版 兰州大学、复旦大学化学系有机教研室组编 高等教育出版社 1998年。
《有机化学实验》第二版 黄涛主编 高等教育出版社
《综合化学实验》 浙江大学、南京大学、北京大学、兰州大学主编 高等教育出版社
《综合化学实验》浙江大学化学系杜志强主编 科学出版社
《综合化学实验》王尊本主编 科学出版社
《有机化学实验》焦家俊编著 上海交通大学出版社
《新编普通化学实验》浙江大学化学系郑豪主编 科学出版社
《基础化学实验技术绿色化教程》林宝风等主编 科学出版社
《有机精细化学品实验》蔡干 曾汉维 钟振声合编 化学工业出版社
有机化学实验
Organic Chemistry Experiments
(生科、环科、医科大学32学时)
一、目的与任务
有机化学实验课的主要目的是:使学生掌握有机化学实验的基本技能;学会正确选择有机化学合物的合成、分离提纯与分析鉴定的方法;并且培养学生实事求是的科学态度、良好的学习习惯和科学素养。通过实验,加深学生对有机化学基本理论与概念的理解,增强运用所学知识解决实际问题的能力。为此,编写了有机化学实验教学大纲。
二、适合专业
本实验课程适合于生科、环科、医科大学生。
三、基本要求
培养学生动手能力,使学生能够正确、熟练、灵活、规范地掌握基本操作技能。
1. 玻璃管的弯曲和毛细管的拉制
2. 木塞、胶塞的选用和打孔
3. 玻璃仪器的洗涤和干燥
4. 常用仪器的选择和安装
5. 沸点和熔点的测定
6. 回流、蒸馏、分馏、水蒸气蒸馏
7. 分液漏斗的使用
8. 固体物质的重结晶
9. 各种过滤方法
10. 液体物质和固体物质的干燥
11. 薄层色谱和柱色谱
12. 加热和冷却
四、教学环节
1. 掌握基本操作技术和技能。
2. 合成实验是训练、巩固学生的基本操作的重要环节,也是培养学生正确选择有机化合物的合成、分离、提纯、分析鉴定的主要途径。作为一门基础课实验,基本操作实验和合成实验仍是以常量和半微量为主。
3. 性质实验的选择,是为了使学生获得直观的感性认识,为单独进行。
4. 有机化学实验作为一门独立的课程,在教学过程中,教师方兴未艾就实验原理及有关问题,进行必要的讲解和提问,防止学生“照方抓药”简单从事。必要时进行随堂测验(笔试),在最后结束时,适当地进行总结考试。
五、实验内容和学时安排
生科、环科、医科大专业实验内容和学时安排(32学时)

六、教材及参考书
《有机化学实验》第二版 黄涛主编 高等教育出版社
《有机化学实验》第二版 兰州大学、复旦大学化学系有机教研组编 高等教育出版社 1998年
第二篇:有机化学心得
有机化学心得
——13170210014 赖自成
有机化学又称为碳化合物的化学,是研究有机化合物的组成、结构、性质、制备方法与应用的科学,是化学中极重要的一个分支。学习大学有机化学已经一个学期了,相比与高中,无论是学习的深度还是广度都远远超过高中有机化学。这就要求我们学习有机化学应遵循一定的方法经验、在学习时适当拓宽我们的视野,更重要的是培养学好有机化学的素质。
(一)学习方法
大学有机化学绝大部分是学习掌握官能团,一般来说我们可以遵循这样的步骤:物质的分类和命名;官能团的制法;官能团的物理性质;官能团的化学性质、官能团的反应机理、影响反应的因素。既“是什么”、“哪里来”、“什么样”、“为什么”这四个步骤。
首先,通过学习物质的分类和命名可以帮助我们对官能团进行初步概念的建立,即回答“是什么”这个问题。在这一节中我们需要对一些特殊结构及命名给予关注,明辨取代基顺序和母体官能团顺序的区别。
而物质的制法则是回答“哪里来”了。这一节中由于制法的多样性,可能会涉及多章的内容。如在卤代烃的制法中就涉及有:烃的卤化、由不饱和烃制备、由醇制备、卤原子交换、偕(连)二卤代烷部分脱卤化氢、氯甲基化、由重氮盐制备这七种方法。其中涉及了二、三、五、七、九、十五这六章内容。在这一节中,由于每章学习基础不同,所以针对不同的制法需要有不同学习策略。以前章节的内容在课堂上就要进行背诵形成记忆;本章节的内容由于反应还不熟悉,可以抓住突出的特征,记忆反应的特点,这时脑子里就要开始建立新的反应类型。如卤原子交换制法中就需要建立卤原子可交换这一概念,并注意到I-能置换出Cl-这一特征;而对于后面的陌生章节,当堂只需要了解就行,后面内容与之联系不大,课后复习即可。
官能团的物理性质这一节主要是让我们对相应官能团衍生物的物理性质,如熔沸点等有个大体把握,以及了解一些相关实际应用,既“什么样”的问题。在这一节中我们应该掌握影响其熔沸点的一些因素,并学会进行比较。如卤代烃中,卤代烃的沸点随分子中碳原子数的增加而升高;烃基相同的卤代烃,其沸点是:碘代烃>溴代烃>氯代烃;在异构体中则是支链越多沸点越低。例如正丁基溴支链少于异丁基溴,则其沸点更高;正己基溴碳原子数少于正庚基溴,则其沸点更低。
官能团的化学性质及反应机理这块由于内容庞杂,最好在课堂前有个整体把握。如卤代烃的化学性质这一节中整体分为四大块:1.亲核取代反应(水解、与醇钠作用、与氰化钠作用、与氨作用、卤离子交换反应、与硝酸盐作用);2.消除反应(脱卤化氢、脱卤素);3.与金属反应(与镁反应、与锂反应);4.相转移催化反应。在化学性质这一节学习中除了记忆相应的化学方程式,我们还应该掌握相应的活性次序及其影响因素、相应的反应规则及其原理,为下节反应机理打下基础。例如溶剂对反应物活性的影响,在极性质子溶剂如(水、醇、酸)中、卤离子与溶剂通过形成氢键而被溶剂化,原子序数越大的卤素,其负离子与溶剂形成的氢键越弱,因此亲核性越强,由此可知,x-的亲核性次序为:I->Br-> Cl->F-;但在极性非质子溶剂(如二甲基酰胺、二甲基亚砜等)中,由于氢键的溶剂化作用不大,x-能自由地进行, x-的亲核性次序为:F-> Cl->Br-> I-。
官能团的反应机理这一节尤为重要,学好这一节会对整章的把握有一个内在的贯通。有机化学是大学课程中学方程式最多的一门课程,而且有机化学方程式并不只是要求简单的记忆,更需要掌握内在的规律,对反应机理等要有深刻的理解。同时,掌握机理后根据反应物性质,溶剂性质,反应温度,催化剂等条件经行一定的推断,才能够更有效的记忆有机化学方程式。如果遇到相似的机理我们还可以进行一定的比较。
以学习卤代烃一章中的亲核取代反应机理为例。饱和碳上的亲核取代反应,是指饱和碳原子上的一个原子或基团被另外一个带负电荷或中性的原子或基团取代的化学过程。根据新旧健断裂和生成情况,可分为一步进行的双分子亲核取代SN2机理和两步进行的单分子亲核取代SN1机理。在学习时通过对两种机理同时进行比较,如从烷基结构的影响、卤原子(离去基团)的影响、亲核试剂的影响、溶剂的影响以及邻助作用经行比较学习,能够更好的帮助我们的记忆。

(二)拓展视野
有机化学书中有许多有特点、有技术含量或和生活相关的反应和物质。虽然考试中它们不一定会作为重点,但是了解它们有助于拓宽我们的视野,增强我们的学习兴趣,同时夯实我们的知识点。下面我们来举2个关于自由基链式反应和与甲醛缩合的例子。
(1) 氟利昂
氟里昂是臭氧层破坏的元凶,它是本世纪20年代合成的,其化学性质稳定,不具有可燃性和毒性,被当作制冷剂、发泡剂和清洗剂,广泛用于家用电器、泡沫塑料、日用化学品、汽车、消防器材等领域。
在对流层的氟里昂分子很稳定,几乎不发生化学反应。但是,当它们上升到平流层后,会在强烈紫外线的作用下被分解,含氯的氟里昂分子会离解出氯原子,然后同臭氧发生连锁反应,不断破坏臭氧分子
如此周而复始,结果一个氯氟里昂分子就能破坏多达10万个臭氧分子。(虽然反应中氟里昂分子所起的作用类似于催化剂,但由于其参加了反应过程,因而严格意义上不属于催化剂)。反应机理以CF2Cl2为例。
臭氧在紫外线作用下,氯氟烃分解: CF2Cl2 → CF2Cl? + Cl?
自由基链反应:Cl? + O3 → ClO? + O2 ClO? + O3 → Cl? + 2O2
总的结果,可以用化学方程式表示为:O3 + O = 2O2
(2) 杯芳烃
1942年金克(Zinke,奥地利)首次合成得到,因其结构像一个酒杯而被古奇(C.D.Gutscht,美国)称为杯芳烃。杯芳烃可由对叔丁基苯酚与甲醛水溶液在氢氧化钠存在下反应制备,生成环状四聚体化合物。
杯芳烃上部是具有疏水性的空腔,能与中性分子(如氯甲烷、苯、甲苯等)形成配合物;分子底部是羟基,能螯合阳离子(如锂、钠、钾、钙等离子);因此杯芳烃能与中性分子和离子型分子均可形成配合物。例如,对叔丁基杯[4]芳烃能与甲苯形成稳定的包结物。
绝大多数的杯芳烃熔点较高,在250℃以上。在常用的有机溶剂中的溶解度很小,几乎不溶于水。杯芳烃可以用来作为离子交换剂、相转移催化剂以及涂料和黏合剂的组分等使用。另外,杯芳烃具有大小可调节的“空腔”,能够形成主-客复合物,与环糊精、冠醚相比,是一类更具广泛适应性的模拟酶,被称为继冠醚和环糊精之后的第三代主体化合物。
 对叔丁基杯[4]芳烃
对叔丁基杯[4]芳烃
(三)比拼素质
1967年,白川英树的研究生做实验时错用了一千倍的催化剂,加上搅拌器凑巧停止,在溶液表面生成了银色的薄膜状物。白川英树以此为切入点,进行了深入细致的研究,终于发现制备膜状聚乙炔的有效方法。1975年,美国的Macdiarmid教授偶然见到白川英树的金属光泽的膜状聚乙炔后,立即邀请他去美国与Heeger合作研究。后来,三人一起获得了20##年诺贝尔化学奖,也被传为佳话。
机会往往在我们身边,就像故事中白川英树偶然获得膜状聚乙炔,要把握这些机会需要我们不放过每一个细节,对每一次结果都要进行系统的分析。在学习有机化学课本中我们也许不会像科研一样对每一次结果经行仪器研究,但我们应对每一道作业题都要明确背后的化学方程式,对每一道化学方程式都需要明确背后的反应机理,对每一道反应机理都需要理解背后的缘由,对其中牵扯到的无机化学知识也需要我们适当翻阅。
学习有机化学表面上是对化学概念、化学方程式和化学机理经行记忆。但到最后,本质上其实是我们对素质的比拼。看谁更认真,看谁更仔细,同时还需要我们在学习时一起互帮互助。
-
有机化学实验实验报告
实验一有机化学实验基本操作实验目的1使学生明白进入有机化学实验学习必须阅读有机化学实验的一般知识的内容及安全实验是有机化学实验的基…
-
大学有机化学实验报告:肉桂酸的制备
有机化学实验报告实验名称肉桂酸的制备学院化学工程学院专业班级姓名学号指导教师日期20xx年12月22日一实验目的1了解肉桂酸的制备…
-
大学有机化学实验
西北大学化学系有机化学实验教学课件讲义非化学专业学生使用王少康李剑利前言有机化学实验教学课件融合了西北大学化学系有机化学实验课教学…
-
大学有机化学实验基本知识
实验一有机化学实验基本知识课时数3学时教学目标通过学习使学生了解做有机化学实验时要达到的目的和实验要求掌握有机化学实验室规则和实验…
-
大学有机化学实验报告:肉桂酸的制备
大学有机化学实验报告肉桂酸的制备一实验目的1了解肉桂酸的制备原理和方法2掌握水蒸气蒸馏的原理用处和操作3学习并掌握固体有机化合物的…
-
20xx年非公有制经济组织党建工作情况总结
湖丰镇非公有制经济组织党建工作总结我镇按照“非公有制经济组织发展到哪里,党的组织就延伸到哪里,党的工作就做到哪里”的思路,开展了非…
-
20xx-20xx学年上学期学生会生活部工作总结
转眼间半年过去了,在这一学期的工作中,我部全体成员团结共勉,认真协作,不断发扬全心全意心服务同学,服务学校的宗旨,发扬创新意识,在…
-
镇党委中心组学习20xx年总结
**镇20xx年度党委中心组学习总结20xx年,**镇党委中心组加强理论学习的规范化、制度化建设,不断丰富学习内容,不断改进学习方…
-
C语言上机考试改错题分析总结
以下对改错题的改错方式做一些总结,当然这些总结只能对大部分改错行有效。1、若错误行是函数首部,可分为以下几种情况:A、该行最后若有…
-
分子生物学总结
09生物类专业分子生物学复习大纲第一章绪论1、早期主要由哪些实验证实DNA是遗传物质?这这些实验的主要论点证据?答:㈠美国微生物学…