报告发射光谱定性与定量分析
华南师范大学实验报告
学生姓名:杨秀琼 学号: 20082401129 专业: 化 学 年级班级:08化二 课程名称:仪器分析实验 实验项目:发射光谱定性分析 实验类型:综 合 实验时间:2010/4/8
发射光谱定性分析
一、【实验目的】
1.学习利用光谱图比较法进行光谱定性分析的操作方法。
2.学会使用摄谱仪和光谱投影仪以及谱片的显影和定影方法。 了解电感耦合等离子体原子发射光谱仪的使用方法。
二、【实验原理】
原子发射光谱分析法是根据受激发的物质所发射的光谱来判断其组成的一门技术。在室温下,物质中的原子处于基态(E0),当受外能(热能、电能等)作用时,
核外电子跃迁至较高的能级(En),即处于激发态,激发态原子是十分不稳定的,
其寿命大约为10s。当原子从高能级跃迁至低能级或基态时,多余的能量以辐射形式释放出来。其辐射能量与辐射波长之间的关系用爱因斯坦——普朗克公式表示:
△E=En-Ei=hc/λ (1)
式中,En、Ei为高能级和低能级的能量,h为普朗克常数,c为光速,λ为波
长。
谱线的波长:λ=c/v
由于各种元素的原子结构不同,故其发射光谱的谱线波长也各不相同,根据各元素的特征谱线,可判别相应元素存在与否。
一个元素可以有很多条谱线,其中最容易激发的谱线称为该元素的“灵敏线”或”“最后线"。如为确定试样中存在与否,不必检查该元素所有的谱线,只需要根据几条灵敏线的出现与否可作出判断。
光谱分析就是依据元素的特征光谱来鉴别元素的存在(定性分析),而谱线的强度与试样中该元素的含量有关,因此也可以利用谱线的强度来测定元素的含量-8
(定量分析)。当温度一定时,谱线强度与元素浓度之间的关系符合下列经验公式。
I=acb
LgI=blgc+lga
此公式称为赛伯-罗马金公式,是光谱定量分析的基本关系式。
三、【仪器与试剂】
仪器:IRIS INTREPID II高频电感耦合等离子直读光谱仪(美国热电公司) 试剂:氩气、 未知样品、钙、镁标准储备液(1mg/Ml),优级纯硝酸,水(二次蒸馏水)
四、【实验步骤】
1.定性分析
定性分析包括分析元素和分析谱线,通常全谱直读电感耦合等离子体发射光谱仪通过全谱谱图对样品中的元素进行更详细的了解,全谱谱图包含样品中所有元素的所有谱线。样品的所有信息都包括在两张全谱谱图中(uv和vis,以238nm为分界线),同股沟全谱谱图可以对未知样品进行定性分析,或证明某些元素的存在。
对于未知样品,首先点击“run”选择“fullframe”命令,获得样品的uv和vis全谱,然后点击观测到的某条强谱线,用谱线库对其进行鉴别,同样寻找该元素的其他二级谱线进行辅助证明。
如果要证明某元素的存在,全谱直读电感耦合等离子体发射光谱仪可以先建立一个含有待测元素的方法,选择所需元素和相应谱线,然后转变一份含有待测元素的溶液,它可以看是典型样品或合成样品,并运行全谱命令,得到的全谱谱图中就会将选定元素和谱线标记出来。如果在标记处有光标就可以证明该元素存在,反之亦然。
(1)未知样品的定性分析。按照仪器操作规程,设置仪器参数,点燃等离子体,运行光谱命令,25psi,蠕动泵转速,100r/min;溶液提升量,1.85ml/min。
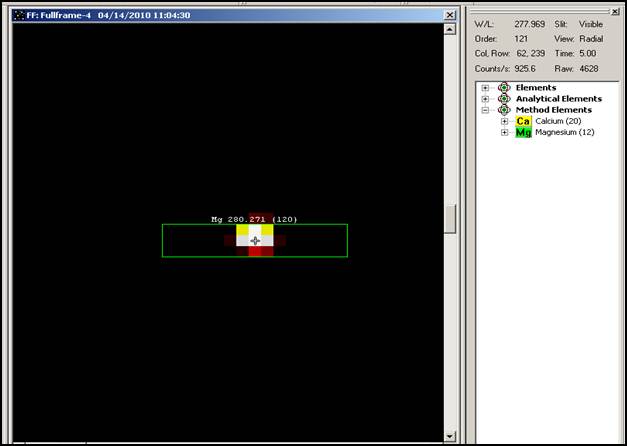
(2)证明自来水中Ca Mg元素的存在。设定含有待测元素的方法,选择Ca,Mg元素和相应的分析线,运行全谱命令,查看Ca,Mg元素特征谱线标记处是否有光斑,如果有证明存在该元素。
2、定量分析
测定自来水中Ca,Mg元素的含量,由于ICP-AES 具有较宽的线性范围,通常可以通过两点定线,一点是空白溶液,另外一点是高于待测元素含量的高标准溶液。 标准溶液的配制
Mg标准使用液的配置(100ug/ml)移取10mlMg标准储备液于100ml容量瓶中,用二次蒸馏水稀释至刻度,摇匀备用。
混合标准溶液的配置(Ca100ug/ML Mg5ug/ml)移取10mlCa贮备液,5mlMg标准使用液于100ml容量瓶中,用二次蒸馏水稀释至刻度,摇匀备用。
测定
暗中仪器操作规程设置测定条件
A.选择待测元素与分析线,
B、进行标准化,绘制标准曲线
C、直接测定自来熟中Ca,Mg含量(如果水的硬度较大,可以将自来水稀释后进样)
五、【实验数据以及实验结果】
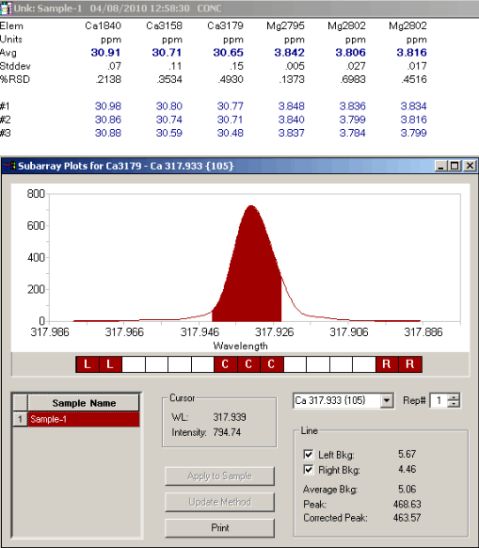

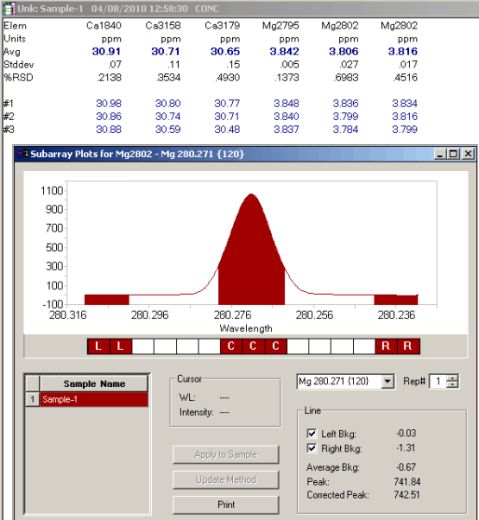
结论:Ca,Mg元素特征谱线标记处有光斑,如果有证明存在Ca,Mg元素。通过比较三条谱线的性噪比,得到最佳的谱线。在该最佳谱线下,进行定量分析。得出未知液中钙的浓度为30.65ug/ml,镁的浓度为3.806ug/ml。
六、【思考题】
1、比较原子发射光谱法与原子吸收光谱法
相同点:
(1) 检出限低,10-10~10-14 g;
(2) 准确度高
(3) 选择性高,
(4) 难熔元素、非金属元素测定困难
不同点:
A、原理不同:
原子发射光谱:是价电子受到电或热激发跃迁到激发态,激发态电子再由高能态回到各较低的能态或基态时,以辐射的形式放出其激发能,产生原子发射光谱; 原子吸收光谱:是基态原子吸收共振辐射跃迁到第一激发态,产生原子吸收光谱,它的产生是一个共振吸收过程;
B、光源不同
原子发射光源要求能量较高,而原子吸收光源要求能量相对较低。原子发射能同时测定70种元素,而原子吸收每次只能测定一个元素,测另一个元素时要相应换灯。
C、原子吸收法的选择性高,干扰较少且易于克服。
由于原于的吸收线比发射线的数目少得多,这样谱线重叠的几率小得 多。而且空心阴极灯一般并不发射那些邻近波长的辐射线经,因此其 它辐射线干扰较小。
D、原子吸收具有更高的灵敏度。
在原子吸收法的实验条件下,原子蒸气中基态原于数比激发态原子数 多得多,所以测定的是大部分原子。
E、原子吸收法比发射法具有更佳的信噪比
这是由于激发态原子数的温度系数显著大于基态原子。
适用范围:
(1)当需测定几种元素时,可以使用原子吸收法
(2)当需测定几十种元素时,使用原子发射法
2.标准曲线法的特点及适用范围
答:标准曲线法的特点:
优点是绘制好标准工作曲线后测定工作就变得相当简单,易标准化,可直接从标准工作曲线上读出含量;
缺点:
①、每次样品分析条件很难完全相同,因此容易出现较大误差
②、标准工作曲线绘制时,一般使用欲测组分的标准样品(或已知准确含量的样品),而实际样品的组成却千差万别,因此必将给测量带来一定的误差。
适用范围:大量样品且组成明确的样品分析。
3.如果试样成分复杂,应该怎样测定?
标准加入定量法。标准加入法适用于试样的基体组成复杂且对测定有明显干扰时,但在标准曲线呈线性关系的浓度范围内的样品。该方法能消除基体效应的影响,但不能消除背景吸收的影响,故应扣除背景值。具体操作:吸取试液四份以上,第一份不加待测元素标准溶液,第二份开始,依次按比例加入不同量待测组分标准溶液,用溶剂稀释至同一的体积,以空白为参比 ,在相同测量条件下,分别测量各份试液的吸光度,绘出工作曲线,并将它外推至浓度轴,则在浓度轴上的截距,即为未知浓度cX。
第二篇:原子发射光谱定性和定量分析
【实验题目】
原子发射光谱定性和定量分析
【实验目的】
1、掌握光谱定性分析的一般原理和方法。
2、掌握光谱定量分析的一般原理和方法。
3、了解电感耦合等离子体原子发射光谱仪的使用方法。
【实验原理】
但当原子受到能量(如热能、电能等)的作用时,原子由于与高速运动的气态粒子和电子相互碰撞而获得了能量,使原子中外层的电子从基态跃迁到激发态,处于激发态的原子是十分不稳定的,在极短的时间内便跃迁至基态或其它较低的能级上。当原子从较高能级跃迁到基态或其它较低的能级的过程中,将释放出多余的能量,这种能量是以一定波长的电磁波的形式辐射出去的,其辐射的能量可用下式表示:
△E=E2-E1=hv
谱线波长:
λ=c/v
每一种元素因其原子结构不同,受激发后都可以产生自己的特征光谱,每一种元素的特征光谱通常包含有很多谱线,谱线的强度各不相同。一个试样如含有若干种元素,谱线上就有这若干种元素的特征光谱,特征光谱的条数多少与各元素含量高低有关。当某元素含量降低时,其光谱中的弱线相继消失,而不被检出。最后消失的几条谱线叫“灵敏线”定性分析一般只需找出某元素的灵敏线即可确定该元素的存在。
光谱分析根据这些元素的特征光谱就可以准确无误的鉴别元素的存在(定性分析),而这些光谱线的强度又与试样中该元素的含量有关,因此又可利用这些谱线的强度来测定元素的含量(定量分析)。当温度一定时,光谱线的强度与试样中该元素的浓度之间的关系符合下列经验公式:
I=aCb
lgI=blgc+lga
【实验仪器与试剂】
(1) 仪器:
IRIS INTREPIDⅡ XSP 高频电感耦合等离子直读仪。
(2) 试剂:
氩气;未知样品;钙、镁保准储备液:100ug/mL;蒸馏水。
【实验内容与步骤】
1、定性分析
按仪器操作规程,设置仪器参数,点燃等离子体,运行全谱命令,对未知样品进行分析。
仪器主要参数:高频功率,1150W;冷却气流量,15L/min;辅助气流量,0.5L/min;载气压力,25psi;蠕动泵转速,120r/min;溶液提升量,1.85mL/min。
证明自来水中钙和镁元素的存在,选择测定方法,选择相应分析线,运行全谱命令,查看钙、镁特征谱线标记处是否有光斑,如果有证明有该元素存在。
2、定量分析
测定自来水中Ca、Mg元素含量,通常可以通过两点定线,一点是空白溶液,一点是高于待测元素含量的高标准溶液。
按照仪器操作规程设定测定条件:
a. 选择待测元素及分析线:Ca 315.933nm,Mg 279.079nm;
b. 进行标准化,绘制标准曲线;
c. 直接测定自来水中Ca、Mg的含量。
【实验数据记录与分析】

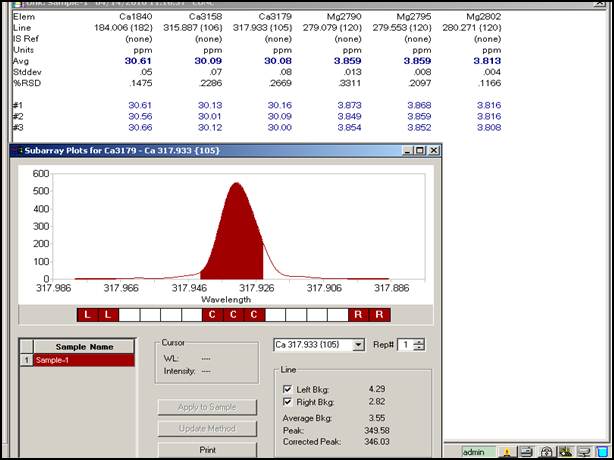
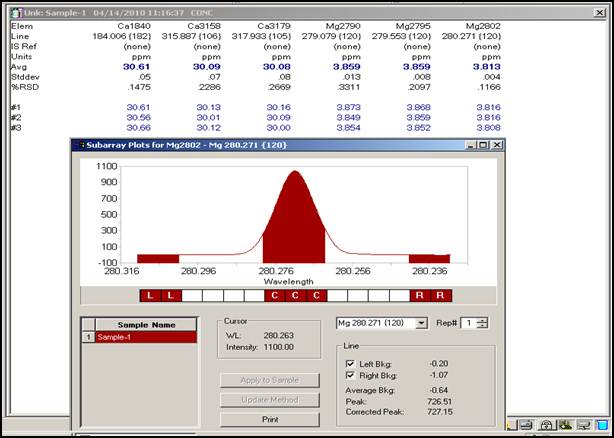
由上数据可知Ca在315.887nm时测定最优,多次测得浓度平均值为30.09ppm。Mg在280.271nm时测定最优,多次测得浓度平均值为3.813ppm。
-
光谱分析实验报告
仪器分析实验光谱分析实验一光谱分析食质检测20xx级02班钟凯成学号20xx5782一实验目的1了解主要光学仪器AASAFSV2S…
-
报告发射光谱定性与定量分析
华南师范大学实验报告学生姓名杨秀琼学号20xx2401129专业化学年级班级08化二课程名称仪器分析实验实验项目发射光谱定性分析实…
-
红外光谱分析实验报告
一实验题目红外光谱分析实验二实验目的1了解傅立叶变换红外光谱仪的基本构造及工作原理2掌握红外光谱分析的基础实验技术3学会用傅立叶变…
-
仪器分析实验一 紫外吸收光谱定性分析的应用
实验一紫外吸收光谱定性分析的应用一实验目的1掌握紫外吸收光谱的测绘方法2学会利用吸收光谱进行未知物鉴定的方法3学会杂质检出的方法二…
-
实验10 碳酸钙、聚乙烯醇、丙三醇、乙醇的红外光谱定性分析(罗娅君)
实验十碳酸钙聚乙烯醇丙三醇乙醇的红外光谱定性分析一实验目的1了解傅立叶变换红外光谱仪的基本构造及工作原理2掌握红外光谱分析的基础实…
-
光谱分析实验报告
仪器分析实验光谱分析实验一光谱分析食质检测20xx级02班钟凯成学号20xx5782一实验目的1了解主要光学仪器AASAFSV2S…
-
红外光谱分析实验报告
一实验题目红外光谱分析实验二实验目的1了解傅立叶变换红外光谱仪的基本构造及工作原理2掌握红外光谱分析的基础实验技术3学会用傅立叶变…
-
实验报告-物质的吸收光谱——分光光度法测定铁
实验报告一实验名称物质的吸收光谱分光光度法测定铁二实验目的1了解物质的分子吸收光谱及其测定方法初步了解比尔定理所反映的物质吸光度与…
-
仪器分析实验一 紫外吸收光谱定性分析的应用
实验一紫外吸收光谱定性分析的应用一实验目的1掌握紫外吸收光谱的测绘方法2学会利用吸收光谱进行未知物鉴定的方法3学会杂质检出的方法二…
-
实验10 碳酸钙、聚乙烯醇、丙三醇、乙醇的红外光谱定性分析(罗娅君)
实验十碳酸钙聚乙烯醇丙三醇乙醇的红外光谱定性分析一实验目的1了解傅立叶变换红外光谱仪的基本构造及工作原理2掌握红外光谱分析的基础实…
-
定性研究方法第二次讨论课读书报告
定性研究方法第二次讨论课读书报告丁倩如12级社会学1230027对于定型研究而言,搜集资料是一个非常重要的过程。研究者所搜集的资料…