乙酰水杨酸的制备
《有机化学》课程实验报告
姓名 学号 成绩
日期 2015.12.16 同组姓名 指导教师 戴箭
实验名称:乙酰水杨酸的制备
一、实验目的:
1、了解乙酰化反应。
2、掌握回流、抽滤及重结晶等操作技术。
二、仪器
干燥的大试管、带玻璃钉的玻璃漏斗、10mL吸滤瓶、温度计、2mL吸量管。
三、药品
水杨酸、乙酸酐、浓硫酸、95%乙醇、1%三氯化铁溶液。
四、实验原理
乙酰水杨酸又称阿司匹林,具有解热镇痛和抗风湿等作用,是一种常用药,可由水杨酸与酰化剂(乙酸酐或乙酰氯)发生酰化反应而得。为加快反应,常用浓硫酸或磷酸作催化剂。










粗产物中由于残留少量的副产物和未反应的原料,需要用乙醇-水混合溶剂进行重结晶,使之纯化。乙酰水杨酸的纯品为白色结晶,熔点为136~138℃,无臭,略带酸味,难溶于水,易溶于醇、醚和氯仿。
五、实验步骤及数据记录
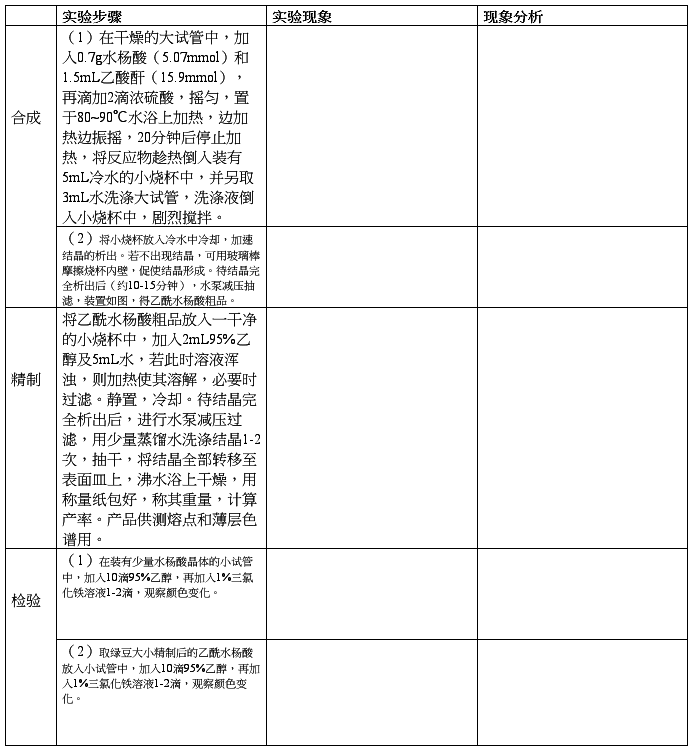
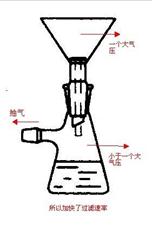
微型抽滤装置
六、注意事项:
七、实验结果讨论
八、思考题
第二篇:乙酰水杨酸的合成及表征
实验四 乙酰水杨酸的合成及检测
(4学时)
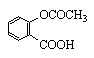 阿司匹林为解镇痛药,用于治疗伤风、感冒、头痛、发烧、神经痛、关节痛及风湿病等。近年来,又证明它具有抑制血小板凝聚的作用,其治疗范围又进一步扩大到预防血栓形成,治疗心血管疾患。阿司匹林化学名为2-乙酰氧基苯甲酸,化学结构式为:
阿司匹林为解镇痛药,用于治疗伤风、感冒、头痛、发烧、神经痛、关节痛及风湿病等。近年来,又证明它具有抑制血小板凝聚的作用,其治疗范围又进一步扩大到预防血栓形成,治疗心血管疾患。阿司匹林化学名为2-乙酰氧基苯甲酸,化学结构式为:
阿司匹林为白色针状或板状结晶,mp.135~140℃,易溶乙醇,可溶于氯仿、乙醚,微溶于水。合成路线如下:
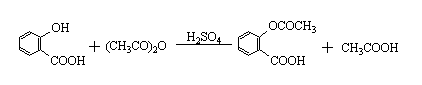
一、实验目的
1.了解酯类的合成方法,熟悉酰化反应的原理和实验操作;
2.掌握有机化合物的纯化机理和基本操作,掌握其纯度的检测方法;
3.了解工业化生产与实验室小试工艺间的区别与联系;
二、实验原理
1、合成:原料水杨酸是双官能团化合物,它即是酚又是芳香族羧酸,因此它能进行两种不同的酯化反应。既可与甲醇反应生成水杨酸甲酯(即冬青油),又可与乙酸酐作用,使水杨酸分子中酚羟基上的氢原子被乙酰基取代,从而得到乙酰水杨酸。
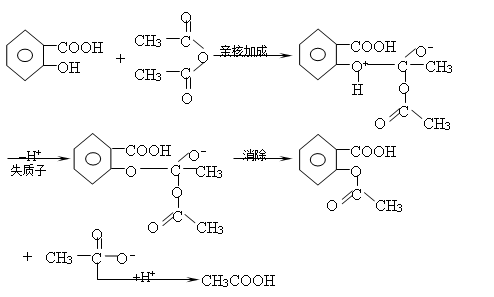 本实验采用将水杨酸和乙酸酐,在少量浓硫酸催化作用下,通过破坏水杨酸分子中羧基与酚羟基间形成的氢键,从而使得乙酰化反应容易完成,其机理式:
本实验采用将水杨酸和乙酸酐,在少量浓硫酸催化作用下,通过破坏水杨酸分子中羧基与酚羟基间形成的氢键,从而使得乙酰化反应容易完成,其机理式:
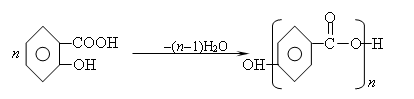 2、纯化:由于水杨酸的苯环上既有羟基又有羧基,在反应过程中会形成一种高聚物副产物:
2、纯化:由于水杨酸的苯环上既有羟基又有羧基,在反应过程中会形成一种高聚物副产物:
可以利用乙酰水杨酸与NaHCO3反应生成水溶性的钠盐,而高聚物不溶于NaHCO3溶液的原理,通过过滤将高聚物分离出去。然后再用酸将乙酰水杨酸沉淀出来,从而达到纯化产品的目的,其反应式如下:
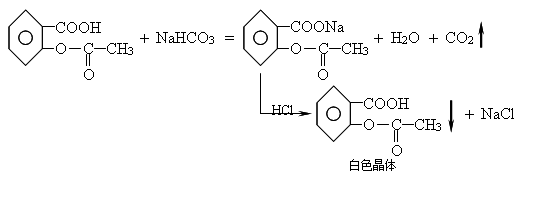
3、重结晶:在最终产物中最有可能产生的杂质是水杨酸本身,这是由于乙酰化反应不完全或是产物在分离步骤中发生水解造成的。因此还可以用乙醇、丙酮或乙酸乙酯对最终产物进行重结晶,从而得到纯度更高的产品——阿司匹林。
由于阿司匹林的生产是一个成熟的工艺,将它与实验室制备作对比,从而了解化工产品的工业生产与实验室制备的联系与区别。
三、实验预习题
1.酰化反应的条件是什么?
2.浓硫酸在反应中的作用是什么?能否用稀硫酸代替?
3.本实验中所用的水杨酸和玻璃仪器必需是干燥的,为什么?
4、本实验中可产生什么副产物?
四、实验设备、仪器、试剂
1.设备、仪器:旋转蒸发仪、循环水泵、电子天平、干躁箱,显微熔点仪、红外、布氏漏斗及抽滤装置;100ml锥型烧瓶、10-50 ml量筒、250ml烧杯、100℃温度计等;
2.试剂: 水杨酸、乙酸酐、硫酸,碳酸氢钠、盐酸、95%乙醇、1%三氯化铁,丙酮或乙酸乙酯等;
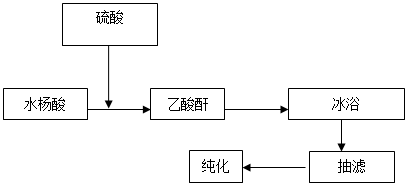 五、实验制备流程
五、实验制备流程
六、实验内容及操作步骤
1.乙酰水杨酸的合成:
1) 酯化:称量2g水杨酸(0.045mol)放入干燥的锥形瓶中,慢慢加入5ml乙酐(5.4g 0.053mol),并滴加5~6滴浓硫酸,轻轻摇荡锥形瓶使溶解,在80~85℃水浴中加热约15min,从水浴中移出锥形瓶,当内容物温热时慢慢滴入3~5mL冰水,此时反应放热,甚至沸腾。反应平稳后,再加入40~50mL水,用冰水浴冷却,并用玻棒不停搅拌,使结晶完全析出,若无晶体或出现油状物,可用玻棒(在冰水浴中)摩擦内壁以助沉淀,抽滤,用少量冰水洗涤两次,得阿斯匹林粗产物。
2) 纯化: 将阿斯匹林的粗产物移至烧杯中,加入25mL饱和NaHCO3溶液搅拌,直至无CO2气泡产生,抽滤,用少量水洗涤,保留将洗涤液与滤液,弃去滤渣(此滤渣为何物?)。
3) 首先在烧杯中放大约5mL浓盐酸并加入l0mL水,摇匀此盐酸水溶液,再将步骤(2)的滤液倒入此烧杯中,阿斯匹林随即重复沉淀析出;再用冰水冷却令结晶完全析出,抽滤,冷水洗涤,压干滤饼,自然晾干为佳。(产率约80%,熔点134~136°C )
4) *重结晶:此内容供同学选做,选做的同学须在预习报告中提出并写清实验方法;(提供的试剂为95%乙醇或丙酮)
2.乙酰水杨酸纯度的检测与测定:
由于水杨酸的酚羟基可与FeCl3稀试剂呈现颜色反应,产生Fe(II)—酚深紫色络合物,所以可用1%FeCl3溶液来定性检验产品的纯度。
1) 检验:
将少量(少于 0.05g)的水杨酸放入试管A,再将少量产品放入试管B内,然后在A、B试管里各加入1ml左右的乙醇使其溶解,再在各试管里滴加几滴1%FeCl3水溶液,观察和记录颜色变化,鉴定产品纯度;(可在合成与纯化后,各做一次检验,进行比较)
2) 熔点的测定*(略)
3) 产品的红外表征*(略)
注:由于课时所限,凡标注*号的内容不做。
七、实验数据记录及处理表

八、实验思考题
1、为什么使用新蒸馏的乙酸酐?加入浓硫酸的目的是什么?
2、乙酰水杨酸还可以使用溶剂进行重结晶?重结晶时需要注意什么?
3、通过什么样的简便方法可以鉴定出阿斯匹林是否变质?
4、若在硫酸的存在下,水杨酸于乙醇作用将得到什么产物?写出反应方程式。
5、本实验是否可以使用乙酸代替乙酸酐?
一、实验预习报告
(要求:①简述实验目的和原理;②简述实验内容及步骤、仪器设备及试剂的名称;③简述实验装置或流程;④了解注意事项,回答预习题)
二、实验记录与数据处理
(要求:根据化学反应方程式,计算理论产量,并与实际产量对比分析误差原因;写出计算过程,将实验记录与处理的结果填于表内)
三、实验讨论
(①分析误差原因,回答思考题;②试着从理论上解释现象,讨论你想讨论的问题;③阿司匹林的生产是一个成熟的工艺,与实验室制备相比较,了解化工产品的工业生产与实验室制备的联系与区别,阐述自己的观点)
-
乙酰水杨酸的制备实验报告
一实验目的1通过本实验了解乙酰水杨酸阿斯匹林的制备原理和方法2进一步熟悉重结晶熔点测定抽滤等基本操作3了解乙酰水杨酸的应用价值二实…
-
乙酰水杨酸的制备实验报告
乙酰水杨酸阿司匹林的合成实验报告一教学要求1通过本实验了解乙酰水杨酸阿斯匹林的制备原理和方法2进一步熟悉重结晶熔点测定抽滤等基本操…
-
乙酰水杨酸的制备的预习实验报告
乙酰水杨酸的制备一实验目的1了解和熟悉乙酰水杨酸的基本方法2巩固抽滤的技术操作二实验原理乙酰水杨酸又名阿司匹林aspirinCAS…
-
实验1 乙酰水杨酸的合成实验报告
实验1乙酰水杨酸的合成实验目的掌握由酸酐作为酰基化试剂和醇反应制备酯的方法巩固普通蒸馏抽滤重结晶等基本操作学习应用显微镜熔点仪测定…
-
乙酰水杨酸的制备实验报告[1]
乙酰水杨酸阿司匹林的合成实验报告一教学要求1通过本实验了解乙酰水杨酸阿斯匹林的制备原理和方法2进一步熟悉重结晶熔点测定抽滤等基本操…
-
乙酰水杨酸片的制备-_戎欣玉
乙酰水杨酸片的制备一实验目的掌握湿法制粒压片的一般工艺单冲压片机的使用方法及片剂质量的检查方法通过本实验使学生对工业药剂学药物分析…
-
乙酰水杨酸的制备实验报告
乙酰水杨酸阿司匹林的合成实验报告一教学要求1通过本实验了解乙酰水杨酸阿斯匹林的制备原理和方法2进一步熟悉重结晶熔点测定抽滤等基本操…
-
实验1 乙酰水杨酸的合成实验报告
实验1乙酰水杨酸的合成实验目的掌握由酸酐作为酰基化试剂和醇反应制备酯的方法巩固普通蒸馏抽滤重结晶等基本操作学习应用显微镜熔点仪测定…
-
乙酰水杨酸的制备的预习实验报告
乙酰水杨酸的制备一实验目的1了解和熟悉乙酰水杨酸的基本方法2巩固抽滤的技术操作二实验原理乙酰水杨酸又名阿司匹林aspirinCAS…
-
乙酰水杨酸实验预习报告
乙酰水杨酸有机化学实验报告实验项目名称乙酰水杨酸的制备一实验目的1了解和熟悉乙酰水杨酸的基本方法2巩固抽滤的操作技术二实验基本原理…