紫外光谱测氨基酸类物质实验报告
氨基酸类物质的紫外光谱分析和定量测定实验报告
一、实验目的
(1)掌握紫外–可见分光光度计的工作原理与基本操作。
(2)学习紫外–可见吸收光谱的绘制及定量测定方法。
(3)了解氨基酸类物质的紫外吸收光谱的特点。
二、实验原理
紫外-可见分光光度法属于吸收光谱法,分子中的电子总是处在某一种运动状态中,每一种状态都具有一定的能量,属于一定的能级。电子由于受到光、热、电等的激发,从一个能级转移到另一个能级,称为跃迁。当这些电子吸收了外来辐射的能量,就从一个能量较低的能级跃迁到另一个能量较高的能级。物质对不同波长的光线具有不同的吸收能力,如果改变通过某一吸收物质的入射光的波长,并纪录该物质在每一波长处的吸光度(A),然后以波长为横坐标,以吸光度为纵坐标作图,这样得到的谱图为该物质的吸收光谱或吸收曲线。
当一定波长的光通过某物质的溶液时,入射光强度I0与透过光强度It之比的对数与该物质的浓度c及厚度b成正比。其数学表达式为:
 (一)
(一)
式(一)为Lambert-Beer定律,是分光光度法定量分析的基础,其中T为透光率(透射比)。
物质的吸收光谱反映了它在不同的光谱区域内吸收能力的分布情况,不同的物质,由于分子结构不同,吸收光谱也不同,可以从波形、波峰的强度、位置及其数目反映出来,因此,吸收光谱带有分子结构与组成的信息。
氨基酸类物质的一个重要光学性质是对光有吸收作用。20种氨基酸在可见光区域均无光吸收,在远紫外区(<220 nm)均有光吸收,在紫外区(近紫外区)(220 nm—300 nm)只有三种AA有光吸收能力,这三种氨基酸分别是苯丙氨酸、酪氨酸、色氨酸,因为它们的结构均含有含有苯环共轭双键系统。苯丙氨酸最大吸收波长在259 nm、酪氨酸在278 nm、色氨酸在279 nm,蛋白质一般都含有这三种氨基酸残基,所以其最大光吸收在大约280 nm波长处,因此能利用分光光度法很方便的测定蛋白质的含量。
本实验将对苯丙氨酸、酪氨酸和色氨酸三种氨基酸进行光谱测定及相关定量测定。
三、仪器和试剂
1 仪器
紫外-可见-近红外分光光度计(UV-3600或UV-2401);分析天平; 0.5 mL、1.0 mL、2.0 mL移液管若干;10 mL带塞比色管若干。
2 试剂
标准溶液(a): 2.0 g/L的苯丙氨酸溶液;
标准溶液(b):0.4 g/L的酪氨酸溶液;
标准溶液(c):0.4 g/L的酪氨酸溶液(所有溶液均用去离子水配制);酪氨酸待测样。
四、实验步骤
(1)分别移取标准溶液(a)(2.0 g/L,1.0 mL)、标准溶液(b)(0.4 g/L,1 mL)和标准溶液(c)(0.4 g/L,0.4 mL)标准溶液于10 mL比色管中,用去离子水稀释、定容、摇匀,待用。
(2)分别移取0.00、0.5、1.0、1.5、2.0 mL标准溶液(b)于5个10 mL比色管中,并用去离子水稀释、定容,摇匀,待用。
(3)双击分光光度计图标“UVProbe”,出现软件界面,点左下角“连接”,系统开始自检,等系统自检结束。预热15-30分钟。待仪器稳定后方可使用。
(4)在光谱测量模式下,以去离子水为参比溶液,分别绘制步骤(1)中各溶液在200~350nm波长范围内的吸收光谱。并记录各标准溶液的λmax 。
(5)在定量测定模式下,以去离子水为参比溶液,测定步骤(2)中的各标准溶液在λmax处的吸光度。
(6)在步骤5同样条件下,测定未知样品溶液在λmax处的吸光度。
五、数据处理与分析
1、将苯丙氨酸、酪氨酸和色氨酸溶液的吸收光谱叠加在一个坐标系中如下:
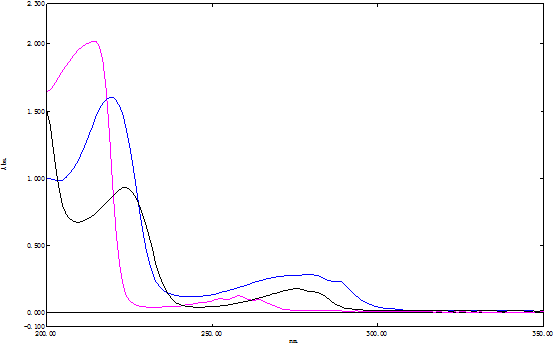
由图中可以看出,苯丙氨酸的最大吸收波长为257.73nm;色氨酸为278.70nm;酪氨酸为275.15nm。
2.对酪氨酸和色氨酸的光谱图作1-4阶导数分别如下:
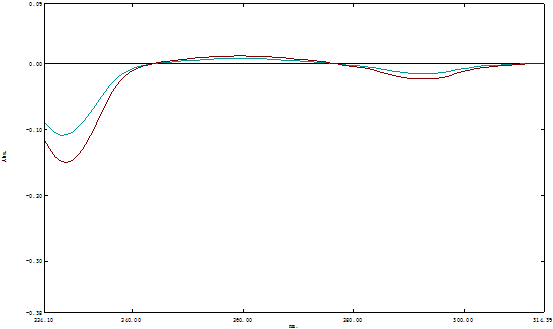
一阶导数
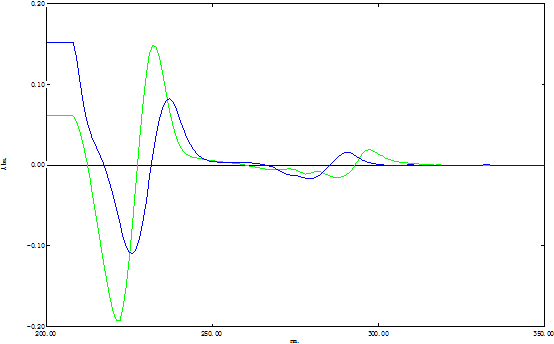
二阶导数
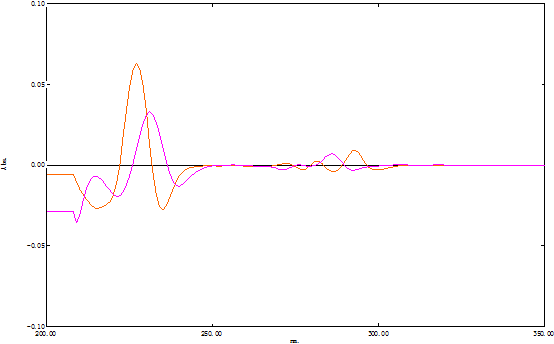
三阶导数
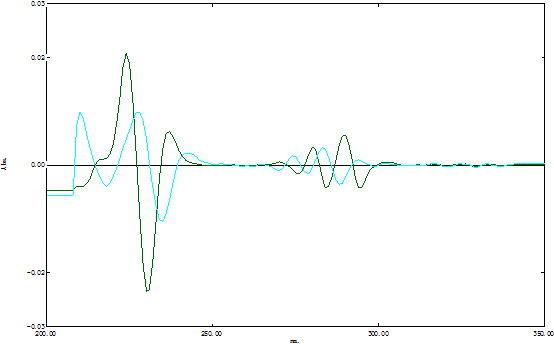
四阶导数
通过观察可知四阶导数光谱在 230.49nm处色氨酸与酪氨酸分离最完全,故选取四阶导数处理标准液和未知样品。
3.将标准液的光谱图分别做四阶导数曲线如下:
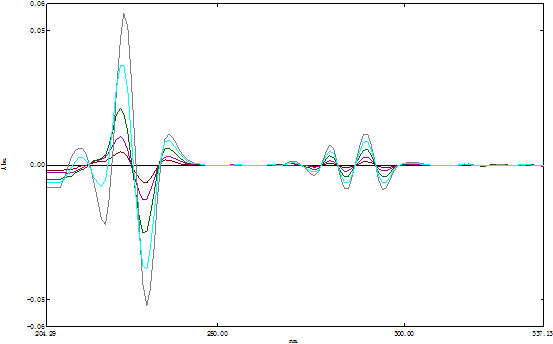
4.将未知样的光谱图做四阶导数曲线如下:
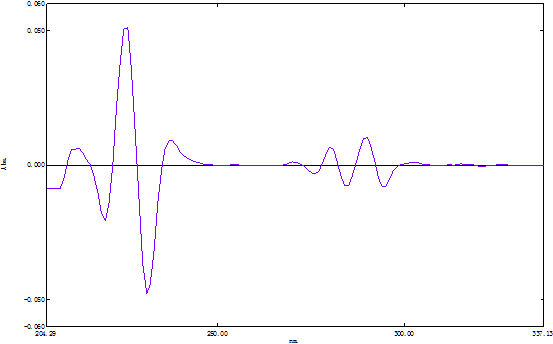
由图知未知样在230.49nm处的吸光度为-0.048.
5.将以上述步骤测得的各标准酪氨酸溶液的吸光度为纵坐标,相应的浓度为横坐标绘制工作曲线如下:

所得直线拟合方程为:Y=5×10-4-0.0026X.
6.将未知样的吸光度(-0.048)代入得到的标准工作曲线方程,解得未知样中色氨酸的浓度为:18.654mg/L.
六、思考题
(1)本实验是采用紫外吸收光谱中最大吸收波长进行测定的,是否可以在波长较短的吸收峰下进行定量测定,为什么?
答:最大吸收处信号强度较大,误差较小,如果在较小的吸收峰下进行测定,峰值易受其它因素影响,而且读数误差较大,不是很合适。
(2)被测物浓度过大或过小对测量有何影响?应如何调整?调整的依据是什么?
答:浓度过大导致信号过大,在实际的测量中可能超出实验范围;而浓度过小可能会导致吸收峰不明显,给实验和计算带来较大误差。在实际实验中,应挑选在线性范围内的浓度相对平均合适的几个点进行测量,保证实验的准确性。
(3)思考紫外-可见分光光度法应用于蛋白质测量的依据,并设计相应的实验方案,测定奶粉中蛋白质的含量。
答:蛋白质分子中所含酪氨酸、色氨酸及苯丙氨酸的芳香环结构对紫外光有吸收作用。色氨酸的吸收最强,但由于一般蛋白质中酪氨酸的含量比色氨酸高许多,因此这一吸收可认为主要是由酪氨酸提供的。其最大值在280nm附近,不同的蛋白质吸收波长略有差别。在无其他干扰物质存在的条件下,280nm的吸光度即可作蛋白质的测定用,但不同种的蛋白质对280nm波长的光吸收强度因芳香性氨基酸残基含量的不同而有差异。实验可以根据朗博比尔定律,利用配置一定浓度的标准溶液进行对照,做出标准工作曲线,再对未知样品进行测定。
第二篇:紫外光谱实验报告
紫外-可见吸收光谱实验报告
一、实验目的
学习测定有机化合物或生物大分子的测定方法;掌握分光光度计的基本操作及数据处理方法。
二、实验内容
用双光路紫外分光光度计测量已知化合物在某未知浓度时的吸光度,同时,根据实验数据用origin做出紫外光谱图,并根据朗伯-比尔 (Lamber-Beer)定律,计算所测物质的浓度。
三、实验仪器及试剂:
UV2550紫外-可见分光光度仪;
本组所测溶剂为苯甲酸。
四、实验原理
根据朗伯-比耳 (Lamber-Beer)定律:A=εbc,通过紫外分光光度计测量出最大吸收峰A,而b与ε已知,故可求得苯甲酸的浓度。
五、实验结果与讨论
1、根据图一可知,苯甲酸在λ=226nm处有最大吸收峰,此时,A=0.77525;
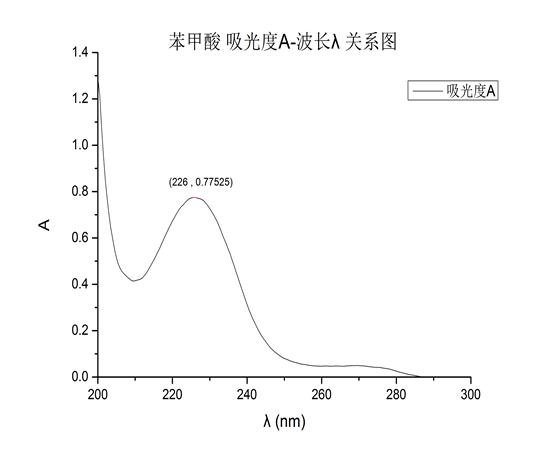
苯甲酸吸光度与波长关系图(图一)
2、苯甲酸在λ=226nm时的摩尔吸光系数ε=1000L/(mol·cm);
3、已知b=1cm,因此,根据据朗伯-比尔 (Lamber-Beer)定律,可求得苯甲酸的浓度c=7.75*10-4mol/L。
-
紫外吸收光谱实验报告
利用紫外吸收光谱检查物质纯度紫外-可见分光光度法测定水中苯酚含量一、实验目的1.学会使用Cary50型紫外-可见分光光度计2.掌握…
-
紫外光谱实验报告
紫外吸收光谱分析的应用实验报告班级环科10姓名王强学号20xx012127一实验目的1掌握紫外吸收光谱仪的使用方法2学会利用紫外光…
-
1紫外可见光谱实验报告
紫外可见光谱实验报告一、实验目的1、学会使用UV-2550型紫外-可见光分光光度计。2、掌握紫外可见分光光度计的定量分析方法。3、…
-
实验1紫外-可见吸收光谱实验报告
实验一紫外可见吸收光谱一实验目的1熟悉和掌握紫外可见吸收光谱的使用方法2用紫外可见吸收光谱测定某一位置样品浓度3定性判断和分析溶液…
-
实验1、紫外可见光谱实验报告
一实验目的1学会使用UV2550型紫外可见光分光光度计2掌握紫外可见分光光度计的定量分析方法3学会利用紫外可见光谱技术进行有机化合…
- 氨基酸的薄层层析实验报告
-
生物化学实验-氨基酸分析实验报告
实验报告第一部分预习报告内容实验原理实验材料包括实验样品主要试剂主要仪器与器材实验步骤包括实验流程操作步骤和注意事项评分满分30分…
-
氨基酸分析实验报告
生物化学实验报告姓名学号专业年级组别生物化学与分子生物学实验教学中心实验名称氨基酸的薄层层析实验日期20xx1022合作者评分实验…
-
实验六 氨基酸的纸层析法
氨基酸的纸层析法一.目的了解并掌握氨基酸纸层析的原理和方法。二、原理以滤纸为支持物的层析法,称为纸层析法。纸层析所用展层剂大多由水…
-
生物化学实验二 ——纸层析法分离氨基酸
生命学院生物化学实验实验二氨基酸的分离鉴定纸层析法一实验目的1掌握氨基酸纸层析的方法和原理学会分析待测样品的氨基酸成分2学习用纸层…
-
氢原子光谱实验报告_-_完成版
南京理工大学大学生物理实验研究论文氢原子光谱中文摘要本实验用三棱镜对汞原子光谱进行测量得出定标曲线再对氢原子光谱进行测量测得了氢原…