肉桂酸的合成
肉桂酸的合成
摘要::采用醋酸铵为催化剂,在无溶剂微波辐射下以苯甲醛和丙二酸为原料发生Knoevenagel缩合 反应,合成肉桂酸,测定了产物的熔点;同时对微波加速反应的机理进行了探讨。结果表明,该方法不但化学选择性好、反应时间短(3-6min)、产率高,而且产物易处理,对环境污染小。
关键词:醋酸铵;苯甲醛;丙二酸;Knoevenagel 缩合;微波辐射;无溶剂反应;肉桂酸
肉桂酸又名桂皮酸,是一种重要的有机合成中间体。广泛用于医药、香料、农药、塑 料和感光树脂等精细化工生产。在医药行业,肉桂酸用作冠心病人用药心可安的中间体,还可用于制造局部麻醉剂、杀菌剂、抗癌、抗炎、抗传染、血管扩张剂、止血药、止痛药和低血糖药等的制备;在香料行业,肉桂酸是羧酸类香料,有良好的保香作用,主要用于配制樱桃、杏、蜂蜜等型香料;在日化行业,肉桂酸用于配制香皂和日用化妆品用香精,由于其沸点较分子质量相近的其它有机物高,因此常被作为香料中的定香剂使用;在农药行业,肉桂酸可用于植物生长促进剂、长效杀菌剂、果蔬保鲜防腐剂和除草剂的制备。可见,肉桂酸及其衍生物具有广泛的用途, 其市场前景十分看好。
[1] 近来,随着人们对环境因素重视的提高 ,无溶剂有机反应引起了人们极大的兴趣
Knoevenagel 缩合反应作为一个重要的碳—碳键生成反应已经得到了人们广泛的研究。该反应通常是以碱或路易斯酸作为催化剂来进行的醛和丙二酸之间的Knoevenagel 反应在干介质中以ZnCl2、硅胶和醋酸胺- 碱性氧化铝为催化剂的反应。[2] 本实验采用微彼辐射技术,在无溶剂条件下,用价廉无毒无污染的醋酸铵作催化剂催化
Knoevenagel 反应,安全、高效、快速以及无污染地合成了肉桂酸。其反应方程式为:
1 实验部分
1.1 主要仪器和试剂 微波化学实验仪(微波功率可由外接调压器连续调节,上面有孔,可接冷凝管)、熔点测定仪、锥形瓶(有瓶塞)、冷凝管、布氏漏斗、玻璃棒、表面皿、电子秤 苯甲醛、丙二酸、醋酸铵
1.2 肉桂酸的制备 在50mL锥形瓶中2.8g(0.026mol)苯甲醛、一定比例的丙二酸和醋酸铵,摇匀后放进微波炉,装上回流冷凝管。火力键置“高火”,调节电流控制一定功率(由电表电流可查功率校准曲线,确定微波输出功率),微波辐射数分钟,(本反应640W时,辐射6min,产率最高,达84.5%),反应混合物完全熔融成液体并有CO2气体放出。稍冷,取出锥瓶,加入约50mL

冷水,产物即变为固体,将固体产
物搅碎,抽滤,用水充分浸润、洗涤两次,抽干后,干燥即得较纯的浅黄色产物肉桂酸。用含水乙醇(水/乙醇=1/3体积比)重结晶,得白色针状结晶性粉末,熔点为132~133℃。
2 实验结果与讨论
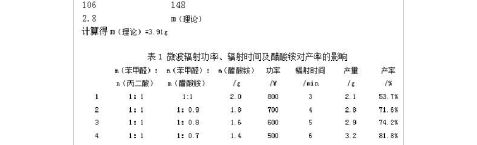
2.1 实验结果 由肉桂酸的制备反应方程式,得
由表1表明微波辐射功率、辐射时间对肉桂酸的产率产生一定的影响,且当微波辐射功 率在500-600W、辐射时间在5-6min时,产率较高。醋酸铵只需少量就有较高催化活性,所以在此实验中醋酸铵的量对产率影响不大。
2.2 如何提纯肉桂酸 用水蒸气馏蒸馏除去未反应的原料,酸化抽滤得到粗产品,用有机溶剂进行重结晶。 具体操作:待反应物冷却后,往瓶内加入20mL热水,以溶解瓶内固体,同时改装成水蒸气蒸馏装置,开始水蒸气蒸馏,至无白色液体蒸出为止,将蒸馏瓶冷却至室温,加入10%NaOH(约10mL)以保证所有的肉桂酸成钠盐而溶解。待白色晶体溶解后,滤去不溶物,滤液中加入0.2g活性炭,煮沸5分钟左右,脱色后抽滤,滤出活性炭,冷却至室温,倒入250mL烧杯中,搅拌下加入浓HCl,酸化至刚果红试纸变蓝色。冷却抽滤得到白色晶体,粗产品置于250mL烧杯中,用水-乙醇重结晶,先加60mL水,等大部分固体溶解后,稍冷,加入10mL无水乙醇,加热至全部固体溶解后,冷却,白色晶体析出,抽滤,产品空气中晾干后,称重。
2.3 如何检测肉桂酸的纯度 熔点测定。将样品研成细末,放入干燥的一端封口的毛细管中,取一高约80cm的干燥的玻璃管,直立于台面上,将装有样品的毛细管头落10次直至毛细管内样品紧缩为2~3mm高。放入熔点测定仪进行观察,记录熔程,然后利用熔程初步判断其含量。

3 结论 由于本次实验条件及各种因素的限制,只做了4组实验。因此采用无溶剂微波促进Knoevenagel缩合反应合成肉桂酸法仍需进行更深层次的实验,本实验只能算是一小部分。虽然本实验次数不多,但也从表1得出初步结论,微波辐射功率在500-600W、辐射时间在5-6min时,产率较高。催化剂醋酸铵的量仍需进一步实验。 无溶剂微波促进Knoevenagel缩合反应合成肉桂酸法使得在制备过程中降低了反应温度,提高了收率和产物纯度,简化了合成工艺。更好的以绿色化学的宗旨发展药物的作用。
参考文献 [1] 梁克中.肉桂酸合成实验的改进[A]. 林产化工通讯. 2004 年第38卷第2 期,21-22 [2] 王官武,王宝亮. 微波辐射和加热条件下的无催化剂无溶剂
Knoevenagel缩合反应[J]. 有机化学,2004,24(1):85~87
第二篇:PerKin法制备肉桂酸实验条件的优化
目录
摘要... i
Abstract ii
1文献综述... 3
1.1肉硅酸的用途... 3
1.1.1. 香精香料中的应用... 3
1.1.2. 食品添加剂的应用... 3
1.1.3. 药物合成中发展... 3
1.1.4. 美容方面的应用... 4
1.1.5. 保鲜剂方面的应用... 4
1.2 肉桂酸的合成方法... 4
2论文设计思路及实验方案... 6
2.1设计思路... 6
2.2实验方案... 6
3实验部分... 7
3.1化学试剂及仪器... 7
3.1.1主要试剂... 7
3.1.2 仪器设备... 7
3.2实验条件优化... 7
3.2.1 实验方法... 7
3.2.2 催化剂对产率的影响... 8
3.2.3 薄层色谱法(TLC)跟踪反应... 9
4结果与讨论... 11
参考文献... 13
致谢... 14
摘要
肉桂酸的Perkin法制备中不同催化剂、催化剂的用量及反应时间等对肉桂酸产率有较大的影响。论文主要从不同催化剂对肉桂酸产率的影响和薄层色谱(TLC)来跟踪反应时间等方面进行研究。实验结果表明: Perkin法制备肉桂酸的最佳工艺条件是用4.4g质量比1∶2的碳酸钾和醋酸钾混合碱作催化剂产率较高;运用薄层色谱(TLC)来跟踪其反应最佳时间是50min。
关键词:肉桂酸 催化剂 Perkin法 TLC
Abstract
Perkin cinnamic acid prepared by different catalysts, catalyst dosage and reaction time on the yield of cinnamic acid have greater impact. Thesis from different catalysts the yield of cinnamic acid and thin layer chromatography (TLC) to track the response time of aspects. The results show that: Perkin acid prepared the optimum conditions for the mass ratio of 1:2 with 4.4g of potassium carbonate and potassium acetate mixed alkali as a catalyst with high yield; the use of thin-layer chromatography (TLC) to track the response most Best time is 50min.
Key words: cinnamic acid; catalyst; perkin law;TLC
1文献综述
1.1肉硅酸的用途
肉桂酸又名桂皮酸,化学名称:β-苯丙烯酸,英文名:Cinnamic Acid,分子式为C6H5-CH=CH-COOH,相对分子量148.17,白色单斜棱晶,微有桂皮香气。熔点135℃,溶于乙醇、甲醇、石油醚、氯仿,易溶于苯、乙醚、丙酮、冰醋酸、二硫化碳及油类,不溶于水。肉桂酸是一种重要的有机合成原料,主要用于医药、农药、香料、感光树脂和塑料等精细化工产品的制备[1-2] 。目前肉桂酸在日本、美国、加拿大、德国、西班牙、意大利、巴西等世界各国和地区被广泛用于香料、食品、医疗、化工、饲料、粮食等领域[3];国内肉桂酸的市场需求量会日益扩大。其中应用最为广泛的有以下几点:
1.1.1 香精香料中的应用[4]
(1)调制苹果、樱桃,可作为苹果香精、樱桃香精、花香香精调和使用。
(2)可作为芳香混合物,用于香皂、洗衣粉、日用化妆品中。
(4)肉桂酸本身就是一种香料,具有很好的保香作用,通常作为配香原料,
肉桂酸的各种酯(如甲、乙、丙、丁等)都可用作定香剂,用于饮料、冷饮、糖果、酒类等食品。
1.1.2 食品添加剂的应用[5]
(1)以肉桂酸为原料,用微生物酶法合成L-苯丙氨酸。L-苯丙氨酸是重要的
食品添加剂——甜味阿斯巴甜(Aspartame)的主要原料。
(2)肉桂酸还是辣椒素合成酶的一个组成部分——肉桂酸水解酶,可以利用转基因培育具有高产辣椒素含量的辣椒优良品种,必将大大提高辣椒品质,从而有力推动辣椒产业化发展。
(3)利用肉桂酸的防霉防腐杀菌的功能,可应用于粮食、蔬菜、水果中的保鲜、防腐。
(4)还可用在葡萄酒中,使其色泽光鲜。
(5)肉桂酸具有很强的兴奋作用,可直接添加于食品中。
1.1.3 药物合成中发展[6-7]
医药工业中,可用于合成治疗冠心病的重要药物乳酸可心定和心痛平,及合成氯苯氨丁酸和肉桂苯哌嗪,用来制造“心可安”、局部麻醉剂、杀菌剂、止血药等。还可合成氯苯氨丁酸和肉桂苯哌嗪,用作脊锥骨骼松弛剂和镇痉剂。主要用于脑血栓,脑动脉硬化,冠状动脉硬化等病症。对肺腺癌细胞增殖有明显抑制作用。
1.1.4 美容方面的应用
肉桂酸可应用于美容方面,酪氨基酸酶是黑色素合成关键酶,它启动了由酪氨酸转化为黑色素生物聚合体的级链反应,肉桂酸有抑制形成黑色酪氨酸酶的作用,对紫外线有一定的隔绝作用,能使褐斑变浅,甚至消失,是高级防晒霜中必不可少的成分之一。肉桂酸显著的抗氧化功效对于减慢皱纹的出现有很好的疗效。
1.1.5 保鲜剂方面的应用[8]
保鲜剂方面,我国每年因加工储存不善导致的粮食损失高达25%,水果蔬菜流通消费中的损失更是高达30-40%,因此要求有高效的防腐保鲜剂以储存和保鲜农产品。肉桂酸作为水果蔬菜的防腐鲜剂必将有广阔的市场发展空间。
1.2 肉桂酸的合成方法
目前,肉桂酸制备方法有Perkin(柏琴)法、苯乙烯-四氯化碳法、苯甲醛-丙酮法、苯甲醛-乙烯酮法及苯乙烯—一氧化碳法[9]等。
(1)Perkin法是芳香醛和酸酐在相同羧酸的碱金属盐存在下,发生类似醛醇缩合反应得到α,β-不饱和芳香酸,这个反应用于合成肉桂酸及其同系物,称为铂金醇醛缩合反应[10-11]。Perkin法合成肉桂酸,是以苯甲醛与乙酸酐为原料, 在弱碱作用下,乙酸酐的α-H被夺去,生成碳负离子, 进而进攻苯甲醛,最后生成肉桂酸,其合成路线为:
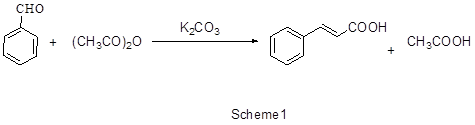
(2)苯乙烯-四氯化碳法:苯乙烯-四氯化碳法是以苯乙烯和四氯化碳为原料的新合成路线。与Perkin法相比,苯乙烯-四氯化碳法具有原料廉价易得、反应条件温和、收率高和三废少等特点,是生产肉桂酸很有前途的方法。因此,苯乙烯-四氯化碳法生产肉桂酸不仅为四氯化碳找到了一条理想的出路,而且提高了该法生产肉桂酸的市场竞争力。由于四氯化碳是甲烷氯化物的一种,具有破坏臭氧层的作用,将逐步停止生产,苯乙烯-四氯化碳法亦将停止应用。
(3)苯甲醛-丙酮法:合成路线如下:
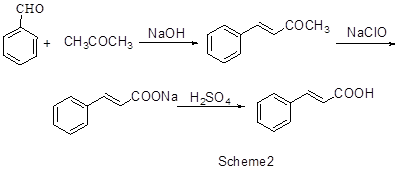
这条合成路线曾经用于工业合成,但由于工业流程长,操作复杂,能耗大,转化率低等问题而被淘汰。
(4)苯甲醛-乙烯酮法:苯甲醛和乙烯酮在锌盐和C6-18脂肪族羧酸催化下于100~125℃反应可以制得肉桂酸,当锌盐为2-乙基己醇时,收率可达87% [12]。乙烯酮是剧毒气体,化学性质活泼,反应条件不易控制,副产物多,因此此法不适于工业生产。
(5)苯甲醛-醋酸法:这是一个气相反应合成的方法,催化剂是将碱性催化剂固在于铝硅酸盐、SiO2-Al2O3或者硅胶等上制得。将苯甲醛和60%醋酸于350℃气化,再通过装有催化剂得反应器,空速300h-1。苯甲醛得转化率为49%,对肉桂酸得选择性73%[13]。
(6)苯乙烯—一氧化碳法:反应式如下:
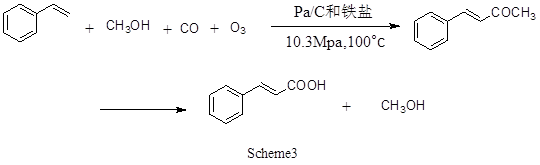
此法是由日本首先开发的一条以苯乙烯为原料的新和成路线。该法原料价廉,产率较高,但反应条件苛刻,工艺错综复杂,所用的钯催化剂昂贵。
(7)苄叉二氯-无水醋酸钠法:反应式如下:
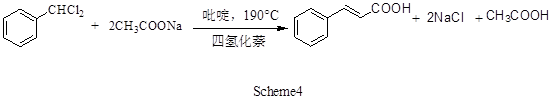
该法副产物多,产率低,曾经被以苄叉二氯为副产物的厂家采用,但已趋淘汰。
2论文设计思路及实验方案
2.1设计思路
在肉桂酸的合成方法中,工业生产肉桂酸的方法主要有Perkin法和苯乙烯-四氯化碳法,在实验室主要是用Perkin法制备肉桂酸。Perkin法制备法肉桂酸中不同催化剂、催化剂的用量及反应时间等对肉桂酸产率有较大的影响。
Perkin法制备肉桂酸所用的催化剂主要有为两类,一类为无水醋酸钾,另一类为无水碳酸钾。用无水醋酸钾为催化剂,反应时间长(苯甲醛转化率低),水蒸气蒸馏的时间长,产率低;改用无水碳酸钾为催化剂, 反应时间有所缩短,水蒸气蒸馏所用的时间需40 min以上,产率低。但实际实验时发现用无水K2CO3作催化剂,水蒸气蒸馏的时间仍长。通过查阅资料,任碧野[14]等采用氟化钾作催化剂,加入相转移催化剂PEG-600,反应1.5 h,所得肉桂酸产率达较高;李志平等[15]在研究混合固体碱催化合成肉桂酸时报道了反应时间对肉桂酸产率的影响,指出用碳酸钾和醋酸钾混合碱4.0g作催化剂,或用氟化钠和碳酸钾等混合催化剂进行催化合成肉桂酸时,得到了较好的效果。在本实验中,用Perkin法以碳酸钾、碳酸钠、醋酸钾、醋酸钠及混合碱为催化剂制备肉桂酸,分析反应中的各种因素对产率的影响,从而为肉桂酸生产的工业化提供依据和参考。另外,不同文献资料对同一催化剂所提供的反应时间不同,本实验采用TLC跟踪反应进程以确定不同催化剂下最佳反应时间[16-17]。
2.2实验方案
通过调查文献资料,本论文采用的实验方案为:
(1)以苯甲醛和乙酸酐为原料,固定原料摩尔比及回流温度,考察在不同的碱性环境:如无水碳酸钾、碳酸钠、醋酸钾、醋酸钠及混合碱等催化剂对肉桂酸产率的影响,并通过综合评价确定最佳反应催化体系。
(2)用重结晶技术对产品进行分离提纯。
(3)采用TLC跟踪反应,以确定不同催化剂下的最佳反应时间。
通过实验条件优化后,得出Perkin 法制备肉桂酸的最佳条件。
3实验部分
3.1化学试剂及仪器
3.1.1主要试剂
本实验所用的主要试剂(见表3.1)
表3.1 主要试剂
Table3.1 Important reagents

3.1.2 仪器设备
(1)X85-2恒温磁力搅拌器;
(2)SHⅠ-ⅡD型循环水真空泵;
(3)有机合成标准磨口仪器。
3.2实验条件优化
3.2.1 实验方法
在100mL三颈烧瓶中加入3.0mL(0.03mol)新蒸馏过的苯甲醛、8mL(0.072mol)新蒸馏过的乙酸酐以及催化剂。在恒温磁力搅拌器上加热回流。
反应一定的时间后,停止反应。待反应物冷却后,加入适量的温水。改为水蒸气蒸馏装置蒸馏出未反应的苯甲醛。在将烧瓶冷却,加入适量的碳酸钾至体系为碱性,以保证所有的肉桂酸成盐而溶解。用10mL乙酸乙酯萃取3次,冷却至室温,在搅拌下用浓盐酸酸化至酸性,析出固体肉桂酸。抽滤,用少量的水多次的洗涤沉淀,抽干。所得的粗产品在空气中晾干,称量。最后用5∶1的水-乙醇重结晶。
在后处理过程中,有的文献[16-17]是用水蒸气蒸馏除去未反应的苯甲醛;本实验用水蒸气蒸馏和萃取方法结合来除去未反应的苯甲醛,用这种处理方法能减少产品肉桂酸的损失,产品肉桂酸的纯度也会提高。
3.2.2 催化剂对产率的影响
取3.0mL(0.03mol)新蒸馏过的苯甲醛、8mL(0.072mol)新蒸馏过的乙酸酐,再分别取(0.032mol)的醋酸钾3.2g、碳酸钾4.4g、醋酸钠2.6g、碳酸钠3.4g。按上述步骤进行实验,且每组实验平行做三次,实验结果如表3.2 。
表3. 2单个催化剂对产率的影响
Table 3.2 single catalyst on the yield

通过表3.2可知,用Perkin法合成肉桂酸的最佳催化剂是碳酸钾,产率可达51%。所以在制备肉桂酸选择单一催化剂时碳酸钾效果较好,产率高,且碳酸钾的价格便宜。
在反应物的量及其他条件不变的情况下,取混合碱碳酸钾和醋酸钾以及混合碱碳酸钾和氟化钠共4.4g,按质量比1∶1投料,实验结果如表3.3。按质量比1∶2投料,实验结果如表3.4。
表3.3混合催化剂(按质量比1∶1)对产率的影响
Table 3.3 Mixed catalyst (mass ratio 1:1) to yield

表3.4混合催化剂(按质量比1∶2)对产率的影响
Table 3.4 Mixed catalyst (mass ratio 1:2) to yield
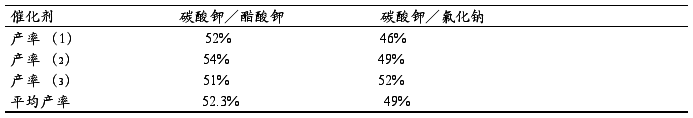
通过表3.3及表3.4可知, 在混合催化剂中,碳酸钾和醋酸钾混合碱产率高于碳酸钾和氟化钠, 且质量比按1∶2混合的产率高于质量比按1∶1混合的产率,其产率可达52.3%。
催化剂对肉桂酸产率影响实验表明:选择单一催化剂时碳酸钾较好,产率可达51%,或选择质量比1∶2的碳酸钾和醋酸钾混合碱,产率可达52.3%,且反应过程中结块少,利于后处理。这是由于碳酸钾的碱性较强,有利于夺取乙酸酐的α氢原子;同时,碳酸钾可以中和该反应产生的乙酸,生成的乙酸钾可以作催化剂。有关研究表明[18],钾阳离子非常广泛地以络合物形式参与反应,有利于反应的进行。
3.2.3 薄层色谱法(TLC)跟踪反应
薄层色谱法(Thin Layer Chromatography, TLC)是快速分离和定性分析少量物质的一种很重要的实验技术,也用于跟踪反应进程[16]。薄层层析法在很多方面得到了广泛的应用,如判断有机合成反应进行的程度;合成药物的质量控制及杂质检查;中草药的分离提纯;药物分析及含量测定等,本实验用薄层层析法判断有机合成反应进行的程度。
3.2.3.1 薄层板的制备
取羧甲基纤维素钠8g,溶于1000ml水中,在水浴上加热搅拌使完全溶解,倒入烧杯中,在中研钵中加入一定量羧甲基纤维清夜,向其中慢慢地加入吸附剂硅胶,边加边研磨,制成均匀的稀糊,按照硅胶G薄层涂布法制备薄层,或把两块载玻片面对面结合在一起,这样每片只有一面与硅胶糊接触,使薄片浸入硅胶稀糊中,然后慢慢取出,分开二块薄片,将未粘附硅胶糊的那一面水平放在一张清洁的纸上,这样重复操作多制备薄层板,让其自然凉干,100℃下烘30分钟。冷后于干燥器内备用。未消耗的硅胶稀糊可贮存在广口瓶内,以供再用。
3.2.3.2 点样
通常将样品溶于低沸点溶剂(丙酮、甲醇、乙醇、氯仿、苯、乙醚、四氯化碳和乙酸乙酯)配成稀溶液,用内径小于1mm管口平整的毛细管点样:
(1)先用铅笔在距薄层板一端1cm处轻轻划一横线作为起始线,然后用毛细管吸取样品,在起始线上小心点样,斑点直径一般不超过1-2mm。
(2)若因样品溶液太稀,可重复点样,但应待前次点样的溶剂挥发后方可重新点样,以防样点过大,造成拖尾、扩散等现象,而影响实验效果。
(3)若在同一板上点几个样,样点间距离应为1—1.5cm。
(4)点样要轻,不可刺破薄层。
3.2.3.3 展开
薄层色谱展开剂的选择和柱色谱一样,主要根据样品的极性、溶解度和吸附剂的活性等因素来考虑。凡溶剂的极性越大,则对一化合物的洗脱能力也越大,即Rf值也越大(如果样品在溶剂中有一定溶解度)。薄层色谱用的展开剂绝大多数是有机溶剂,薄层色谱的展开,在广口瓶中进行,将色谱板垂直于盛有展开剂的容器中。展开一段时间后在紫外灯下显色。
3.2.3.4 用TLC跟踪反应进程
安装好装置,投料后记录下开始加热时的反应时间T,在一块板上点上苯甲醛和反应混合物样(均需配成稀溶液),按上述方法进行展开和显色,记下原料样和反应混合物样的斑点位置,计算Rf值。从开始时算起每隔10分钟点一次样,记下苯甲醛和反应混合物样中相应斑点的位置和大小,计算Rf值。过20分钟后每隔5分钟点一次样,如发现反应混合液样中相应于原料斑点的位置处,无斑点或斑点变小,则说明反应已经完成或接近完成,所以依此可跟踪有机化学反应。
以碳酸钾为催化剂时,用TLC跟踪反应在25分钟前原料点无变化,无新点生成,30分钟后有新点出现 ,在55min后的原料点和新点的形状基本保持不变,说明反应以达平衡,该反应最佳时间为55min。TLC跟踪反应进程如表3.5。
表3.5用碳酸钾作催化剂时TLC跟踪反应进程
Table 3.5 using potassium carbonate as the catalyst and reaction process when the TLC
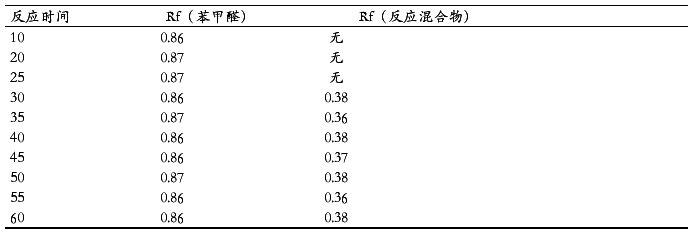
同样用TLC跟踪方法以醋酸钾作催化剂时,最佳反应时间在55分钟;以混合碱碳酸钾和醋酸钾以及混合碱碳酸钾和氟化钠作催化剂时最佳反应时间在50分钟。
4结果与讨论
用Perkin法以苯甲醛和乙酸酐为原料合成肉桂酸反应中,我们分别选用碳酸钾、醋酸钾及碳酸钾和醋酸钾混合碱等作为催化剂进行实验并采用TLC跟踪反应进程,所得结果如表4.1。
表4.1不同催化剂的产率及反应时间
Table 4.1 The yield of different catalysts and reaction time
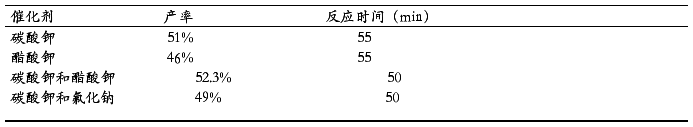
通过不同催化剂对肉桂酸产率的影响及TLC跟踪反应实验得到如下结论:
(1)以苯甲醛和乙酸酐为原料用Perkin法制备肉桂酸最合适的催化剂是碳酸钾和醋酸钾混合碱(质量比1∶2),TLC跟踪其反应的最佳时间是50min,使用该混合催化剂在实验过程中结块少、后处理方便。在实验方法上,本实验用水蒸气蒸馏和萃取方法结合来除去未反应的苯甲醛,用这种处理方法能减少肉桂酸的损失。
(2)薄层色谱(TLC)来跟踪反应时间是目前方便快捷的一种方法,可初步确定反应时间、能跟踪监测反应。该方法容易掌握、经济、方便、灵活。
由于有机反应的复杂性,反应过程中可能发生小部分聚合等其它副反应,使得该合成的产率有很大的不稳定性,因此对每一种条件的选择及控制必须非常严格。结合该课题前人的研究成果及本论文的研究结果,作者认为将来肉桂酸的合成制备研究应着重开展以下工作:
(1)进一步改进反应条件及后处理方法,提高产率。
(2)对肉桂酸及其衍生物性质进行系统的理论和实验研究,将结果进行分析,寻找新的更加经济的合成途径,研究开发肉桂酸及其衍生物的系列产品。
(3)进一步加强薄层色谱跟踪监测反应时间实验研究,在配合其它方法如气相色谱、液相色谱等跟踪反应,以确定反应最佳的时间。
参考文献
[1] 倪宏志, 邓润华. 肉桂酸的制备和应用[J]. 化学世界, 1996, (8): 399-403.
[2] 李明阳, 王永强. 肉桂酸的合成方法研究[J]. 吉林大学自然科学学报, 1989, (2): 131-133
[3] 卢玉华, 药物合成手册[M]. 北京: 人民卫生出版社, 1989: 360-369.
[4] Opdyke D L J. Monographs on Fragrance Raw Materials[J]. Cinnamic Acid. Food Cosmet Toxicol ,1978 ,16 (1) : 687-690.
[5] HunLigwnag. Nondeklunomir.Activationofhtecarbon-halogenbondinPoylhalomehtnaesby
coPPercomPleses[J]. collect.czech.chem.commuunl987. 2(7): 1758-1721.
[6] 天津红旗制药厂肉桂酸的合成[J]. 医药工业, 1974, ( l): 26-28.
[7] 化工部科技报所. 肉桂酸世界细化工产品技经手册[M]. 北京: 科学出版社, 1988: 3-5.
[8] Gerdlin.Ivo.Newsynhtesisofcinnmaicacidnaditsderivatives[J]. Pollena:ThuszezeScrodkiPiorace,kosmet, 1987, 31(l-2): 13-15.
[9] 盛淑铃, 贾晓红. 相转移催化法合成肉桂酸[J]. 化学研究, 20##, 15(2): 37-38.
[10] 余凌种. 有机化学中的人名反应[M]. 北京: 科学出版社, 1984: 320-323, 326-327.
[11] W.H. Pekrin. Pekrin[J]. Chem.soc, 1868, 18(1):21- 53.
[12] 杨贫, 高孝恢. 编著性能结构化学键[M]. 北京高等教育出版社, 1987: 119-121.
[13] 罗渝然. 化学键能数据手册[M]. 北京:科学出版社, 20##: 106-108, 132-140.
[14] 任碧野, 陈国斌. 肉桂酸的Perkin合成工艺改进[J]. 化学世界, 1996, (1): 21-23.
[15] 李志平. K2CO3∕CH3COOK混合固体碱催化合成肉桂酸[J]. 湖南城市学院学报, 20##, 15(1): 53-54.
[16] 曾昭琼, 曾和平. 有机化学实验[M]. 北京: 高等教育出版社, 20##: 121-122.
[17] 王清廉, 沈凤嘉. 有机化学实验[M]. 北京: 高等教育出版社, 1994: 4: 206-208
[18] Keopp E, Roegtle H. Perkin-synthese mit casiumacetat[J]. Syn-thesis, 1982, (2) : 177-179.
-
综合行政部20xx年工作总结及20xx年工作思路
20xx年工作总结及20xx年工作思路一、20xx年工作总结,我部紧紧围绕公司总体安排部署,在公司的正确领导和各职能部门的配合支持…
-
项目技术工作总结(冯伟)
项目技术工作总结本人于20xx年x月至今在福建佳诚建设工程有限公司当施工技术员此期间,我努力钻研专业技术知识,在技术管理过程中努力…
-
建筑施工安全生产互检大检查工作总结
建筑施工安全生产检查工作总结为了更好的保证开发区施工现场的安全,坚决遏制重(特)大建筑施工安全事故的发生,保障人民生命财产安全,切…
-
初中数学研修总结
南钢学校:熊玉忠通过几个月的网上研修学习,我接触到了专家学者们的教育新理念,学习了不少优秀教师的课堂教学设计,同时还与班内的一线教…
-
寒假社会实践总结
寒假的社会实践活动已经结束了,但社会实践给我们带来的巨大影响却远没有结束。它使我们走出校园,走出课堂,向社会,走上了与实践相结合的…