ʵ��һ������ѧʵ�����������ϰ
������ѧʵ��̰�
�γ�Ŀ��
1 ����ȷ�����������ն�����ѧ����ʵ��Ļ����������ܣ�ѧϰ�����յ��͵ķ���������
2 �����������ѧ������֪ʶָ��ʵ�飻�������Բ���������ͳ�ﰲ��������
3 ��ȷ�� �� �� �� �� �� ��� �� ���� �� ��Ч���� �� �ĸ��ѧ����ȷ��������ѡ��ʵ��������ʵ���������Ա�֤ʵ�����Ŀɿ��ԡ�
4 ��ͨ�����ⷽ��ʵ�飬�����ۺ�����������Ϣ�����ϵ��ռ������������ݵļ�¼�����������������֤�����۵�ı��������ۣ������������ɣ�����̽������ʶ��
5 �������Ͻ��Ŀ�ѧ̬�Ⱥ�ʵ�����ǡ�һ˿�����Ŀ�ѧ���磻������ѧ������Ӧ�еĻ������ʡ�
��ѧ��ѧʵ���ѧϰ����
1��Ԥϰ
�� �����Ķ��̲ġ��йؽ̿��鼰�ο����ϣ�������֪ʶ���淶�Ļ�������
�� �Ӹ�¼���й��ֲ��в�����������ѧ����
д ����д��Ԥϰ���档
�ڡ������顢˼����ʽ��Ԥϰ�����У���ȷʵ��Ŀ�ģ��˽�ʵ��ԭ������Ϥʵ�����ݣ���Ҫ�������裬���ݴ������������ע�������������ʵ��ʱ�䡣�ڴ˻�����дԤϰ���档
2����������
ʵ��ǰ ���ʡ����ۣ�����ʵ��ԭ��������Ҫ�㡢ע������
�ۿ�����¼����ʦʾ��
ʵ��� �������ܽ�
ʵ��
��1���������ʵ�顪�����桢ϸ�ġ����Բ��á�
��2����ȷʹ�����������������淶������
��3����ϸ�۲���������ⶨ����
��4����ʱ����ʵ��¼������Ǧ�ʡ�����ֽƬ����������ƾ������Ըɾȥ���ݣ���Ϳ�����ݣ�������Ƥ��������ֽճȥԭʼ���ݣ��Ǵ�������ʱ��ȷ�ĸ�д������
��5������˼�� �����Լ�������⣬�ɲ����ϡ������ʦ����
��3����4����5���ɹ���Ϊ��ʵ�顢��¼����˼��
��6��������������ѧϰ ���ʵ����������л��ɣ��ڷ����Ͳ�ԭ���ͬʱ����������о����Բ������ĵط�����Ľ������
��7������ʵ�����õ���ʦͬ��
ʵ�鱨�����д
��1��Ԥϰ���֣�ʵ��ǰ�� Ŀ�ġ�ԭ�������衢����ֵ��˼����
��2����¼���֣�ʵ��ʱ�� ʵ������ʵ������
��3�����۲��֣�ʵ��� �����������⡢����
����������ʱ���д�����������������ʵ�鱨�档
Ԥϰ�������д
ʵ��Ŀ�� ѧϰ��֪ʶ�뼼����Ҫ���������
ʵ��ԭ�� ΪʲôҪ����������Ӧʽ
ʵ�鲽�� ��Ӽ�ͷ��ÿһ����Ϊһ��������Ԫ�������÷��š�����d
������ԭ����д�IJ��
���裺�������ԭ����Ϊʲô��
��д����Ҫ���ּ�����������������Ҫ�������ͷ����
˼�����д��ԭ����������
��ʵ��ǰ���Ԥϰ���棬����Ԥϰ����������ʵ��
��ѧʵ�����
���ü��ɣ����ٵ��������ˣ�������٣���������̸Ц�����衢��λ����
��Լ��ҩƷ��ˮ���硢��
���ࣺ������·�����������顢�ʡ����汾�ȷ��ڳ����ڡ���ֽ�����װ������´����ڡ������ϣ��ݲ�ʹ�õ���������ķ���ʵ�������棬ϴ���IJ������ιܷ��ڸɾ���250mL�ձ��ڣ�ʵ���в��õ��������ó��������Ҫ��������������������������������ʰ��ʵ���ϴ�����պò���������Ĩ�ɾ����棨�øɾ���Ĩ����������ˮ�ۡ�
ֵ��������ɨ������ʵ���ҡ���ƽ�ң������Լ��ܣ����ˮ���硢ú������֤ʵ���Ұ�ȫ��
���ؽ�ʦָ�����õ���ʦͬ����뿪ʵ���ҡ�
��ȫ֪ʶ
���ز�������һ�б�Ҫ�İ�ȫ��ʩ����֤ʵ�鰲ȫ��
ʹ��Ũ�ᡢŨ��ж�ҩƷʱС�ġ�
���д̼��ԡ�������ж����������ʵ�飻���ȡ��������ᡢ�ܽ�������Լ�ʱ��ͨ����ڽ��С�
ʵ���Ҳ�й©ú����Һ��������ͣˮ��ͣ��ʱ����ʱ�غ�ˮ���磻
��ʵ����ϴ�֣���ʵ���Ҳ��Զ�����
��ʵ���Ҿ��������£������·���ע��𣬲���ע��Ũ�ᡢŨ����ϴҺ��
ʵ������ֱ���
ʵ�����ݼ���� 30%
ʵ����������� 35%
Ԥϰ����¼������ 30%
���������� 5%
ʵ��һ���ζ������������������
һ��ʵ��Ŀ�� 2012��2��21
1. ��Ϥ������ѧʵ���ҹ���Ͱ�ȫ�����˽������ѧʵ��εĻ���Ҫ��
2 ��Ϥ���õζ�����������ʹ�÷��������������У������
3. ��Ϥ����������ϴ�Ӻ��﷽����
������Ҫ�Լ�������
1��������ѧʵ�鳣������һ�ס�2��K2Cr2O7(s),H2SO4(Ũ)��ϴ�ྫ
����������ѧʵ�����֪ʶ
1�����������ϴˢҪ������ڱ�ˮ������ʪ������ˮ��
1��.�ձ�����Ͳ����ƿ�������ȣ�
��ëˢպȥ�۷ۣ���̼���ơ�������ϸɰ�Ȼ�϶��ɣ���ϳ�ϴ�Ӽ�ˢϴ-����ˮϴ��-����ˮ��ϴ (���š���������Ρ���ԭ��) 3�Ρ�
2��.�ζ��ܡ���Һ�ܡ������ܡ�����ƿ�ȣ��о�ȷ�̶ȣ���0.2%��0.5%�ĺϳ�ϴ��Һ�����ϴҺ���ݼ����ӣ�����ϴҺ�ջأ�-����ˮϴ��-����ˮ��ϴ3�Ρ�
3��.��ȷ����õı�ɫ���ɹ�ѧ������ʯӢ�Ƴɣ������ȵ�HCl-�Ҵ�����-����ˮϴ��-ȥ����ˮϴ����
����ϴ�Ӽ���
a������ϴҺ K2Cr2O7-H2SO4��10g K2Cr2O7 +20mLˮ�����Ƚ����ܽ⣭��ȴ����������200mLŨ���ᣭ�����ڲ���ƿ�С�����ǿ���ԡ�ǿ�����ԣ����л�����۵ȵ�ȥ�������ر�ǿ����Ч������ɫ��ʧЧ����ɫ��
b���ϳ�ϴ�Ӽ���ϡHCI��NaOH-KMnO4 ���Ҵ���ϡHCI ��NaOH/�Ҵ���Һ��ȥ�л��Ч���Ϻã���
C��ϴ�ྫ
���������ĸ����
a���������ɣ����ַ�ɡ�
b�����ɣ���������ڲ��ɺ���С��濾����ͣת��������ʹ�����Ⱦ��ȣ����������Թܡ��ձ���������������ĸ��
c����ɣ����������ڽ������������ں����У������¶���105�����Һ�ɡ����������ھ��ܶȸߵ����������ĺ�ɡ���
d�����ɣ��õ紵�紵�ɡ���
3��������ˮ������ˮ��ȥ����ˮ��ʯӢ�Ƿ�����ˮ��ȥ���Ӻ��������ˮ
4�� ��ѧ�Լ�����̲�p9��
IUPAC�������ۺ�Ӧ�û�ѧ���ϻᣨInternational Union of Pure and Applied Chemistry�����弶���ҹ������Ϸ�Ϊ�ļ���
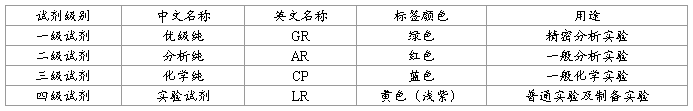
������;�Ļ�ѧ�Լ������״��Լ���ɫ�״��Լ�
������������������
1�����
 ��ʽ��װ�ᡢ���ԡ����������� HCI,AgNO3,KMnO4,K2Cr2O7
��ʽ��װ�ᡢ���ԡ����������� HCI,AgNO3,KMnO4,K2Cr2O7
��ʽ��װ������������� NaOH,Na2S2O3
������100mL,50mL,25mL,10mL,1mL
��1�� ���
��ʽ������ת���Ƿ���©ˮ��Ϳ��ʿ��
��ʽ�������ϻ���©ˮ�� �������ܡ�������
��2�� ϴ��
����ˮ��ϴ��Һ������ˮ������ˮ
��3�� װ�ζ���
ҡ����Һ����ϴ�ζ���2��3����10��15mL/�Σ���װҺ����̶����ϣ�
��4�� �����ݣ����㲢��¼��ʼ����
��5�� �ζ�
��ʽ����������©Һ ������ҡ����ƿ
��ʽ����ѹ������ƫ�ϲ�λ�������ݡ�
���յ�ʱ��Ҫ����Ρ���������ϴ
��6�� �۲���ɫ�仯�Ͷ���
�ζ��ܴ�ֱ��������̶�ƽ�У�����С�������λ
��7�� ��Һ��ϴ�� ��ʽ�ζ��ܳ��ڷ��ã���ֽƬ
2������ƿ
����һ���������Һ��
������1000mL��500mL��250mL�� 100mL, 50mL��
��飺©ˮ���̶�����ƿ��̫����ϵ��Ƥ�
�����Һ������ǩ ��Һ���ڱ��棭�Լ�ƿ ���ڷ��ã���ֽƬ
3����Һ�ܡ�������
����ȷ��ȡһ���������Һ
������25mL��20mL��10mL�� 5mL,2mL��1mLl�ȣ�����ǩ
ϴ�ӣ�����ˮ��ϴ��Һ������ˮ������ˮ����ϴ2��3��
��Һ����Һ��������б30º�������ڴ�ֱ��Һ��ͣ15�룩
ʵ�鲽����
1.�������嵥���������ѧʵ������Ҫ����������Ϥ�����ƺ��
2.��鲢ά�������ζ��ܡ�����ƿ�ȡ���
3.ϴ������ȡ��������ע���ʽ�ζ��ܵ�ϴ�ӷ�������
ע�⣺
1����ʽ�ζ��ܵ�����Ϳ�շ�ʿ�ֺ���©����ʽ�ζ��������ݺ���©��
�ζ����й�ˮ����߱��ߣ� 10 ���Ӻ�۲��Ƿ�©ˮ�����е�©����ʽ�ζ���������Ϳ�ͣ���ʽ�ζ����������������齺�ܡ�ǿ���ζ����Ͽ����¶˳��ڼⲿ�ı�����
2���Ӵ˴�ʵ�鿪ʼ��ÿ��ʵ�����ǰ��Ӧ������ƿϴ�ɾ������Ƿ��������������ɣ�Ϊ�´�ʵ��������
3����ʵ����,Ҫע�ⰲȫ,����������
�ڶ�ƪ��������ѧʵ��κ�ϰ���(���İ�)
ʵ��һ �����ӵ�һ�飨���飩�ķ���
˼���⣺
1.������һ��������ΪʲôҪ��������Һ�н��У����ڼ��������½��У����ᷢ��ʲô�����
����ϵͳ�����У�Ϊ�˷�ֹ��ˮ�����ӵ�ˮ�����ɳ����������һ�飬���Գ�����һ��������ʱҪ��������Һ�н��С����ڼ��������½��У���һ���Ժ�Ĵ������ӽ����ɳ����������Ͳ��������Ŀ�ġ�
2.��δ֪��Һ�м����һ�����Լ�HClʱ��δ���ɳ������Ƿ��ʾ��һ�������Ӷ������ڣ�
����δ֪��Һ�м����һ�����Լ�ʱ��δ���ɳ�����ֻ��˵��Ag+,Hg22+�����ڣ�������˵��Pb2+�����ڣ���Ϊ����Һ��Pb2+��Ũ��С��1mg?ml-1,���¶Ƚϸ�ʱ��Pb2+�����ڵ�һ�������������ڶ��顣
3.�����KI����HCl��Ϊ��һ�����Լ�����������Щ�����
�������KI����HCl��Ϊ��һ�����Լ�ʱ�����̫С���ڶ�����ˮ��������ӽ�ˮ������һ�飬�ﲻ�������Ŀ�ġ�������������������ӽ���I- ����������ԭ��Ӧ��ʹ��Щ���ӵ�Ũ�Ƚ��Ͳ��ܼ�����
ʵ��� �����ӵڶ��飨ͭ���飩�ķ���
˼���⣺
1. ������������ʱ���ڵ�������Ϸ�����ƫ��ƫ��������������Щ�����
�𣺳���������������ƫ��ʱ��������������Zn2+ ������ZnS ��������ڶ��顣�����ƫ��ʱ�������Cd2+ �����������������������顣
2.�ڱ�ʵ����Ϊ����������������ʱ��Ϊʲô�ȵ���0.6mol·L-1HCl��ȣ�Ȼ����ϡ��һ����ʹ�������Ϊ0.2 mol·L-1?
����As(III)��������ȫ��������0.6 mol·L-1HCl�����,Cd2+��������ȫ��������0.2 mol·L-1HCl����¡����Ϊ��ʹ����������ȫ�������������������������ӷ��룬�����ڵ������ʱ,�ȵ���0.6 mol·L-1HCl��ȣ�Ȼ����ϡ��һ����ʹ�������Ϊ0.2 mol·L-1��
3.��TAA����H2S��Ϊ�ڶ������Լ�ʱ��Ϊʲô���Բ���H2O2��NH4I?
����TAA����H2S��Ϊ�ڶ������Լ�ʱ����TAA��90�漰������Һ�У����ڳ���ʱ���ڽ�As(V)��ԭΪAs(III)���ʲ�������NH4I������TAA�ڼ�����Һ�м���ʱ��������һ���ֶ������������������ԣ��ɽ�Sn(II)����ΪSn(IV)���ʲ���Ҫ��H2O2��
4.��֪ijδ֪��Һ���������������ӣ��ڳ����ڶ�������ʱ�Ƿ�Ҫ������ȣ�
����As(III)��������ȫ���������0.6 mol·L-1,�ڴ�����£���������Ӳ�����ȫ�������������������ڵ���0.2 mol·L-1ʱ������Cd2+�����������ȫ����As(III)�����ﲻ���������δ֪Һ������������������ʱ��Ϊ��ʹ�ڶ��������ӳ�����ȫ������Ҫ������ȡ�
5.��ԭ��ҹ���顢�ࡢ���ߵͼ�̬�����Ӵ��ڣ���˵��������������ϵ���������м�̬�ı仯��
������HCl������һ��������ʱ���顢�ࡢ���ĸߵͼ����Ӿ��������Ӵ��ڣ�Ҳ�������������ӡ�����TAA��������ʱ��As(V)����ԭΪAs(III), Sb(V)Ҳ����ԭΪSb(III)����Sn(II)����Һ�еĶ���������ΪSn(IV)���ڼ���ʱ��Sb(III)������ԭΪSb��Sn(IV)������ԭΪSn(II)��Sn(II)�ֱ�Hg2+����ΪSn(IV)��
ʵ���� �����ӵ����飨���飩�ķ���
˼���⣺
1.��ϵͳ�����У�������������ʱ�ɷ���Na2S����(NH4)2S��
����ϵͳ�����в�����Na2S����(NH4)2S ����Na2S�ļ��Ա�(NH4)2S�ļ���ǿ����pH=10.7ʱ�������Mg2+��Ҫ�������뱾������С�
2.��(NH4)2S��TAA������������ΪʲôҪ���㹻��NH4Cl��
����(NH4)2S��TAA������������ʱ��ֻ����pH=9.0����������²�����������������������������������ӷ��롣���ǣ������ڷ�Ӧ���������ų��������ɣ���ʹpH���ͣ�Ϊ�˱���pH=9.0�ͷ�ֹMg2+����������Ӧ�����㹻��NH4Cl����NH3?H2O�γ��ȶ��Ļ�����ϵ������NH4Cl���ɷ�ֹ�����γɽ��塣
3.��ϵͳ�����У���������������ɺ���ĸҺ���ù�ҹ�����ij������Ƿ���ԣ�
����ϵͳ�����У���������������ɺ���Ҫ�������������������ӣ���Ӧ�������ķ��룬����Һ���������������ӣ���Ӧ��ŨHAc�ữ�������ȳ�ȥH2S������S2-�ڼ�����Һ��������ΪSO42-��ʹ�������е�Ba2+��Sr2+ �����������γ�������ʧ�����Ա�������������ɺ�����ĸҺ���ù�ҹ��
4.��6mol·L-1HNO3�ܽⱾ�����ʱ��Ϊʲô��KNO2��KClO3�����������Լ����ܽ⣿
����6mol·L-1HNO3�ܽⱾ�����ʱ����KNO2��KClO3�������ɼ��ٳ����ܽ⣬����Ҫ����Ϊ������������ԭ��Ӧ���ƻ���M2++S2-==MS��ƽ�⣬������S2-Ũ�ȣ�ʹ��Ӧ������У��Ӷ������˳������ܽ⡣
5.��֪ NiS��CoS ��0.3mol·L-1HCl��Һ�в��ܱ�H2S��������Ϊʲô���ɵ� NiS��CoS��������1mol·L-1HCl��
��NiS��CoS��0.3mol·L-1HCl��Һ�в��� H2S���������ڵ���������ɳ������ֲ�����1mol·L-1HCl����������NiS��CoS���Բ�ͬ������ڵ�Ե�ʣ����γɵij����Ǧ��壬���û���Ⱥܿ��Ϊ���壨 Ni2S3��Co2S3�������������1mol·L-1HCl��
ʵ���� �����ӵ����飨�����飩�ķ���
˼���⣺
1.��ϵͳ�����У�����������ж������Ӷ�ʧ�Ŀ���ԭ������Щ��
�𣺢��ڳ���������������ʱ�������ȿ��Ʋ����������������������Ӻ����Һĩ��ʱ������S2-������ΪSO42-��ʹ�������ж������ӳ�������ʧ���ڳ�������������Ҫ�㹻��CO32-���ӣ�����ȿ��Ʋ���, CO32-����Ũ�Ƚ��ͣ��������Ӳ��ڱ����������ʧ��
2.��K2CrO4�Է�����Ba2+ʱ��ΪʲôҪ��HAc��NaAc��
������K2CrO4����Ba2+ʱ��Ϊ��ʹBa2+����BaCrO4��ɫ������Sr2+������SrCrO4��������Һ�� pHֵӦ��4��5������HAc��NaAcʹ���γɻ�����Һ���Կ�����һ��ȡ�
3.��þ�Լ�����Mg2+ʱ������(NH4)2S�����������ӵ������У�����ӵò��㣬������ʲô�����
����þ�Լ�����þʱ�������ؽ��������и��ţ�Ҫ����(NH4)2S�������������������㣬�������ӳ�����ȫ�������ڼ�����Һ���������������������Щ�������ڱ�������ɫ�������������Լ�����ɫ�ȶ��Լ��� Mg2+��ɸ��š�
ʵ���� �����ӵķ���ͳ�������
˼���⣺
1.�������ӷ����Լ��У�
(1)BaCl2����ó�������ܷ�һ�������������ų���
��BaCl2����ó���������ܽ���һ�������������ų�����S2O32-��Ba2+���ɵ�BaS2O3�����ܽ�Ƚϴ�ֻ�е�S2O32-Ũ�ȴ���4.5mg·ml-1ʱ��������������������BaS2O3�������γɹ�������Һ������
(2)AgNO3����ó��϶�������ܷ���Ϊ�ڶ�����������������һ�ִ��ڣ�
�� ��ΪS2O32-��Ũ�Ƚ�Сʱ�������ڵ�һ��������������ڵڶ�������Ag+����Ag2S���������Ե�AgNO3����ó��϶����ʱ��������Ϊ�ڶ�����������������һ�ִ��ڡ�
2.�������Ի�ԭ�������У�
��1�� ��ϡHNO3����ϡH2SO4���ữ��Һ�Ƿ���ԣ�
����HNO3���������ԣ��ữʱ��ʹS2-��S2O32-��SO32-��I-���������Բ�����HNO3����H2SO4�ữ��
��2�� ��ϡHCl����ϡH2SO4�Ƿ���ԣ�
�������Cl-����ʱ�������������£���ʹKMnO4��ɫ�����Բ�����HCl����H2SO4�ữ��
��3�� ��ŨH2SO4���ữ��Һ�Ƿ���ԣ�
����ŨH2SO4���������ԣ����Բ��������ữ��Һ��
3.���и�����Һ���ڸ�����������н��������ı��֣�
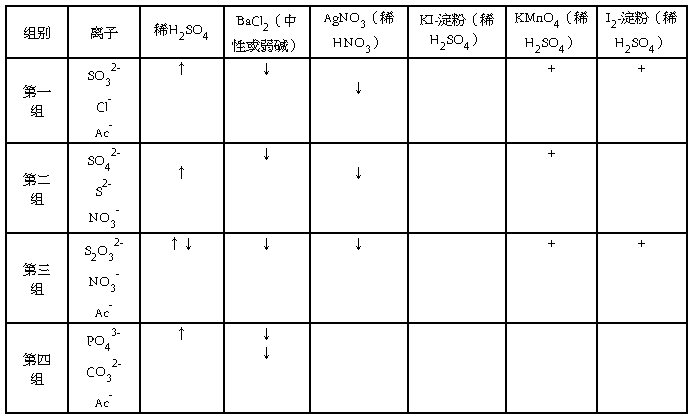
��������ʵ��
ʵ��һ ������ƽ������ϰ
˼���⣺
1.�Ӽ����롢Ȧ��ͳ�����ʱ��Ϊʲô����ر���ƽ��
����ƽ���������ںܴ�̶���ȡ����������觵��ڵ������������ڲ�������ȱ�𣬽���Ӱ������������ȣ���ˣ��ڼӼ����롢ȡ������ʱ������ر���ƽ��ʹ��觵��͵��зֿ����Ա�����觵��ڡ�
2.������ƽ��������Խ�ߣ��Ƿ������ȷ�Ⱦ�Խ�ߣ�
�𣺷�����ƽ��������Խ�ߣ����dz�����ȷ�Ⱦ�Խ�ߡ���Ϊ̫��������ﵽƽ���Ϊ���ѣ������ڳ�����
3.�ݼ������������������ܷ���С��ȡ����Ϊʲô��
�𣺵ݼ����������������в�����С��ȡ������Ϊ�������в���Ҫմ��С���ϣ�Ӱ�������ȷ�ȡ�
4.�ڳ��������У���ͶӰ���Ϲ۲쵽����������100�ֶȵ��ұߣ���ʱ˵�������ػ��������أ�
���ڳ��������У���ͶӰ���Ϲ۲쵽����������100�ֶȵ��ұߣ���ʱ˵�������ء�
ʵ��� �ζ���������������ϰ
˼���⣺
1.HCl��NaOH����Һ�ܷ���ֱ�����Ʒ����ƣ�Ϊʲô��
������NaOH���������տ����е�CO2��ˮ�֣�ŨHCl��Ũ�Ȳ�ȷ����������HCl��NaOH����Һʱ������ֱ�ӷ���
2.����������Һʱ��Ϊʲô����Ͳ��ȡHCl����̨�ӳ�ȡNaOH��S���������������ܺͷ�����ƽ��
�������������ڱ���ȡ�費ͬ�����������������ƽ������ȷ��ȡһ�����ľ��ܺ�����������HCl��Ũ�Ȳ����� NaOH������CO2��ˮ�֣�����ֻ��Ҫ����Ͳ��ȡ ����̨�ӳ�ȡNaOH���ɡ�
3.����Һװ��ζ���֮ǰ��ΪʲôҪ�ø���Һ��ϴ�ζ���2��3�Σ�����ƿ�Ƿ�Ҳ���ø���Һ��ϴ���ɣ�Ϊʲô��
��Ϊ�˱���װ���ı���Һ��ϡ�ͣ�����Ӧ�øñ���Һ��ϴ�ι�2��3�Ρ�����ƿ����ˮҲ����Ӱ�챻���������ı仯��������ƿ�������ñ���Һ��ϴ���ɡ�
4.�ζ����ٽ��յ�ʱ�����εIJ������������еģ�
�𣺼����εIJ�����:����ʽ�ζ��ܵ���������ת�����ʽ�ζ��ܵ��齺�����ɶ���ʹ�����Һ���ڹܿڣ�����ƿ�ڱ���ܿڽӴ���ʹҺ������������ϴƿ�Դ�ˮ���¡�
ʵ���� NaOH��HCl����Һ�ı궨
˼���⣺
1.��μ����ȡ�����ڱ���������ػ�Na2CO3��������Χ���Ƶ�̫���̫�ٶԱ궨�к�Ӱ�죿
���ڵζ������У�Ϊ�˼��ٵζ��ܵĶ�����һ�����ı���Һ�����Ӧ��20��25ml֮�䣬��ȡ����Ĵ�Լ����Ӧ����ʽ��ã�
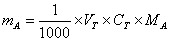
��������ʳƵ�̫�࣬�����Ƶı���Һ��Ũ������һ�λ��ι�������ɵ����ͽϴ�ȡ�����ʵ���Ҳ����̫�٣���Ϊÿһ�ݻ����ʶ�Ҫ�������γ��������ÿ����±0.1mg������ÿ�ݾͿ�����±0.2mg������ˣ���ȡ�����ʵ�����Ӧ����0.2000g����������ʹ���������������1�� ��
2.�ܽ������ʱ����20��30mlˮ��������Ͳ��ȡ����������Һ����ȡ��Ϊʲô��
����Ϊ��ʱ���ӵ�ˮֻ���ܽ�����ʣ�������Ӱ������ʵ�������˼����ˮ����Ҫ�dz�ȷ�����Կ�������Ͳ��ȡ��
3.�������δ��ɣ���ʹ����ҺŨ�ȵı궨���ƫ����ƫ�ͣ�
�����������δ��ɣ���ʹ����ҺŨ�ȵı궨���ƫ�ߡ�
4.��NaOH����Һ�궨HCl��ҺŨ��ʱ���Է�̪��ָʾ������NaOH�ζ�HCl����NaOH��Һ�����治��������CO2���ʶԲⶨ����к�Ӱ�죿
����NaOH����Һ�궨HCl��ҺŨ��ʱ���Է�̪��Ϊָʾ������NaOH�ζ�HCl����NaOH��Һ�����治��������CO2�����γ�Na2CO3��ʹNaOH��ҺŨ�Ƚ��ͣ��ڵζ���������Ȼ���е�Na2CO3��һ�����Ĺ�ϵ��HCl������Ӧ�����յ��̪��ɫʱ����һ����NaHCO3ĩ��Ӧ������ʹ�ⶨ���ƫ�ߡ�
ʵ���� ����е������IJⶨ����ȩ����
˼���⣺
1.����е��IJⶨΪ�β�����NaOHֱ�ӵζ�����
����NH4+��Ka=5.6×10-10����Cka<10-8,����̫�������Բ�����NaOHֱ�ӵζ���
2. Ϊʲô�кͼ�ȩ�Լ��еļ����Է�̪��ָʾ�������к���������е����������Լ�����ָʾ����
�𣺼�ȩ�Լ��еļ����Է�̪Ϊָʾ����NaOH����ȫ�������кͣ����Լ���Ϊָʾ������NaOH�ζ���ָʾ����Ϊ��ɫʱ����Һ��pHֵΪ4.4�����������ȫ�к͡���������е����������Է�̪Ϊָʾ������NaOH��Һ�ζ����ۺ�ɫʱ����ξ����ٲ��ֱ��ζ���ʹ�ⶨ���ƫ�ߡ�
3.NH4HCO3�к������IJⶨ���ܷ��ü�ȩ����
��NH4HCO3�к������IJⶨ�����ü�ȩ��,����NaOH��Һ�ζ�ʱ��HCO3-�е�H+ͬʱ���ζ������Բ����ü�ȩ���ⶨ��
ʵ���� ��ϼ�ķ�����˫ָʾ������
˼���⣺
1.��˫ָʾ�����ⶨ��ϼ���ɵķ���ԭ����ʲô��
�𣺲��ϼ���Һ����ѡ�÷�̪�ͼ�������ָʾ������HCl����Һ�����ζ����ζ��ķ���ԭ����ͼ�����£�
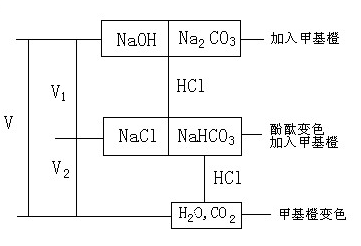
2.����˫ָʾ�����ⶨ��ϼ�ж�������������£���ϼ����ɣ�
��1�� V1=0 V2>0��2��V1>0 V2=0��3��V1>V2��4��V1<V2��5��V1=V2
�� V1=0 V2>0ʱ�����Ϊ��HCO3-
�� V1>0 V2=0ʱ�����Ϊ��OH-
�� V1>V2ʱ�����Ϊ��CO32-+ OH-
�� V1<V2ʱ�����Ϊ��HCO3- +CO32-
�� V1=V2ʱ�����Ϊ�� CO32-
ʵ���� EDTA����Һ��������궨
˼���⣺
1.��ϵζ���Ϊʲô���뻺����Һ��
�𣺸��ֽ���������ζ������������ʱ��Ӧ���������pHֵ������Ͳ��ܱ�ȷ�Ρ����һ�����Ӱ��ָʾ���ı�ɫ�����������ɫ�������յ��������������ȷ�ζ��������ȶ���ϵζ���Ӱ���Ƕ��ģ���Ҫ���뻺����Һ���Կ��ơ�
2. ��Na2CO3Ϊ����Ը�ָʾ��Ϊָʾ���궨EDTAŨ��ʱ��Ӧ������Һ�����Ϊ���Ϊʲô����ο��ƣ�
����Na2CO3Ϊ�����ʣ��Ը�ָʾ��Ϊָʾ���궨EDTAŨ��ʱ����Ϊ��ָʾ����Ca2+��pH=12��13֮�����γɾƺ�ɫ�����������ʴ���ɫ�����ζ����յ�ʱ��Һ����ɫ�ɺ�ɫ�䴿��ɫ��������NaOH������Һ��pHΪ12��13��
3.�Զ��ӳ�Ϊָʾ������Zn2+�궨EDTAŨ�ȵ�ʵ���У���Һ��pHΪ���٣�
�⣺ ���μ��İ������ᷴӦΪ��
(CH2)6N4+HCl==(CH2)6N+H+·Cl-
��Ӧ����������ʵ�����
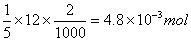
���μ��İ������ʵ�����
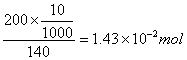
�����μ��İ�������
������ϵ��ʣ�����μ��İ���Ũ��Ϊ��
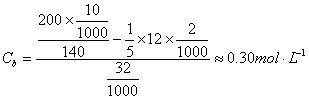
���μ��İ��ε�Ũ��Ϊ��

����һ�㻺����Һ���㹫ʽ��
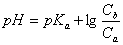 �ã�
�ã�

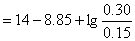
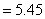
�����μ��İ�pKb=8.85��
4.��ϵζ��������ζ�����ȣ�����Щ��ͬ�㣿������Ӧע����Щ���⣿
����ϵζ��������ζ������������������ͬ�㣺
�� ��ϵζ���Ҫ���γɵ������������ӣ�Ҫ�൱�ȶ��������õ����Եĵζ��յ㡣
�� ��һ�������£���λ������̶�����ֻ�γ�һ����λ����������
ʵ���� ˮ����Ӳ�ȵIJⶨ
˼���⣺
1.ʲô��ˮ����Ӳ�ȣ���������ˮ����Ӳ�ȣ�
��ˮ��Ca2+��Mg2+��������Ϊˮ����Ӳ�ȡ�
����ˮ����Ӳ�ȵĹ�ʽΪ��
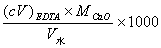 ��mg·L-1��
��mg·L-1��
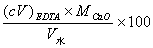 ( o )
( o )
2.Ϊʲô�ζ�Ca2+��Mg2+����ʱҪ����pH��10�����ζ�Ca2+����ʱҪ����pHΪ12��13����pH>13ʱ��Ca2+�Խ���к�Ӱ�죿
����Ϊ�ζ�Ca2+��Mg2+����ʱҪ�ø���T��ָʾ��������T��pHΪ8��11֮��Ϊ��ɫ������������γɵ������Ϊ�Ϻ�ɫ���յ�ʱ��ҺΪ��ɫ��������Һ��pHֵҪ����Ϊ10���ⶨCa2+ʱ��Ҫ����Һ��pH������12��13����Ҫ����Mg2+��ȫ����Mg(OH)2�������Ա�֤ȷ�ⶨCa2+�ĺ�������pHΪ12��13���ָʾ����Ca2+�γɾƺ�ɫ����ָʾ�������ʴ���ɫ���������յ�ʱ��ҺΪ����ɫ����pH>13ʱ��ָʾ������Ϊ�ƺ�ɫ������ȷ���յ㡣
3.���ֻ�и���Tָʾ�����ܷ�ⶨCa2+�ĺ�������βⶨ��
�����ֻ�и���Tָʾ����������NaOH��pH>12��ʹMg2+���ɳ�����Ca2+���룬����Mg2+�����Һ��HCl��pH=10���ڼ��백�Ի�����Һ���Ը���TΪָʾ������Mg��EDTA����Һ�ζ�Ca2+�ĺ�����
ʵ��� Ǧ������Һ��Ǧ���麬���������ⶨ
˼���⣺
1.����ʵ��������ζ�Bi3+����ʼ����Ƿ��ζ�Bi3+�������ȣ��ζ���Bi3+���յ�ʱ����Һ�����Ϊ���٣���ʱ�ڼ���10mL200g·L-1�����Ļ��İ�����ҺpHԼΪ���٣�
�𣺰���ʵ��������ζ�Bi3+����ʼ���û�г����ζ�Bi3+�������ȡ����ŵζ��Ľ�����ҺpH��1������10mL200g·L-1�����Ļ��İ�����Һ��pH=5��6��
2.�ܷ�ȡ���������Һ���ۣ�һ�ݿ���pH��1.0�ζ�Bi3+����һ�ݿ���pHΪ5��6�ζ�Bi3+��Pb2+������Ϊʲô��
�𣺲�����pHΪ5��6ʱ�ζ�Bi3+��Pb2+��������Ϊ����Һ��pHΪ5��6ʱ��Bi3+ˮ�⣬����ȷ�ζ���
3.�ζ�Pb2+ʱҪ������ҺpHΪ5��6��Ϊʲô���������Ļ��İ�������������ƣ�
����ѡ����Һʱ������Ҫ�������Ļ��巶Χ����������Ҫע���������ĸ���Ӧ���ٵζ�Pb2+ʱ������NaAc�����ʱ��Ac-����Pb2+�γ�����Ӱ��Pb2+��ȷ�ζ��������������Ļ��İ�����ȡ�
ʵ��� ���Ͻ����������IJⶨ
˼���⣺
1.Ϊʲô�ⶨ�������е�Al3+�÷��ζ������ɣ����ⶨ���������е�Al3+��������û��ζ�����
������������������������٣�����һ��������������һ��������EDTAʱֻ��Al3+�γ������ӣ���������EDTA����ȷ���ζ������������н������ӵ�����϶࣬���������ƣ������EDTA��ֻ�Ǻ�Al3+��Ӧ����Ҫ���������ӷ�Ӧ�����ԾͲ�����ʣ���EDTAֱ�Ӽ���Al3+�ĺ���,����Ҫ���û�����Al3+��ϵ�EDTA����˲ⶨ���������е�Al3+ ����������û��ζ�����
2.�÷��ζ����ⶨ�������е�Al3+ʱ�����������EDTA��Һ��Ũ���Ƿ����ȷ��Ϊʲô��
�𣺼����EDTA��Һ��Ũ�ȱ���ȷ�����Ũ�Ȳ�ȷ�����������Al3+��Ӧ������
3.��ʵ����ʹ�õ�EDTA��ҺҪ��Ҫ�궨��
�𣺱�ʵ���в����û��ζ����ⶨAl3+�ĺ������������Zn2+����Һ�������Ũ�ȼ���������Al3+�ĺ���������ʹ�õ�EDTA��Һ��Ҫ�궨��
4.Ϊʲô���������EDTA����һ����Zn2+����Һ�ζ�ʱ�����Բ��������ĵ����������ʱ�Ƿ���ȷ�ζ���Һ�ɻ�ɫ��Ϊ�Ϻ�ɫ��Ϊʲô��
�����һ���ǵζ�������EDTA��Ҳ��δ��Al3+��Ӧ��EDTA�����Կ��Բ��������������ȷ�ζ���Һ�ɻ�ɫ��Ϊ�Ϻ�ɫ��������Һ�л���ʣ��EDTA��ʹ���ƫ�ߡ�
ʵ��ʮ ������ر���Һ�����ƺͱ궨
˼���⣺
1.����KMnO4����Һʱ��ΪʲôҪ��KMnO4��Һ���һ��ʱ�䲢�������죿��õ�KMnO4��ҺΪʲôҪ���˺���ܱ��棿����ʱ�Ƿ��������ֽ��
����KMnO4�Լ��г���������MnO2���������ʣ�����ˮ�г���������ԭ������������������ʹKMnO4��ԭΪMnO(OH)2������������MnO2��MnO(OH)2���ܽ�һ���ٽ�KMnO4��Һ�ֽ⡣��ˣ�����KMnO4����Һʱ��Ҫ��KMnO4��Һ���һ��ʱ�䲢�������죬�û�ԭ��������ȫ��Ӧ�����ײ���©�����ˣ���ȡMnO2��MnO(OH)2��������ɫƿ�С�
2.���ƺõ�KMnO4��ҺΪʲôҪʢ������ɫƿ�б��������û����ɫƿ��ô�죿
����Mn2+��MnO2�Ĵ�����ʹKMnO4�ֽ⣬����ֽ���졣����.���ƺõ�KMnO4��ҺҪʢ������ɫƿ�б��档���û����ɫƿ��Ӧ���ڱܹ���档
3.�ڵζ�ʱ��KMnO4��ҺΪʲôҪ������ʽ�ζ����У�
����KMnO4��Һ���������ԣ���ʹ��ʽ�ζ����¶���Ƥ�����������Եζ�ʱ��KMnO4��ҺҪ������ʽ�ζ����С�
4.��Na2C2O4�궨KMnO4ʱ��Ϊʲô������H2SO4�����н��У���ȹ�������к�Ӱ�죿������HNO3��HCl���������ΪʲôҪ���ȵ�70��80�棿��Һ�¶ȹ�������к�Ӱ�죿
��������HCl�����ʱ��Cl-���л�ԭ�ԣ�����KMnO4���á�����HNO3�����ʱ��HNO3���������ԡ�����ֻ����H2SO4�����н��С��ζ�������ǿ������Һ�н��У�����ȹ���KMnO4�뱻�ζ����������ɺ�ɫ��MnO(OH)2��������Ӧ���ܰ�һ���ļ�����ϵ���С��������£�KMnO4��Na2C2O4֮��ķ�Ӧ�ٶ��������뽫��Һ���ȵ�70��80�棬���¶Ȳ��ܳ���90�棬����Na2C2O4�ֽ⡣
5.�궨KMnO4��Һʱ��Ϊʲô��һ��KMnO4�������Һ�ĺ�ɫ��ȥ���������Ժ��ɫ��ȥԽ��Խ�죿
������KMnO4Na2C2O4�ķ�Ӧ�ٶȽ�������һ��KMnO4���룬������Һ��û��Mn2+����Ӧ�ٶ�������ɫ��ȥ���������ŵζ��Ľ��У���Һ��Mn2+��Ũ�Ȳ�����������Mn2+�Ĵ����ã���Ӧ�ٶ�Խ��Խ�죬��ɫ��ȥҲ��Խ��Խ�졣
6.ʢ��KMnO4��Һ���ձ�����ƿ���������ýϾú�����ϳ�����ɫ�������ʲô������ɫ��������ͨ������������ϴ����Ӧ����ϴ�Ӳ��ܳ�ȥ�˳�����
����ɫ������ΪMnO2��MnO(OH)2���˳�������������Բ���������ǰ�ϴ��Һϴ�ӡ�
ʵ��ʮһ ������ط��ⶨ��������ĺ���
˼���⣺
1.�ø�����ط��ⶨH2O2ʱ���ܷ���HNO3��HCl��������ȣ�
���ø�����ط��ⶨH2O2ʱ��������HCl��HNO3��������ȣ���HCl���л�ԭ�ԣ�HNO3���������ԡ�
2.�ø�����ط��ⶨH2O2ʱ��Ϊ�β���ͨ�����������ٷ�Ӧ��
����H2O2�ڼ���ʱ�ֽ⣬�����ø�����ط��ⶨH2O2ʱ������ͨ�����������ٷ�Ӧ��
ʵ��ʮ�� ���̿���MnO2�����IJⶨ
˼���⣺
1.ΪʲôMnO2������KMnO4����Һֱ�ӵζ���
����MnO2��һ�ֽ�ǿ�������������Բ�����KMnO4����Һֱ�ӵζ���
2.�ø�����ط��ⶨ���̿��е�MnO2�ĺ���ʱ��Ӧע�������Щʵ������������Ʋ��ã���������ʲô�����
��Ӧ��H2SO4������Һ��ȣ���Ȳ��ܹ��ͣ�����KMnO4����MnO(OH)2��������Һ���¶�Ӧ������70��80�棬������90��������Na2C2O4�ֽ⡣
ʵ��ʮ�� SnCl2-HgCl2-K2Cr2O7���ⶨ����ʯ��
���ĺ������й�����
˼���⣺
1.��Ԥ����ʱΪʲôSnCl2��ҺҪ������μ��룬��HgCl2��ҺȴҪ��ȴ��һ�μ��룿
����SnCl2��ԭFe3+ʱ����Һ���¶Ȳ���̫�ͣ�����Ӧ�ٶ�������ɫ��ȥ���۲죬ʹSnCl2����̫��׳�ȥ��������Һ�У�Hg2+��������Fe2+���������ڼ���HgCl2ǰ��ҺӦ��ȴ�����¡�
2.�ڵμ�ǰ����H3PO4��������ʲô������H3PO4��ΪʲôҪ�����ζ���
�������ŵζ��Ľ��У�Fe(��)��Ũ��Խ��Խ��FeCl-4�Ļ�ɫ�������յ�Ĺ۲죬����H3PO4��ʹFe3+������ɫ��Fe(HPO4)-2�����Ӷ�������ͬʱ����Fe(HPO4)-2�����ɣ�������Fe3+/Fe2+��Եĵ�λ��ʹ��ѧ�����㸽���ĵ�λͻԾ����ָʾ�������������Ƶı�ɫ������ͻԾ��Χ֮�ڣ�����˵ζ���ȷ�ȡ���H3PO4��Һ������Եĵ缫��λ���ͣ�Fe2+���ױ��������ʲ�Ӧ���ö�Ӧ�����ζ���
ʵ��ʮ�� SnCl2-TiCl3-K2Cr2O7���ⶨ����ʯ��
�������������
˼���⣺
1.��Ԥ����ʱΪʲôSnCl2��ҺҪ������μ��룿
����SnCl2��ԭFe3+ʱ����Һ���¶Ȳ���̫�ͣ�����Ӧ�ٶ�������ɫ��ȥ���۲죬��ʹSnCl2������
2.��Ԥ��ԭFe(��)��Fe(��)ʱ��ΪʲôҪ��SnCl2��TiCl3���ֻ�ԭ����ֻʹ������һ����ʲôȱ�㣿
�𣺶�����ԭFe(��)ʱ�����ܵ�����SnCl2����SnCl2���ܻ�ԭW(��)��W(��)����ָʾԤ��ԭ�յ㣬�����ȷ��������������������SnCl2��û���ʵ���������������Ҳ���ܵ�����TiCl3��ԭFe(��)��������Һ���������϶�����Σ�����ˮϡ��ʱ������Ti(��)��ˮ�����ɳ�����Ӱ��ⶨ����ֻ�ܲ���SnCl2-TiCl3����Ԥ��ԭ����
3.�ڵζ�ǰ����H3PO4��������ʲô������H3PO4��Ϊʲô�����ζ���
�������ŵζ��Ľ��У�Fe(��)��Ũ��Խ��Խ��FeCl-4�Ļ�ɫ�������յ�Ĺ۲죬����H3PO3��ʹFe3+������ɫ��Fe(HPO4)-2�����Ӷ�������ͬʱ����Fe(HPO4)-2�����ɣ�������Fe3+/Fe2+��Եĵ�λ��ʹ��ѧ�����㸽���ĵ�λͻԾ����ָʾ�������������Ƶı�ɫ������ͻԾ��Χ֮�ڣ�����˵ζ���ȷ�ȡ���H3PO4��Һ������Եĵ缫��λ���ͣ�Fe2+���ױ��������ʲ�Ӧ���ö�Ӧ�����ζ���
ʵ��ʮ�� I2��Na2S2O3����Һ�����Ƽ��궨
˼���⣺
1.������ƺͱ���I2��Һ������I2��ҺʱΪʲôҪ�μ�KI��
����I2����ˮ��������KI��Һ�У���ϡ��KI��Һ���ܽ�Ҳ������������ʱ�Ƚ�I2�ܽ��ڽ�ŨKI����Һ�У����ϡ�͵�����Ũ�ȡ���������ɫƿ�С�
2.������ƺͱ���Na2S2O3��Һ?
��ˮ�е�CO2��ϸ�����ն���ʹ��ֽ⣬ˮ�е���Ҳ�ܽ���������������Na2S2O3��Һʱ���Ƚ�����ˮ��У��Գ�ȥˮ�е�CO2��O2����ɱ��ϸ������ȴ���������Na2CO3ʹ��Һ��������������Na2S2O3�ķֽ��ϸ������������������ɫƿ�С�
3.��K2Cr2O7�������ʱ궨Na2S2O3��Һʱ��ΪʲôҪ���������KI��HCl��Һ��ΪʲôҪ����һ��ʱ�����ܼ�ˮϡ�ͣ�Ϊʲô�ڵζ�ǰ��Ҫ��ˮϡ�ͣ�
��Ϊ��ȷ��K2Cr2O7��Ӧ��ȫ�����������Һ�����Ϊ0.2-0.4moL·l-1HCl��Һ�����������KI��K2Cr2O7��KI�ķ�Ӧ��һ����ʱ����ܽ��еñȽ���ȫ���������5min���ڼ�ˮϡ�ͣ�������ȣ��Է�ֹNa2S2O3�ڵζ���������ǿ����ֽ⡣
4.�궨I2��Һʱ���ȿ�����Na2S2O3�ζ�I2��Һ��Ҳ������I2�ζ�Na2S2O3��Һ���Ҷ����õ���ָʾ����������������¼������ָʾ����ʱ���Ƿ���ͬ��Ϊʲô��
�������Na2S2O3�ζ�I2��Һ�����������I2������Ӧ�ζ�����Һ��ǰ��ɫʱ�ټ������ָʾ���������I2�ζ�Na2S2O3��Һʱ��Ӧ��ǰ������ۣ������ι�����
ʵ��ʮ�� ��ӵ������ⶨͭ���е�ͭ
˼���⣺
1.��ʵ�����KI��������ʲô��
�𣺱�ʵ���еķ�ӦʽΪ��
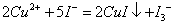
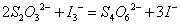
��������Ӧ���Կ�����I-������Cu2+�Ļ�ԭ��������Cu+�ij�������I-����ϼ���
2.��ʵ��ΪʲôҪ����NH4SCN��Ϊʲô���ܹ���ؼ��룿
����CuI������������I2���ⲿ��I2���ܱ��ζ�������ɽ��ƫ�͡�����NH4SCN��Һ��ʹCuIת��Ϊ�ܽ�ȸ�С��CuSCN����CuSCN������I2�Ӷ�ʹ���������Dz���I2�ͷų���������˲ⶨ��ȷ�ȡ���Ϊ�˷�ֹI2��SCN-����������NH4SCNӦ���ٽ��յ�ʱ���롣
3.�������к����������������Լ����������Բⶨͭ�ĸ��Ų�������ҺpHֵ��
���������к��������ɼ���NH4HF2���ڱ�Fe3+��ͬʱ����HF��F-�Ļ������ÿ�����Һ�����ΪpH=3-4��
ʵ��ʮ�� �������ⶨ�����ǵĺ���
˼���⣺
ʲô������������ʱ�μ�NaOH���ٶ�Ҫ�����Ҽ����Ҫ����һ��ʱ�䣿�����ữ����Ҫ������Na2S2O3����Һ�ζ���
��IO-������������ʱ�μ�NaOH���ٶ�Ҫ�������������IO-���������������Ƿ�Ӧ���绯Ϊ�����Խϲ��IO3-�����ܵ��������Dz�����ȫ���������ڼ�����Һ�����ɵ�IO3-��I-���ữʱ������I2����I2�ӷ��������ữ��Ҫ�����ζ���
ʵ��ʮ�� ���������������Ⱥ����IJⶨ��Ī������
˼���⣺
1.���ƺõ�AgNO3��ҺҪ������ɫƿ�У������ڰ�����Ϊʲô��
��AgNO3����ֽ�,�����ƺõ�AgNO3��ҺҪ��������ɫƿ��,�����ڰ���.
2.���հײⶨ�к����壿
�����հײⶨ��Ҫ�ǿ۳�����ˮ�е�Cl-������AgNO3����Һ�������ʹ�ⶨ�����ȷ.
3.�ܷ���Ī������NaCl����Һֱ�ӵζ�Ag+��Ϊʲô��
��Ī��������������NaCl����Һֱ�ӵζ�Ag+����Ϊ��Ag+��Һ�м���ָʾ��KCrO4�ͻ���������Ag2CrO4��������NaCl����Һ�ζ�ʱ��Ag2CrO4��ת���ɵ�AgCl���ٶȼ�����ʹ�յ��Ƴ١�
4.K2Cr2O7��Һ��Ũ�ȴ�С���������ٶԲⶨ����к�Ӱ�죿
��K2Cr2O7��Ũ�ȱ������,��̫�������յ���ǰ����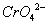 �����Ļ�ɫ��Ӱ���յ�Ĺ۲죻��̫С�ֻ�ʹ�յ��ͺ���Ӱ��ζ���ȷ�ȡ����ݼ��㣬�յ�ʱ
�����Ļ�ɫ��Ӱ���յ�Ĺ۲죻��̫С�ֻ�ʹ�յ��ͺ���Ӱ��ζ���ȷ�ȡ����ݼ��㣬�յ�ʱ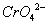 ��Ũ��ԼΪ5×10-3 mol/LΪ�ˡ�
��Ũ��ԼΪ5×10-3 mol/LΪ�ˡ�
ʵ��ʮ�� ���Ͻ����������IJⶨ��������·���
˼���⣺
1.�÷�����·��ⶨAg+���ζ�ʱΪʲô�������ҡ����
���÷�����·��ⶨAg+ʱ��Ϊ��ֹAgSCN��Ag+��������������յ��������ڵζ�ʱҪ����ҡ��
2.������·��ܷ����FeCl3��ָʾ����
������ֱ�ӵζ�ʱ��Cl-����Һ�б��ζ���Ag+����AgCl�������ڷ��ζ����У������FeCl3��ָʾ��ʱ������Һ������Cl-��������������¶�������յ������Է�����·����ܲ���FeCl3��ָʾ����
3.�÷��ζ����ⶨCl-ʱ���Ƿ�Ӧ�þ���ҡ����Ϊʲô��
���÷��ζ����ⶨCl-ʱ����Ӧ�þ���ҡ������ΪAgSCN���ܽ�ȱȴ�ʣ���Ag+���ζ���Ϻ���SCN-����AgCl��������ת����Ӧ��ʹAgCl�����ܽ⣬�յ��ɫ�Ƴٳ��֡��������ҡ���ͻ�������������ķ�������˲��ܾ���ҡ��
ʵ���ʮ �����б������IJⶨ��������������
˼���⣺
1.����BaSO4ʱΪʲôҪ��ϡ��Һ�н��У����Ͻ����Ŀ����ʲô��
�𣺳���BaSO4ʱҪ��ϡ��Һ�н��У���Һ����Ա��ͶȲ���̫�����ľ���Ҳ����̫�࣬�������������ɴִ�Ľᾧ���������Ͻ����Ŀ���ǽ������Ͷȣ�����ֲ�Ũ�ȹ��ߵ�����ͬʱҲ�������ʵ���������
2.Ϊʲô����BaSO4ʱҪ������Һ�н��У�������Ȼ��ȴ����й��ˣ����ȹ��˻�ǿ����ȴ�ò��ã�
�𣺳���Ҫ������Һ�н��У�ʹ�������ܽ���������ӣ��������Խ�����Һ�Ĺ����Ͷȣ����������ɴִ�Ľᾧ������ͬʱ���Լ��ٳ��������ʵ�������Ϊ�˷�ֹ����������Һ�е���ʧ��Ӧ���ڳ���������Ϻ���Һ��ȴ�����£�Ȼ���ٽ��й��ˡ�
3.ϴ�ӳ���ʱ��Ϊʲô��ϴ��ҺҪ��������Σ�Ϊ��֤BaSO4�������ܽ���ʧ������0.1%��ϴ�ӳ�����ˮ�����������ٺ���/
��Ϊ��ϴȥ�������������������ʺͲ�����ĸҺ����ô����ij�������ϴ���в��ɱ����Ҫ��ɲ��ֳ������ܽ⡣��ˣ�ϴ�ӳ���Ҫ�����ʵ��ķ��������ϴ��Ч�ʣ������ܵؼ��ٳ������ܽ���ʧ������ͬ�����ϴ��ҺӦ�ֶ��ϴ�ӣ�ÿ����15-20mLϴ��Һ��
4.��ʵ����Ϊʲô��ȡ0.4-0.5g BaCl2·2H2O��������������������ʲôӰ�죿
�������ȡ�������࣬�������ʹ����ʺͲ���ĸҺ��ϴ�ӣ���ȡ�������٣����������٣�ϴ����ɵ���ʧ�ʹ�
ʵ���ʮһ �Ͻ�����������IJⶨ������ͪ���������
˼���⣺
1.����ͪ��������ⶨ��ʱ��Ӧע����Щ����������Ϊʲô����ʵ����BaSO4����������Щ��֮ͬ����ͨ����ʵ�飬����л����������ص�����Щ��ʶ��
��ϴ������Ϊ��1�����ʯ���ڱ�Cu2+��Fe3+��Cr3+��2������ҺpHΪ8-9����pH���ߣ���D2-�϶��⣬Ni2+�백�γ����������ӣ�ʹ����ͪ��������ܽ⣻3ˮԡ�����¶���70��80��,�ɼ���Cu2+��Fe3+��������
��ʵ��ֻ��������ˡ�ϴ�ӡ�����ٳ�������BaSO4������Ҫ̿�������ա�
�л���������1.ѡ���Ժã�2.�������ܽ��С�������ڱ�����ֵij�����ȫ��3.�����ļ���С�����������٣���ýϴ����ij�����4.����������ʽ��Ħ�������������ڼ��ٳ�������߷��������ȷ�ȣ������ڳ�������ֺ㶨������ɺ�������������������IJ�����
2.�����ʯ���������ʲô�����������������ϡ�͵�Ŀ�ĺ��ڣ�
�𣺼����ʯ����Ϊ���ڱ�Cu2+��Fe3+��Cr3+����Cu2+��Cr3+�붡��ͪ����ɿ�������������������ij��������ҹ���������Ҳ�����ء���ˣ��ɶ����һЩ������������Һϡ�͡�
ʵ���ʮ�� ��ͭ����Ĺ��������뼰�����IJⶨ
˼���⣺
1.���ù��������������ֽ��з���������ŵ�����Щ����ʵ��������������MnO(OH)2�����û�����ʲô��
�����л�������������������ֽ��з���������ŵ��ǣ�1.���нϸߵ�ѡ���ԣ�2.���ɵij����ܽ��С��3.������Ⱦ��
��ʵ�����и���Һ�м���MnSO4��KMnO4��Һ��к�����MnO(OH)2��ͬʱ��Һ�е�Bi3+��MnO(OH)2����������ͭ���롣
2.��ϱ�ʵ��˵����߳�������ѡ���Ե�;������Щ��
�����ù�����������������ʱ���ڲ�����Ӧ���ݾ���Ҫ�� ѡ�����˵Ĺ��������ͳ������������ﵽ���������Ŀ�ġ�
3.��ȡ������IJ���Ӧע����Щ���
��1.���������Һ��ȫϴ���Һ©����2.ÿ��һ���Լ�����ҡ�ȣ�3.�����CHCl3���Ҫȷ��4.�����ʹ����������ȫ��CHCl3��ȡ��5.һ��Ҫ��ȥ��ȡҺ�е�ˮ�֡�
ʵ���ʮ�� �Ͻ������ͭ����ȡ��Ȳⶨ
˼���⣺
1.�ܷ�����Ͳ����CHCl3��Ϊʲô��
�𣺲�������Ͳ����CHCl3����ʵ��Ҫ��������Ҫȷ�������Ӱ����ȡ���Ũ�ȡ�
2.�ܷ�����Ũ��ˮ������ҺpH8��9��EDTA������Fe3+��Co2+��Ni2+�ĸ��ţ�Ϊʲô��
�𣺲�������Ũ��ˮ������ҺpH8��9���ټ�EDTA������Fe3+��Co2+��Ni2+�ĸ��š���Ϊ��ʱFe3+�����ɳ��������ڱε�Ч����
ʵ���ʮ�� ���ӽ�����֬���������IJⶨ
˼���⣺
1.ʲô�����ӽ�����֬�Ľ������������ֽ��������IJⶨԭ����ʲô��
�𣺽���������ָÿ�˸���֬���ܽ������൱��һ�����ӵ����ʵ�����
���������IJⶨԭ�����������ӽ��������IJⶨ������ȷ��ȡһ��������������ӽ�����֬��������ƿ�С�Ȼ�����һ�����ҹ���NaOH�ı���Һ����������24h��ʹ��֬���Ի����е�H+ȫ����Na+����������HCl����Һ���ζ�ʣ���NaOH����
�����ӽ�������=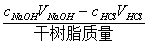
�����ӽ�����������෴��
2.Ϊʲô��֬�㲻�ܴ��������ݣ�����������δ�����
�������֬���д���������ʱ����Һ����֬����ֽӴ��������ʹﲻ�������Ľ������������Ӧ�������������ɡ�
3.����������֬������װ����Ӧ�ֱ�ע��ʲô���⣿
�������ӽ�����֬�������ӽ�����֬����ʱ��ͨ����4mol/LHCl��Һ����1��2�죬���ܽ�������ʣ�Ȼ��������ˮϴ�������ԣ�����ˮ�б��á�
װ��ʱ���������¶���һ�㲣����ά����������ˮ���ٵ����ˮ����֬��ʹ��֬�Զ��³����γɽ����㡣��֬�ĸ߶�һ��ԼΪ���ߵ�90%��Ϊ��ֹ���Լ�ʱ��֬�����������϶�Ӧ��һ�㲣����ά�������������Һ���Ը�����֬���Է�ֹ��֬���Ѷ��������ݡ�
ʵ���ʮ�� ��þ����������ӽ�������ͺ����IJⶨ
˼���⣺
1.�������ӽ���������þ����Һ�����ԭ����
����þ����NaOH���ڷ�����ֽ⣬����HCl�ܽ��ۿ顣����������ʽ����������β��ܲ������롣Ȼ���������ӽ�����������ȥ�������ȸ��������ӣ�����������ʽ��������Һ�У���һ���������²ⶨ��
2.���ӽ���ǰ��ΪʲôҪ��ǿ���Եĺ�����Һ������pH=2��3����������pH��
�𣺽�������ȫ����ʹ���ƫ�ߡ��������������ӽ���������ҺӦ����pH=2��3Ϊ�ˡ�����NaOH��Һ�к������ԣ�����ϡHCl�ữ����Һ��pH=2��3��
3.Ϊʲô�����ӽ����������Һ��pH������5��6����ε���pH��
�����ڽ���������H+����Ũ��Խ��Խ��ʹ����Һ���������������Ҫһ������NaOHʹ���ƫ�ߡ������ڵζ�ǰ��������Һ�м������ָʾ������NaOH�к�����Һ�ʻ�ɫ��Ȼ��μ�HCl����ɫ������NaOH����Һ�ζ�����ɫ��ȥ�����ȶ��ijȻ�ɫ����ʱ��ҺpHԼΪ5��6��
4.�����Ǽ����ᣬ��ʵ��Ϊʲô����NaOH����Һ�ζ������ӽ�����������
�������Ǽ����ᣬ�����ü�ֱ�ӵζ�������������Һ�м����¶���ȶ��ǻ���������֮�γ�һ�ֽ�ǿ������ᣬ��KaΪ1×10-6��3×10-5�������Ϳ��ü����Һ�ζ���
ʵ���ʮ�� ֽɫ�շ�����ͼ���������
˼���⣺
1.ʵ��ʱ������ֱָ����ȡ��ֽ���в�����ʵ�����к�Ӱ�죿
��ֽɫ������ֽ��һ��������Ҫ���籡�������ȣ���Ե���룬ƽ�������ۺۣ��������յȡ�ʵ���У��������ֱָ����ȡ��ֽ���в�������ֽ������Ӱ���ճ�����ա��Ӷ�Ӱ��չ��������ֽ�ϵ��ƶ��ٶȣ�ҲӰ���˸���ֵı˴˷���Ŀ�ġ�
2.�����������ֽ�����ڲ���Ͳ�ڣ���ԭ��Ҳ���뵽չ�����У�ʵ������������
�������ԭ��Ҳ���뵽չ�����У�������չ�������������������٣������ͻ�Ӱ����ɫ��
ʵ���ʮ�� ż�����Ͷ����������ı���ɫ����
˼���⣺
1.չ��ʱ��������Ͳ�Dz����ܣ��Ա����������Ӱ�죿Ϊʲô��
�𣺽��������ڱ�����ϣ�����������չ��ʱ��Ӧ�ڱ��͵��ܼ������н��У�����Ӱ�����ֵ�չ�����룬ʹ����ֵ����һ�£��������ж��Լ���
2.���չ��ʱ���������̣��Ի����ķ����к�Ӱ�죿
��������������һ���ij��ȣ���չ��ʱ�����ʱ����ߵ㽫���Ƴ������塣���ʱ����̣�����ֱ˴˷ֲ����������Լ�����
- ��ѧʵ�������������ϰ
- ��ѧʵ���������ʵ�鱨�浥
-
��ѧʵ�鱨�� ʵ��__��ѧʵ���������
ʵ�鱨���������༶��ͬ���ˣ������ɼ�����Ŀ����ѧʵ����������γ̣�ѧ�ţ�һ��ʵ��Ŀ��1.��Ϥʵ���ҹ���ȫ���������¹ʴ�����2��
-
��ѧʵ���������ʵ�鱨�浥
ʵ��һ��ѧʵ��������������꼶�����ον�ʦʵ��Ŀ��1��ʶ��ѧʵ�鳣������2����ҩƷ��ȡ�ü��ȵȻ�������ʵ��������ҩƷ�Թ������ԹܼС�
- ���ﻯѧʵ���������-ʵ�鱨��
-
�ζ���������������ϰ
��ʮһ�¶�����������������ʵ��ʵ����ʮһ�����Һ�����ƺ�Ũ�ȵıȽ�һĿ����Ҫ��1�����ζ��ܵ�ϴ�Ӻ�ʹ�ü��ζ�����ѧ��ȷ��ȷ���յ㡭
- ʵ��3 �ζ���������������ϰ
-
ʵ��һ �ζ���������������ϰ
ʵ��һ������ƽ������ϰʵ��Ŀ��1ѧϰ������ƽ�͵�����ƽ�Ļ��������ʹ�÷���2����ȷ�����淶�ؼ�¼ʵ��ԭʼ���ݵķ���ʵ��ԭ��1���̡�
- ʵ��� �ζ�����������ϰ
-
ʵ��һ �ζ���������������ϰ
ʵ��һ�����Һ�����ƺ�Ũ�ȵıȽ�һĿ����Ҫ��1�����ζ��ܵ�ϴ�Ӻ�ʹ�ü��ζ�����ѧ��ȷ��ȷ���յ�ķ���2����������Һ�����ƺ�Ũ��
- ���л�ѧʵ���ܽ�----ʵ���������