实验三 食醋中总酸度的测定
实验三 食醋中总酸度的测定
总学时:2学时
一、实验目的
1. 熟练掌握滴定管,容量瓶,移液管的使用方法和滴定操作技术
2. 掌握氢氧化钠标准溶液的配制和标定方法
3. 了解强碱滴定弱酸的反应原理及指示剂的选择
4. 学会食醋中总酸度的测定方法
二、实验原理:
食醋中的主要成分是醋酸,此外还含有少量的其他弱酸如乳酸等,用NaOH标准溶液滴定,在化学计量点是呈弱碱性,选用酚酞作指示剂,测得的是总酸度
三、实验仪器及试剂
1. 滴定常用玻璃仪器
2. 邻苯二甲酸氢钾
3. NaOH标准溶液
4. 酚酞指示剂
四、实验提示:
1. 食醋中醋酸的浓度较大,且颜色较深,故必须稀释后在进行滴定
2. 测定醋酸含量时,所用的蒸馏水不能含有二氧化碳,否则会溶于水中生成碳酸,将同时被滴定
五、思考题:
1. 醋酸时为什么要用酚酞作指示剂?
2. 该方法的测定原理是什么?
六、教学实施经验小记
在学习完酸碱滴定法以后,做该实验来对所讲的知识进行实践操作,同学们在实验中主要存在的问题是对终点的判断。
分析化学实验报告
班级 _________ 姓名___________ 报告日期_____________
实验三 食醋中总酸度的测定
一、NaOH溶液浓度的标定
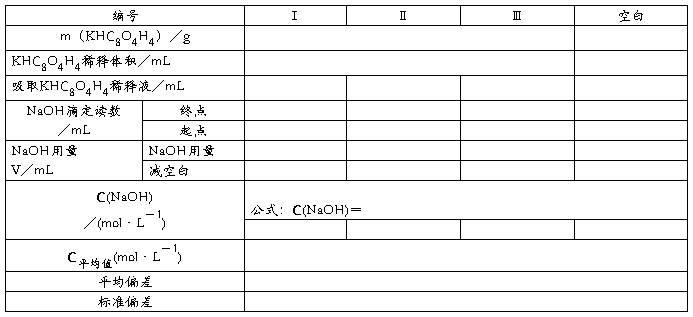
二、食醋总酸度的测定

结果与讨论:
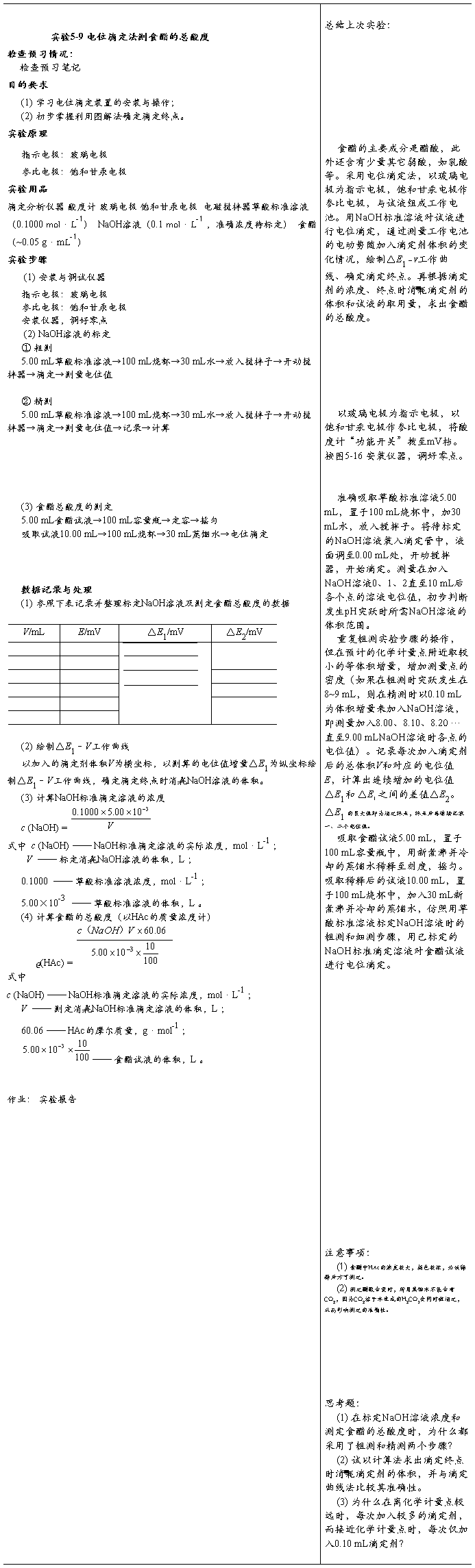
第二篇:电位滴定法测食醋的总酸度
-
食醋中总酸量的测定实验报告
食醋中总酸量的测定姓名学号20xx级化学四班实验小组邮箱一实验目的1初步学会用传感器技术测定食醋中的总酸量2会组织中学生用传感器技…
-
实验3 食醋中总酸度的测定方法
食醋中总酸量的测定扬州大学化学化工学院张磊091301223一实验目的1熟练掌握滴定管容量瓶移液管的使用方法和滴定操作技术2掌握氢…
-
实验三 食醋中总酸度的测定
实验三食醋中总酸度的测定总学时2学时一实验目的1熟练掌握滴定管容量瓶移液管的使用方法和滴定操作技术2掌握氢氧化钠标准溶液的配制和标…
- 实验四 食醋中总酸度的测定
-
食用醋酸总酸量的测定-实验报告模板
一实验目的1学习碱溶液浓度的标定方法2进一步练习滴定操作及天平减量法称量3学会用标准溶液来测定未知物含量4熟悉移液管吸量管和容量瓶…
-
食醋中总酸量的测定实验报告 (1)
食醋中总酸量的测定孟娟20xx级化学3班14小组4120xx49一实验目标1初步学会用传感器技术测定食醋中的总酸量2会组织中学生用…
-
食醋中总酸量实验报告1
食醋中总酸量的测定一实验目的1学习食醋中总酸度的测定方法2了解传感器技术在中学实验中的应用二实验原理待测的食醋中醋酸及其他有机酸可…
-
食醋中总酸量的测定实验报告
食醋中总酸量的测定梁建林4100711820xx级化学3班1号实验小组电话187xxxxxxxx一实验目标1初步学会用传感器技术测…
-
食醋中总酸量的测定实验报告
实验六食醋中总酸量的测定20xx级化学1班1223实验室一实验目的1初步学会用传感器技术测定食醋中的总酸量2会组织中学生用传感器技…
-
食醋中总酸含量的测定
食醋中总酸含量的测定黄岩中学周元勇二基本的操作要求食醋总酸含量的测定实验操作要求基本上等同于老教材的中和滴定实验中和滴定实验的过程…
-
食醋中总酸量的测定实验报告
食醋中总酸量的测定姓名学号20xx级化学四班实验小组邮箱一实验目的1初步学会用传感器技术测定食醋中的总酸量2会组织中学生用传感器技…