乙酰水杨酸的制备与纯化

设计性实验报告
题 目: 乙酰水杨酸的制备与纯化
课程名称: 有机化学实验
姓 名:
学 号: 2009122112
系 别: 化学系
专 业: 应用化学
班 级: 093班
实验学期: 2011 至 2012 学年 第一 学期
乙酰水杨酸的制备与纯化
﹙化学系, 应用化学,093班,学号2009122112﹚
摘要 本次实验的目的是熟悉酰化反应的原理和实验操作方法,并且学会用重结晶的方法提纯有机物。实验中,将水杨酸与乙酐作用,以浓硫酸作催化剂,通过乙酰化反应制得到乙酰水杨酸,再分别加入饱和碳酸钠水溶液和20%的盐酸进行粗产品的纯化。该实验方法简便易行且实验原料容易得到,得到的产品纯度较高,基本符合制备要求。
关键词 酰化反应,乙酰水杨酸,制备,纯化
1 引言
乙酰水杨酸, 通常称为阿斯匹林(aspirin),是由水杨酸(邻羟基苯甲酸)和乙酸酐合成的。早在十八世纪,人们已从柳树皮中提取了水杨酸,注意到它可以作为止痛、退热和抗炎药,不过对肠胃刺激作用较大。水杨酸是1838年第一次由强碱作用于相应的醛后经酸化得到的一种化合物。1859年Kolbe使用干燥的苯酚钠盐粉末和二氧化碳在4—7atm(1atm=101.325kPa)下进行反应,制备成水杨酸,现在工业上都用Kolbe合成法生产。直到目前,阿斯匹灵仍然是一个广泛使用的具有解热止痛作用、用于治疗感冒的药物。常用于治疗风湿病和关节炎。近年来还发现阿斯匹林能抑制血小板凝聚,可防止血栓的形成。
水杨酸是一种具有双官能团的化合物,一个是酚羟基,一个是羧基。能进行两种不同的酯化反应,而且还可以形成分子内氢键,阻碍酰化和酯化反应的发生。当与乙酸酐反应时,可以得到乙酰水杨酸,即阿斯匹林;如与过量的甲醇反应,生成水杨酸甲酯,它是第一个作为冬青树的香味成分被发现的,因此通称为冬青油。
阿斯匹林又名乙酰水杨酸,分子式:C9H8O4,分子量为:180.16,是白色针状结晶或结晶性粉末。熔点:135℃,PKa=2.98,其酸性比苯甲酸强,微溶于水,易溶于乙醇、氯仿、乙醚及碱液等。其分子内的羟基和羧基都可以进行酯化反应。本实验用乙酸酐对水杨酸的酚羟基进行酰化制备乙酰水杨酸,即阿斯匹林。
乙酰水杨酸(阿斯匹林)的相关光谱图:
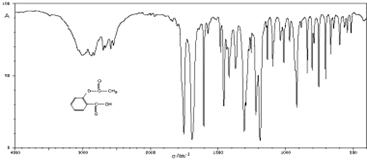
乙酰水杨酸的红外光谱图
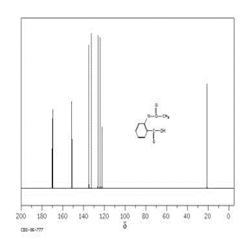
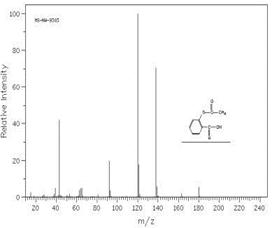
乙酰水杨酸的核磁共振碳谱图 乙酰水杨酸的质谱图
乙酰水杨酸(阿斯匹林)的应用价值:
阿司匹林英文名称:aspirin 其他名称:乙酰水杨酸,醋柳酸。适应症:阿司匹林是使用最多、使用时间长的解热、镇痛和消炎药物,能抑制体温调节中枢的前列腺素合成酶,使前列腺素(pge1)合成、释放减少,从而恢复体温中枢的正常反应性,使外周血管扩张并排汗,使体温恢复正常。本品尚具抗炎、抗风湿作用,并促进人体内所合成的尿酸的排泄,对抗血小板的聚集。适用于解热,减轻中度疼痛如关节炎、神经痛、肌肉痛、头痛、偏头痛、痛经、牙痛、咽喉痛、感冒及流感症状
经过查阅资料,可知利用不同的催化剂均可以制备乙酰水杨酸。总结如下:
1.1 方案一:苯甲酸钠催化法
温热条件下,使水杨酸、乙酸酐和苯甲酸钠混合物全部溶解后,低速匀速搅拌,在适当水浴加热反应一定时间。反应结束后,加入冰水,并置于冰水浴中冷却。晶体析出完全后抽滤得乙酰水杨酸粗产品。加入饱和碳酸氢钠溶液,搅拌,过滤,将得到的滤液缓慢倒入盛有浓盐酸的烧杯中,把烧杯置冰水浴中充分冷却得到乙酰水杨酸产品。[2]
反应式如下:
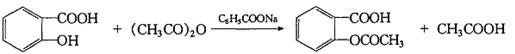
1.2 方案二:对甲苯磺酸催化法
在干燥的锥形瓶中依次加入定量的水杨酸,乙酸酐和对甲苯磺酸,充分摇动。水浴上加热,待水杨酸溶解后,保持瓶内温度在81~85℃(或热水浴水温在85℃左右),磁力搅拌。反应结束后,加入定量的蒸馏水,并用冰水冷却,抽滤得乙酰水杨酸粗品。粗产品用乙醇—水混合溶剂重结晶,得到白色晶体即为纯乙酰水杨酸。[3]
反应方程式:

1.3 方案三:浓硫酸(或浓磷酸)催化法
将水杨酸、乙酸酐和浓硫酸混合物置于热水浴中加热。反应结束后,加入水,放在冷水浴中冷却,抽滤得乙酰水杨酸粗产品。在粗产品中加入饱和碳酸氢钠水溶液,向抽滤得到的滤液中加入20%盐酸,并置于冰水浴中,抽滤。取少量乙酰水杨酸,用1%三氯化铁溶液鉴定水杨酸是否存在。如存在,产物可用乙醇-水混合溶剂重结晶得到纯的乙酰水杨酸。 [4]
反应方程式:

方案选择:这三种方案都较简单,本次试验采用方案三,原因如下:方案一所采用的为有机催化剂,且浓盐酸具有挥发性,对人体有害;方案二也是采用有机催化剂,并且须用水浴保持温度,操作稍显复杂;方案三仍需采用水浴加热,但采用无机催化剂,对人体危害较小,且步骤较少,实验原料容易得到。因此本次实验采用方案三制备乙酰水杨酸。
2 实验原理
水杨酸是一种具有双官能团的化合物,一个是酚羟基,个是酸酸基。羟基和羧酸基都会发生酯化,而且还可以形成分子内氢键,阻碍酰化和酯化反应的发生。将水杨酸与乙酐作用,通过乙酰化反应,使水杨酸分子中酚羟基上的氢原子被乙酰基取代生成乙酰水杨酸。加入少量浓硫酸作催化剂,其作用是破坏水杨酸分子中羧基与酚羟基间形成的氢键,从而使酰化反应容易完成。
反应方程式为:
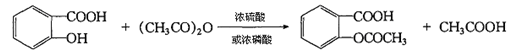
副反应方程式为:
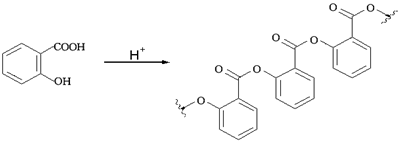

此实验可能的副产物:乙酰水杨酸酐,水杨酸,乙酰苯脂,水杨酸苯脂,乙酰水杨酸苯脂。
物理常数
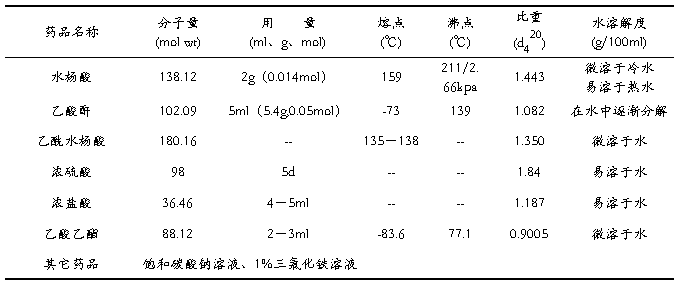
3 实验用品
3.1 仪器:三角烧瓶(100mL)、温度计(250℃)、烧杯(100mL)、布氏漏斗、吸滤瓶、水泵、量筒、台秤、安全瓶、表面皿、试管、玻璃棒
3.2 液体试剂:乙酐5mL(约0.05mol)、浓硫酸、饱和碳酸钠水溶液、20%盐酸10mL、95%乙醇、0.06mol/L三氯化铁溶液
3.3 固体药品:水杨酸2g(约0.016mol)
3.4 材料:水,滤纸
4 实验步骤

4.1 乙酰水杨酸的制备
在锥形瓶中依次加入2g干燥的水杨酸、5 mL乙酐、10滴浓硫酸,充分振荡使水杨酸溶解,在80℃水浴加热20分钟,并且不断振荡。在室温中冷却后,加入5 mL水,且边加边振摇。注意:此过程反应放热,操作时应小心。将上述锥形瓶放在冷水浴中冷却,使晶体完全析出(约需5min),抽滤,并用少量冷水洗涤,抽干,即可得到乙酰水杨酸粗产品。
4.2 乙酰水杨酸的纯化
将制得的粗产品转入到100mL烧杯中,加入饱和碳酸氢钠水溶液,边加边搅拌,直到不再有二氧化碳产生为止。抽滤,除去不溶性聚合物(水杨酸自身聚合)。再将滤液倒入100mL烧杯中,缓缓加入10mL20%盐酸,边加边搅拌,这时会有晶体逐渐析出。将此反应混合物置于冰水浴中,使晶体尽量析出。抽滤,用少量冷水洗涤2~3次。抽干后,取少量乙酰水杨酸, 加几滴乙醇使其溶解,再滴加1~2滴1%三氯化铁溶液,观察是否发生显色反应。
如果发生显色反应,则说明仍有水杨酸存在。此时产物可用乙醇-水混合溶剂重结晶。即先将粗产品溶于少量沸腾的乙醇中,向乙醇溶液中添加热水,直至溶液变混浊。加热至溶液澄清透明。注意:加热不能太久,以防乙酰水杨酸分解。静置慢慢冷却,晶体析出完全后过滤、干燥、称重、并计算产率。
5 实验数据记录与处理

0.047 mol 0.047mol
m理论=0.047×180.16=8.47g
5.1 固体的量取

5.2 数据的处理

6 实验结果与讨论
6.1 实验结果
本实验采用浓硫酸催化法制备乙酰水杨酸,其中制得粗产品的质量为_______g,纯产品的质量为_______g,本次实验的产率为_______%。
6.2 误差分析
6.2.1 系统误差:使用台秤、量筒、量取药品时产生误差;
6.2.2 随机误差:反应未进行完全,有副反应发生;结晶、纯化及过滤时,有部分产品损失。
6.3 注意事项
6.3.1 由于分子内氢键的作用,水杨酸与醋酸酐直接反应需在150~160℃才能生成乙酰水杨酸,而加入酸的目的主要是破坏氢键的存在,使反应在较低的温度下(90℃)就可以进行,而且可以大大减少副产物,因此实验中要注意控制好温度;
6.3.2 此反应开始时,仪器应经过于燥处理,药品也要事先经过干燥处理;
6.3.3 如粗产品中混有水杨酸,用1%三氯化铁检验时会显紫色。
6.3.4 粗产品可用乙醇—水,或1:1(体积比)的稀盐酸,或苯和石油醚(30~60℃)的混合溶剂进行重结晶。
6.3.4 乙酰水杨酸受热后易发生分解,分解温度为126~135oC,因此在烘干、重结晶、熔点测定时均不宜长时间加热;
6.4 收获体会
在本次实验中,我了解了如何设计一个实验,学会了用酰化反应制取乙酰水杨酸,掌握了利用重结晶的方法提纯有机物。在实验中,我感受到了设计并完成一个实验的辛苦与喜悦。
参考文献
[1] http://ks.cn.yahoo.com/question/1406090908746.html
[2] 田旭,林沛和.苯甲酸钠催化合成乙酰水杨酸的研究[J].《延边大学学报》,32(3).
[3] 李继忠.对甲苯磺酸催化合成乙酰水杨酸的研究[J].化学世界,2005(6):365~367.
[4] http://hi.baidu.com/boya123000/blog/item/7ecdcf9564133f4ed0135e30.html;
http://202.203.160.57/jpkc/yjhx/needs/jxzy/实验
Preparation and purification of acetyl salicylic acid
Fan Qianfeng
(Chemistry department, Applied chemistry,class094, Learning numbers 2009122210)
The abstract The purpose of this experiment are familiar with the principle of Acylation and experimental methods of operation, and learn to use the method of purification of organic compounds by recrystallization. Experiments, will be the role of salicylic acid and acetic anhydride to concentrated sulfuric acid as catalyst, through the acetylation reaction are acetyl salicylic acid, and then saturated sodium carbonate aqueous solution were added and 20% hydrochloric acid for purification of crude products. Through this experiment results we can see that the experimental method is simple and readily available raw materials for experimentation, get a higher product purity, the basic requirements in line with preparation.
Keywords aylation reaction, acetyl salicylic acid, preparation, purification
第二篇:6、乙酰水杨酸的制备

有 机 化 学 实 验 报 告

实 验 名 称: 乙酰水杨酸的制备
学 院: 化学工程学院
专 业: 化学工程与工艺
班 级:
姓 名: 学 号:
指 导 教 师:
日 期:
一、实验目的
1、学习乙酰水杨酸的制备原理和方法。
2、进一步掌握搅拌、抽滤等基本操作。
3、了解乙酰水杨酸的主要性质和作用。
二、实验原理
1、乙酰水杨酸,即阿斯匹林(aspirin),是 19 世纪末合成成功的,作为一个有效的解热止痛、治疗感冒的药物,至今仍广泛使用,有关报道表明,人们正在发现它的某些新功能。阿斯匹林是由水杨酸(邻羟基苯甲酸)与醋酸酐进行酯化反应而得的。水杨酸可由水杨酸甲酯,即冬青油(由冬青树提取而得)水解制得。
2、乙酰水杨酸制备的反应式:
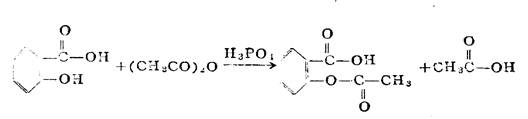
三、主要试剂及物理性质
1、 主要药品:水杨酸、乙酸酐、磷酸、饱和碳酸氢钠、浓盐酸、95%乙醇、1%FeCl3
2、相关试剂的物理性质
水杨酸:水杨酸为白色结晶性粉末,无臭,味先微苦后转辛。其熔点157-159℃,在光照下逐渐京变色。相对密度1.44。沸点约211℃/2.67kPa。76℃升华。常压下急剧加热分解为苯酚和二氧化碳。水杨酸与三氯化铁水溶液生成特殊的紫色。
乙酸酐:无色透明液体,有刺激性气味(类似乙酸),其蒸气为催泪毒气。其熔点为-73.1℃,沸点为138.6℃,相对密度1.08。易溶于苯、乙醇、乙醚,氯仿,渐溶于水(变成乙酸)。 可以用作乙酰化试剂,以及用于药物、染料、醋酸纤维制造、制引发剂、漂白剂等。
乙酰水杨酸:白色针状或板状结晶或粉末。无气味,微带酸味。其熔点135℃。在干燥空气中稳定,在潮湿空气中缓缓水解成水杨酸和乙酸。能溶于乙醇,乙醚和氯仿,微溶于水,在氢氧化碱溶液或碳酸碱溶液中能溶解,但同时分解。
四、试剂用量规格
1、称取水杨酸2.03g。
2、量取乙酸酐5ml,浓盐酸5ml。
3、准备15ml饱和碳酸氢钠。
4、准备试剂水70ml。
五、实验装置
1、主要仪器:100ml烧杯、100ml锥形瓶、玻璃棒、温度计、电炉、吸滤瓶、布氏漏斗、滤纸、量筒
2、实验过程的装置图
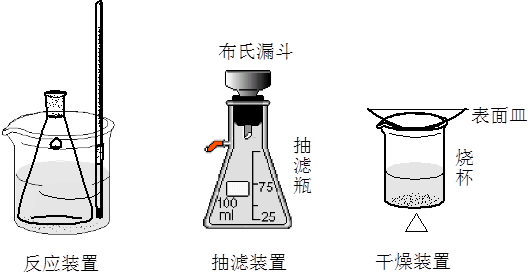
六、实验步骤及现象

七、产率计算
1、乙酰水杨酸的产率=实际产品质量∕理论值*100%
2、表面皿的质量为29.63g,表面皿与产品的总质量为40.47g。
乙酰水杨酸的理论值为2.64g。
即实际产率=0.84∕2.64*100%=31.70%
八、结果与讨论
1、本次实验制备出的乙酰水杨酸晶体质量为0.84g,其实际产率为31.70%。该实验产率值偏小,主要原因是在多次结晶与抽滤过程中有产品损失。
2、本实验的几次结晶都比较困难,就需要足够的耐心。在冰水冷却下,用玻棒充分磨擦器皿壁,促进晶体结晶出来,使之结晶更加完全,以减少实验的误差。
3、在抽滤过程中,由于产品微溶于水,所以水洗时,要用少量冷水洗涤,用水也不能太多,以减少晶体的损失。
4、本实验的反应过程处在一个无水体系中,有水存在就会造成副反应而影响实验结论,所以在实验前要把玻璃装置烘干,除去任何水渍。此外,反应时的水浴温度不能高于90℃,否则就有副产物出来。
5、本实验反应的副产物包括水杨酰水杨酸酯、乙酰水杨酰水杨酸酯和聚合物。乙酰水杨酸能溶于碳酸氢钠水溶液,而副产物不能溶于碳酸氢钠水溶液,从而通过滴加饱和碳酸氢钠将副产物除去。
-
乙酰水杨酸的制备实验报告
一实验目的1通过本实验了解乙酰水杨酸阿斯匹林的制备原理和方法2进一步熟悉重结晶熔点测定抽滤等基本操作3了解乙酰水杨酸的应用价值二实…
-
乙酰水杨酸的制备实验报告
乙酰水杨酸阿司匹林的合成实验报告一教学要求1通过本实验了解乙酰水杨酸阿斯匹林的制备原理和方法2进一步熟悉重结晶熔点测定抽滤等基本操…
-
乙酰水杨酸的制备的预习实验报告
乙酰水杨酸的制备一实验目的1了解和熟悉乙酰水杨酸的基本方法2巩固抽滤的技术操作二实验原理乙酰水杨酸又名阿司匹林aspirinCAS…
-
实验1 乙酰水杨酸的合成实验报告
实验1乙酰水杨酸的合成实验目的掌握由酸酐作为酰基化试剂和醇反应制备酯的方法巩固普通蒸馏抽滤重结晶等基本操作学习应用显微镜熔点仪测定…
-
乙酰水杨酸的制备实验报告[1]
乙酰水杨酸阿司匹林的合成实验报告一教学要求1通过本实验了解乙酰水杨酸阿斯匹林的制备原理和方法2进一步熟悉重结晶熔点测定抽滤等基本操…
-
乙酰水杨酸片的制备-_戎欣玉
乙酰水杨酸片的制备一实验目的掌握湿法制粒压片的一般工艺单冲压片机的使用方法及片剂质量的检查方法通过本实验使学生对工业药剂学药物分析…
-
乙酰水杨酸的制备实验报告
乙酰水杨酸阿司匹林的合成实验报告一教学要求1通过本实验了解乙酰水杨酸阿斯匹林的制备原理和方法2进一步熟悉重结晶熔点测定抽滤等基本操…
-
实验1 乙酰水杨酸的合成实验报告
实验1乙酰水杨酸的合成实验目的掌握由酸酐作为酰基化试剂和醇反应制备酯的方法巩固普通蒸馏抽滤重结晶等基本操作学习应用显微镜熔点仪测定…
-
乙酰水杨酸的制备的预习实验报告
乙酰水杨酸的制备一实验目的1了解和熟悉乙酰水杨酸的基本方法2巩固抽滤的技术操作二实验原理乙酰水杨酸又名阿司匹林aspirinCAS…
-
乙酰水杨酸实验预习报告
乙酰水杨酸有机化学实验报告实验项目名称乙酰水杨酸的制备一实验目的1了解和熟悉乙酰水杨酸的基本方法2巩固抽滤的操作技术二实验基本原理…