三草酸合铁酸钾综合实验报告
三草酸合铁(Ⅲ)酸钾的合成实验报告
一、本实验的制备方法
三草酸合铁(Ⅲ)酸钾的合成
1.称取4.0g FeSO4·7H2O,+5ml 去离子水溶解,+数滴3mol/LH2SO4,加热→+20ml 1mol/L H2C2O4,加热煮沸→不断搅拌,产生FeC2O4沉淀→倾析法洗涤三次
2.取黄色FeC2O4·2H2O,+10ml饱和K2C2O4→加热至40℃,+20ml 3%H2O2并不断搅拌→沉淀转化为黄褐色→加热至沸,在近沸状态下+5ml H2C2O4,趁热+3~4mlH2C2O4调节pH值至3.5左右→将溶液浓缩至25~30ml,冷却→翠绿色K3[Fe(C2O4)3]·3H2O析出,抽滤,称重。
二、本实验的分析方法
㈠.配阴离子组成测定
1.KMnO4溶液的配制
①配置
称取1.6g KMnO4,+1000ml水溶解→盖上表面皿,加热煮沸23~30分钟→冷却→在暗处放置7~10天→用微孔漏斗或玻璃棉滤去MnO2→棕色瓶中储存,摇匀
②标定
称取Na2C2O4 0.10~0.12g,置于250ml锥形瓶,+20~30ml去离子水,+10ml 3mol/L H2SO4→加热至75~80℃(不可煮沸)→立即用待标定KMnO4滴定至浅红
2
试液的测定
称取K3[Fe(C2O4)3]·3H2O 1.0~1.2g,加水溶解→转移至250ml容量瓶,稀释
3.C2O4离子的测定
取三份试液于锥形瓶,+MnSO4滴定液5ml,1mol/L H2SO4 5ml→加热至70~80℃,立即用KMnO4滴定至浅红色。
4.Fe(Ⅲ)离子的测定
取三份25ml试液于250ml锥形瓶,+6mol/LHcl 10ml→加热至70~80℃,逐滴缓慢加入Sncl2→溶液变为浅黄,此时大部分Fe3+变为Fe2+,加入Na2WO4 1ml,+Ticl3,过量一滴,+CuSO4 3~4滴,去离子水 20ml→冷却震荡至蓝色褪尽→1~2分钟后,+MnSO4滴定液10ml→用标准KMnO4溶液滴定4~5ml后,加热至70~80℃,再滴定至浅红色。
㈡.配阴离子电荷测定
①离子交换
1.装柱 在交换柱底部填入少量玻璃棉,8ml左右氯型阴离子交换树脂和适量水的糊状物注入交换柱→用塑料通条赶尽树脂间气泡,保持液面略高于树脂层
2.洗涤 用去离子水淋洗树脂直至流出液不含氯离子,用螺旋夹夹紧交换柱出口管,注意保持液面
3.交换 称取K3[Fe(C2O4)3]·3H2O0.5g→+10~15ml去离子水溶解,溶液转入交换柱中→松开螺旋夹,控制1ml/min的流速,用100ml容量瓶收集流出液→液面下降到略高于树脂层时,用少量去离子水洗涤小烧杯,并转入交换柱,重复2~3次→用去离子水继续洗涤,流速可适当加快→待收集溶液达60~70ml是检验流出液,只是不含氯离子,夹紧螺旋夹,稀释
4.再生 用20ml 1mol/L以1ml/min的流速淋洗交换树脂,直到流出液酸化后检不出Fe3+
②用氯离子选择性电极测定氯离子浓度
1.氯标准溶液系列的配置
1.00mol/L氯标准溶液10ml置于100ml容量瓶,+TISAB 9ml,稀释,得Pcl2=2→同样方法依次配置Pcl3=3,Pc,4=4等的溶液
2.标准曲线的绘制
电极的准备 反复清洗电极至空白电位值达到-240mV以上以缩短点击响应时间→更换双液接甘汞电极外管中KNO3
将仪器的选择开关旋钮置于mV档
将氯标准溶液系列转入小烧杯→氯离子选择性电极和双液接甘汞电极浸入被测溶液,加入搅拌子在酸度计上由浓到稀测电位
3.试液中氯含量的测定
取试液10ml,移入100ml容量瓶+10mlTISAB,稀释→测电位
四、实验结果
产品:产量:,产率:;产品颜色:翠绿色
配阴离子组成测定:
1.KMnO4的标定
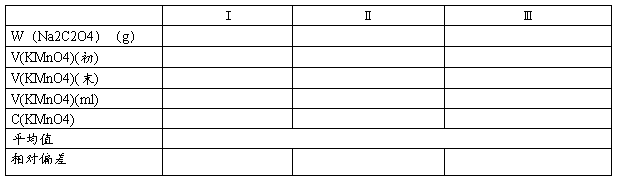
2.C2O42-的测定

3.Fe3+的测定数据
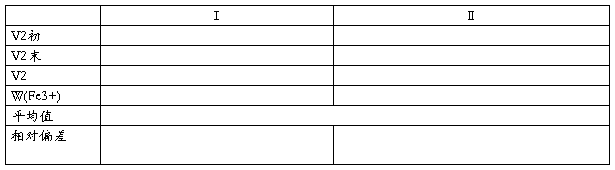
配阴离子电荷测定
氯标准溶液及试样的E/mV数据

结果:试样的克数 ;试样的PCl mV
试样中Cl-的物质的量;配阴离子电荷z
五. 讨论
1. 对产品的分析
(1) 要求产率>50%,产品颜色为翠绿色,分析产生偏差的原因
在合成K3[Fe(C2O4)3]·3H2O过程中,加入H2O2的速度太快,使得Fe2+未被完全氧化,导致得到的晶体偏黄;导致部分过氧化氢分解,Fe2+未被完全氧化,加热FeC2O4过程中溶液暴沸,飞溅,造成部分损失;配合后溶液pH值偏低,未用K2C2O4溶液调节。
(2) C2O42-%、Fe3+%的测定值与理论值比较,分析原因
C2O42-%、Fe3+%的测定值均低于理论值。原因可能是:高锰酸钾溶液颜色较深,读数时有误差;滴定C2O42-前,加热温度可能过高,导致部分离子分解;在滴定过程中溶液温度低于60摄氏度。
(3) 配阴离子电荷z 偏大偏小的原因
实验测得配阴离子电荷数偏高。原因可能是:比色皿未洗净;制备过程中时草酸加得过多,pH值过低。
第二篇:化学实验报告
化学实验报告
姓名: 学号: 同组人: 实验名称:K3Fe[(C2O4)3](三草酸合铁(Ⅲ)酸钾)的制备
一、 实验目的
二、 实验原理
三、 实验步骤
1、草酸亚铁的制备
- 1 -
2、三草酸合铁(Ⅲ)酸钾的制备
四、 实验数据记录及处理
五、 实验结论
- 2 -
-
三草酸合铁酸钾综合实验报告
三草酸合铁酸钾的合成及配离子组成电荷数的测定综合实验报告一综述三草酸合铁酸钾是制备负载型活性铁催化剂的主要原料也是一些有机反应很好…
-
三草酸合铁酸钾的制备与测定
三草酸合铁酸钾的制备与测定一、实验目的1、有助于提高学生的综合实验能力,而且可以提高学生对于化学实验的兴趣。2、掌握制备过程中的称…
-
三草酸合铁(III)酸钾的制备 实验报告
大学化学实验实验报告北京火工大学高材壹叁壹贰班无机及分析化学实验实验题目三草酸合铁III酸钾的制备实验日期月班级高材1312学生姓…
-
三草酸合铁酸钾的合成和组成测定综合实验报告
三草酸合铁酸钾的合成和组成测定综合实验报告一综述一三草酸合铁酸钾的性质及用途三草酸合铁酸钾是一种绿色单斜晶体溶于水0时47g100…
-
三草酸合铁酸钾综合实验报告
三草酸合铁酸钾的合成及配离子组成电荷数的测定综合实验报告一综述三草酸合铁酸钾是制备负载型活性铁催化剂的主要原料也是一些有机反应很好…
-
实验三草酸合铁(III)酸钾的制备和组成测定2齐齐哈尔大学化学专业 实验报告无机部分
齐齐哈尔大学实验报告题目三草酸合铁III酸钾的制备和组成测定学校齐齐哈尔大学专业班级化学101学生姓名叶梦同组者姓名苟登红成绩20…
-
齐齐哈尔大学化学专业实验三草酸合铁(III)酸钾的制备和组成测定
齐齐哈尔大学实验报告题目三草酸合铁III酸钾的制备和组成测定学校齐齐哈尔大学专业班级化学072学生姓名同组者姓名成绩齐齐哈尔大学化…
-
三草酸合铁酸钾综合实验报告
三草酸合铁酸钾的合成及配离子组成电荷数的测定综合实验报告一综述三草酸合铁酸钾是制备负载型活性铁催化剂的主要原料也是一些有机反应很好…
-
三草酸合铁酸钾的制备与测定
三草酸合铁酸钾的制备与测定一、实验目的1、有助于提高学生的综合实验能力,而且可以提高学生对于化学实验的兴趣。2、掌握制备过程中的称…
-
三草酸合铁(III)酸钾的制备 实验报告
大学化学实验实验报告北京火工大学高材壹叁壹贰班无机及分析化学实验实验题目三草酸合铁III酸钾的制备实验日期月班级高材1312学生姓…