完全互溶双液系的平衡相图
实验一 完全互溶双液系的平衡相图
实验者:顾后伟、郑学龙、朱以权 时间:9月29日
一、【目的要求】
1. 绘制常压下环己烷-乙醇双液系的T-X图,并找出恒沸点混合物的组成和最低恒沸点。
2. 掌握阿贝折射仪的使用方法。
二、【实验原理】
常温下,任意两种液体混合组成的体系称为双液体系。若两液体能按任意比例相互溶解,则称完全互溶双液体系;若只能部分互溶,则称部分互溶双液体系。
双液体系的沸点不仅与外压有关,还与双液体系的组成有关。恒压下将完全互溶双液体系蒸馏,测定馏出物(气相)和蒸馏液(液相)的组成,就能找出平衡时气、液两相的成分并绘出T-X图。如图2-4-1所示,图中纵轴是温度(沸点)T,横轴是液体B的摩尔分数xB(或质量百分组成)。上面一条是气相线,下面一条是液相线,对于某一沸点温度所对应的二曲线上的两个点,就是该温度下气液平衡时的气相点和液相点,其相应的组成可从横轴上获得,即x、y。
通常,如果液体与拉乌尔定律的偏差不大,在T-X图上溶液的沸点介于A、B二纯液体的沸点之间见图2-4-1 (a)。而实际溶液由于A、B二组分的相互影响,常与拉乌尔定律有较大偏差,在T-X图上就会有最高或最低点出现,这些点称为恒沸点,其相应的溶液称为恒沸点混合物,如图2-4-1(b)、(c)所示。恒沸点混合物蒸馏时,所得的气相与液相组成相同,因此通过蒸馏无法改变其组成。
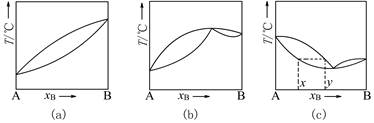
图2-4-1 完全互溶双液系的相图
本实验采用回流冷凝的方法绘制环己烷-乙醇体系的T-X图。其方法是用阿贝折射仪测定不同组分的体系在沸点温度时气相、液相的折射率,再从折射率-组成工作曲线上查得相应的组成,然后绘制T-X图。
三、【仪器药品】
沸点仪1套;量筒3只;恒温槽1台;小试管9支;阿贝折射仪1台;移液管(1mL,2支);。环己烷(A.R.);异乙醇(A.R.)。
四、【实验步骤】
1. 调节恒温槽温度比室温高5℃,通恒温水于阿贝折射仪中。
2. 测定折射率与组成的关系,绘制工作曲线。将9支小试管编号,依次移入0.100mL、0.200mL、…、0.900mL的环己烷,然后依次移入0.900mL、0.800mL、…、0.100mL的无水乙醇,轻轻摇动,混合均匀,配成9份已知浓度的溶液。用阿贝折射仪测定每份溶液的折射率及纯环己烷和纯无水乙醇的折射率。以折射率对浓度作图(按纯样品的密度,换算成质量百分浓度),即得工作曲线。

验完毕,将溶液倒入回收瓶中。
(2) 左半支沸点-组成关系的测定
取25mL环己烷加入沸点仪中,然后依次加入无水乙醇0.1mL、0.2mL、0.3mL、0.4mL、1.0mL、5.0mL。用前述方法分别测定溶液沸点及气相组分折射率ng、液相组分折射率nl。
五、【注意事项】
? 由于整个体系并非绝对恒温,气、液两相的温度会有少许差别,因此沸点仪中,温度计水银球的位置应一半浸在溶液中,一半露在蒸气中。并随着溶液量的增加要不断调节水银球的位置。
? 实验中可调节加热电压来控制回流速度的快慢,电压不可过大,能使待测液体沸腾即可。加热丝不能露出液面,一定要被待测液体浸没。
? 在每一份样品的蒸馏过程中,由于整个体系的成分不可能保持恒定,因此平衡温度会略有变化,特别是当溶液中两种组成的量相差较大时,变化更为明显。为此每加入一次样品后,只要待溶液沸腾,正常回流1~2min后,即可取样测定,不宜等待时间过长。
? 每次取样量不宜过多,取样时毛细滴管一定要干燥,不能留有上次的残液,气相部分的样品要取干净。
六、【数据处理】
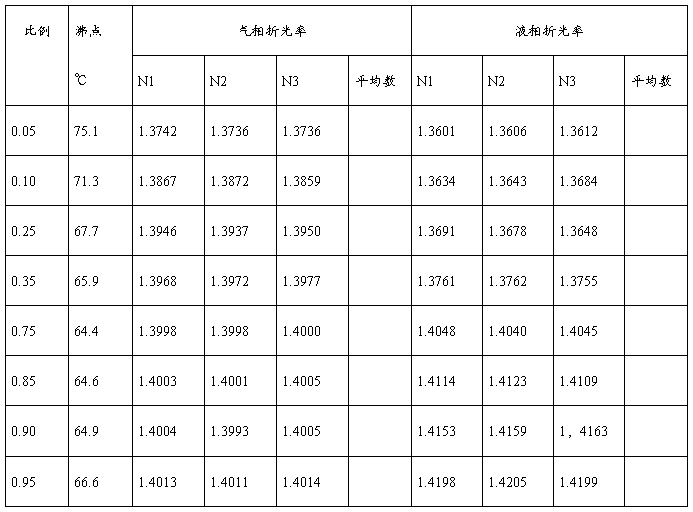
七、思 考 题
1. 该实验中,测定工作曲线时折射仪的恒温温度与测定样品时折射仪的恒温温度是否需要保持一致?为什么?
答:需要保持一致,因为折射率是温度的函数,样品中气液相组成是通过折射率曲线查得到。
2. 过热现象对实验产生什么影响?如何在实验中尽可能避免?
答:过热现象导致相图区域变窄,液相线上移。可以通过每次加入少量沸石或者通入新鲜空气避免。实验中我们通过调节加热电流得大小使沸腾得缓和来避免。
3. 在连续测定法实验中,样品的加入量应十分精确吗?为什么?
答:不需要,因为样品的组成是通过工作曲线查的而不是通过样品的加入量计算得到的。
第二篇:完全互溶双液系的平衡相图

-
四川理工物化实验报告-完全互溶双液系气液平衡相图的绘制
实验四完全互溶双液系气液平衡相图的绘制姓名吴春明学号10031010516班级工艺5班一实验目的1测定常压下环己烷乙醇二元系统的气…
-
完全互溶双液系气液平衡相图的绘制
完全互溶双液系气液平衡相图的绘制一实验目的1测定常压下环己烷乙醇二元系统的气液平衡数据绘制沸点组成相图2掌握双组分沸点的测定方法通…
-
完全互溶双液系气液平衡相图的绘制。实验报告
完全互溶双液系气液平衡相图的绘制一实验目的1测定常压下环己烷乙醇二元系统的气液平衡数据绘制沸点组成相图2掌握双组分沸点的测定方法通…
-
完全互溶双液系气液平衡相图的绘制实验报告
大学化学基础实验学院酿酒与食品工程学院专业食品科学与工程年级食科141学号1400940106140094010714009401…
-
完全互溶双液系统气-液平衡相图的绘制(2) 误差分析
大学化学实验实验报告物理化学部分贵州大学化学与化工学院大学化学教学与示范中心班级专业姓名岳凡耀学号0908100121指导教师谭蕾…
-
华师物化实验报告 双液系气-液平衡相图的绘制
华南师范大学实验报告学生姓名学号专业年级班级课程名称实验项目双液系气液平衡相图的绘制实验类型验证设计综合实验时间年月日实验指导老师…
-
四川理工物化实验报告-完全互溶双液系气液平衡相图的绘制
实验四完全互溶双液系气液平衡相图的绘制姓名吴春明学号10031010516班级工艺5班一实验目的1测定常压下环己烷乙醇二元系统的气…
-
二元完全互溶液体的相图。实验报告
二元完全互溶液体的相图一实验目的1绘制常压下环己烷异丙醇双液系的TX图并找出恒沸点混合物的组成和最低恒沸点2学会阿贝折射仪的使用二…
-
完全互溶双液系气液平衡相图的绘制。实验报告
完全互溶双液系气液平衡相图的绘制一实验目的1测定常压下环己烷乙醇二元系统的气液平衡数据绘制沸点组成相图2掌握双组分沸点的测定方法通…
-
完全互溶双液系气液平衡相图的绘制实验报告
大学化学基础实验学院酿酒与食品工程学院专业食品科学与工程年级食科141学号1400940106140094010714009401…