Cu-SiO2催化剂的制备与应用
Cu/SiO2催化剂的制备与研究
摘要:铜系氧化物及其金属单质负载型催化剂在醇类催化脱氢制取相应的酮、醛、酸等精细化工领域中有着重要的应用价值和广泛的工业应用前景,其中硅胶担载铜催化剂作为加氢催化剂已被广泛研究和应用。本文总结得出Cu/SiO2催化剂的制备常采用溶胶凝胶法和浸渍法,得到的催化剂较大范围的应用于酯类的加氢和醇类的脱氢等反应。但是其工业化生产和催化剂的进一步改性都有待更全面的研究。
关键词:Cu/SiO2催化剂;溶胶凝胶法;表征;合成
ABSTRACT: The supported catalysts of copper oxide and elementary metal copper has an important value and a widely used in fine chemical industry for catalytic dehydrogenation of alcohols obtained in the corresponding ketones, aldehydes, acids, including as a Silica-supported copper catalyst hydrogenation catalysts have been widely studied and applied. This paper summarizes the obtained catalyst Cu/SiO2 often used sol-gel method and Immersion method, the catalyst has been applied to a larger range of esters of hydrogenation and dehydrogenation reactions of alcohols. However, its industrial production and catalyst are further modified to be more comprehensive study.
Keywords:Cu/SiO2 catalyst;Sol-gel method;Characterization;synthesis
一.前言
近年来,Cu/SiO2催化剂在工业上有着广泛应用,作为一种铜基催化剂,对Cu/SiO2催化剂已经有了一个较深的研究。Cu/SiO2催化剂在乙醇脱氢合成乙醛、草酸二乙酯加氢、丙烯的环氧化反应、环境保护等方面都有很好的应用。
现阶段对如何用简单、低廉的原料和仪器制备具有高催化活性的Cu/SiO2催化剂引起了众多学者的关注.根据不同的制备过程和实验条件,活性物种在催化剂中可以形成多种分布状态,在催化反应中起到了不同的作用. Marchi等人的研究表明,CuO-SiO2催化剂上2种不同的CuO相具有不同的性质;Guerreiro等人报道离子交换方法制备的Cu催化剂中存在弱相互作用的Cu物种、高度分散在催化剂表面的Cu物种和表面相互作用的Cu物种[1].
二.制备方案
研究催化剂的制备方法具有极为重要的现实意义,不同的制备方法得到催化剂的性能可能有很大的区别,固体催化剂多数有较复杂的化学组成和物理结构,并因此形成千差万别的品种系列和纷繁用途,由于制备方法的不同,尽管成分、用量完全相同,所制出的催化剂的性能仍然可能有很大的差异[2]。催化剂的制备方法一般包括:沉淀法、溶胶-凝胶法、微乳化制备技术、熔融法、混合法、浸渍法、离子交换法、沉积沉淀法等。
Cu/SiO2催化剂的制备主要采用溶胶-凝胶法和浸渍法。
1. 溶胶-凝胶法
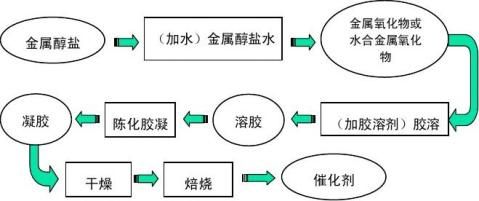
1.1溶胶-凝胶(Sol-Gel)法是一种新兴的催化剂制备方法,其制备过程是将易于水解的金属化合物(金属盐、金属醇盐或酯)在某种溶剂中与水发生反应,通过水解生成金属氧化物或水合金属氧化物,胶溶得到稳定的溶胶,再经缩聚(或凝结)作用而逐步胶凝化,最后经干燥、焙烧等后处理制得催化剂。
1.2溶胶凝胶法具有很多优点: 反应温度低,反应过程易于控制;制品的均匀度、纯度高;化学计量准确,易于改性,掺杂的范围宽;从同一种原料出发,改变工艺过程即可获得不同的产品如粉料、薄膜、纤维等;工艺简单,不需要昂
贵的设备。同时,它也存在一定的缺点:所用原料多为有机化合物,成本较高,有些对健康有害;处理过程时间较长,制品易产生开裂等。
1.3具体方法:
1.将水合硝酸铜(铜源)加适量去离子水搅拌溶解,再加人乙醇和TEOS(硅源),配比为n(TEOS):n(乙醇):n(水)=l:4:n,搅拌一定时间后,将混合液倒人塑料容器中,在室温(25℃)密封进行胶凝,得到绿色均匀透明的凝胶后,切成薄片,加人不同pH的氨水浸泡,然后放人75℃水浴中蒸干液体,再移人烘箱中于100℃下干燥24h。所得固体用蒸馏水洗涤、过滤直至滤液无色,滤饼在烘箱中于120℃下干燥12h,移人马弗炉中于450℃下焙烧5h,再压片成型,粉碎过筛,得到催化剂,催化剂试样记为CuSG-x(x为氨水的pH)。催化剂在使用前需经活化处理
[3]。
2. 11 ml TEOS 溶入 18.5 ml 无水乙醇,搅拌均匀,将一定量的催化剂、5 ml 水、等量乙醇混合,倒入 TEOS 与无水乙醇的混合物中,搅拌均匀,最后将含有 2%Cu 计算量的铜盐(Cu(NO3)2、CuCl2、Cu(CH3COO)2等)溶液 50ml缓慢滴入混合液中,再用硝酸或氨水调节 pH 值,强力搅拌 1h,室温老化 12h,在50℃水浴干燥20 h,110℃ 烘箱干燥 15 h,400℃焙烧 4 h。研磨,过筛到 40-60目[2]。
2. 浸渍法
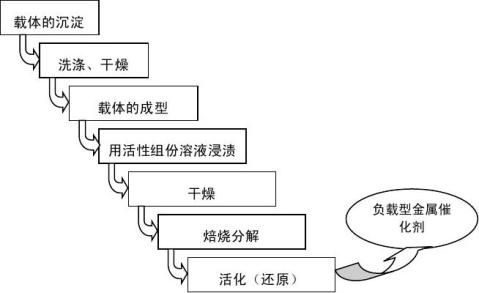
浸渍法广泛用于制备负载型催化剂,尤其负载型金属催化剂,其一般过程是把载体浸渍(浸泡)在含有活性组分(和助催化剂)的化合物溶液中,经过一段时间后除去剩余的液体,再经干燥、焙烧和活化(还原或硫化)后即得催化剂。
2.1浸渍法的优点主要有:
1.负载组分主要分布在载体表面,用量少,利用率高(对于贵金属催化剂尤其重要)
2.市场上有各种载体供应,可以用已成型的载体,省去催化剂成型步骤,而且载体种类很多、物理结构清楚,可根据需要选择合适的载体。 但是对载体有一定的要求,包括机械强度高;载体为惰性,与浸渍液不发生化学反应;合适的颗粒形状与尺寸,适宜的表面积、孔结构等;足够的吸水性;耐热性好;不含催化剂毒物和导致副反应发生的物质;原料易得,制备简单,无污染。一般常用载体为氧化铝、硅胶、分子筛、活性炭、硅藻土、浮石、活性白土、炭纤维、整体载体等。本实验采用的是硅胶作为载体。
2.2浸渍法分类
1过量浸渍法:将载体浸渍在过量溶液中,溶液体积大于载体可吸附的液体体积,一段时间后除去过剩的液体,干燥、焙烧、活化。
2等体积浸渍法:预先测定载体吸入溶液的能力,然后加入正好使载体完全浸渍所需的溶液量(实际采用喷雾法——把配好的溶液喷洒在不断翻动的载体上,达到浸渍的目的)。
3多次浸渍法:将浸渍、干燥和焙烧反复进行多次。应用于浸渍化合物溶解度小,一次浸渍达不到足够大的负载量;多组分浸渍时,竞争吸附严重影响各组分在载体表面上的分布;多组分浸渍时,各组分的可溶性化合物不能共存于同一溶液中(分步浸渍)。
2.3具体制备方法 1.实验采用等体积浸渍法[1],将一定量载体浸入一定浓度的硝酸铜水溶液中,室温浸渍15 h,于120℃的数显示电热恒温干燥箱中干燥4 h,再将其于马弗炉中焙烧。活性测试前将3 mL催化剂前体于50%H2、50%N2混合气中180℃还原3 h。 2. 过量搅拌浸渍法[4]是将预处理过的载体置入根据所需负载量配制一定浓度的Cu(NO3)2和助剂金属硝酸盐水溶液,,在室温条件下搅拌 12 小时后置入干燥箱,在空气气氛中 120℃干燥 6 小时,再在一定焙烧温度下焙烧 4 小时,分解硝酸盐成分。使用前在一定还原温度下还原 2 小时。
此外还有离子交换法的实例,根据所需负载量配制一定浓度的Cu(NO3)2和助剂金属硝酸盐溶液,向溶液中加入氨水,控制PH=10~11,将预处理过的载体置入溶液。在室温条件下搅拌 12 小时后,用蒸馏水洗去催化剂表面游离态的氨水,置入干燥箱,在空气气氛中 120℃干燥 6 小时,在一定焙烧温度下焙烧 4 小时,使用前在一定还原温度下还原 2 小时。
三 催化剂的表征
1.低温N2吸附[5],催化剂的比表面积、孔径、孔容在美国产全自动表面积及空隙测定仪,孔径、孔容在美国产全自动表面积及空隙测定仪上测定,按照BJH等效圆柱孔模型计算孔径分布曲线。操作条件:氮气为吸附质,在7737K吸附,He作载气。脱氢条件:573K,6.666Pa残压,抽空6h。
2. X 射线衍射(XRD),催化剂XRD谱图是在日本理学D/max 2400型X射线衍射仪上进行. CuKα辐射,管电压40 kV,管电流100 mA,扫描范围10-90°扫描速率5°/min.
3. TPD、TPR 分析[4]
采用AutoChem 2910型全自动化学吸附仪进行CO2的程序升温脱附(TPD)分析。考虑样品的酸碱性质比较弱,样品量取约100 mg,温度范围333~1073 K,
升温速率10 K/min,载气为高纯He,流速50 mL/min。在进行程序升温脱附之前,样品先在惰性气氛下在线程序升温到分析测试的最高温度并保持30 min进行预处理,升温速率为20 K/min。探针分子在333 K下脉冲注入流动的载气流中,被带到样品管进行吸附并记录响应信号,直到系统检测到响应信号强度不再变化或注样次数大于8次为止。探针分子吸附饱和后,先在同一温度下使用惰性气体继续吹扫60 min,再进行下一步的程序升温脱附并记录响应信号。
采用同一仪器进行程序升温H2还原(H2-TPR)分析,样品量同样取约 100mg,温度范围 333~923 K,升温速率 10 K/min,还原气氛为 10%H2-Ar,流速30 mL/min。进行程序升温还原实验之前,样品同样在惰性气氛下经过程序升温到分析测试的最高温度并保持 30 min进行预处理。
4. TGA、DSC分析
采用TA-50 型热分析系统进行催化剂的热失重分析。样品池为石英材质,每次装填样品量约为 10 mg。在N2气氛下进行程序升温,气体流量 30 mL/min,温度范围 303~973 K,升温速率 10 K/min,到设定的最高温度后停止信号记录。
采用DSC 204 hp型高压差示量热仪对催化剂在程序升温过程中的热量差异进行分析。样品量 5 mg。常压下在N2气氛中进行程序升温,气体流量 25 mL/min,温度范围 293~753 K,升温速率 10 K/min。
5.SEM分析,催化剂的扫描电镜图是由日本电子株式会社牛津仪器厂生产的JMS-6380LV型场发射扫描电子显微镜得到的。
四 Cu/SiO2催化剂的应用
4.1乙醇脱氢合成乙醛
乙醛作为重要的脂肪族化合物,是制造乙酸、乙酸酐、乙酸乙酯等多种重 要化学品的重要原料,具有很高的工业应用价值。制备乙醛的方法主要有乙烯氧化法、乙酸还原法、CH4和CO合成法、乙炔水合法、乙烷氧化法、C3/C4 烷烃氧化制乙醛[6]、乙醇氧化法和乙醇脱氢法等。
乙醇脱氢法采用价廉的铜系催化剂不仅节约生产成本,而且合成工艺反应条件温和,生产工艺无污染,对环境友好,是合成乙醛的先进生产方法之一。反应 温度较低、常压,温度控制在 270℃~300℃,乙醇转化率为 30%~50%,乙醛选 择性为 90%~95%,同时生成高纯度氢气,可直接用于加氢过程。合成工艺采用 固定床反应器,不需要分离生成物和催化剂的装置,而且操作简单。
马新宾、张悦[4]等人探索了以二氧化硅为载体(直径 2~3mm),铜为活性组分的负载型催化剂对于乙醇脱氢合成乙醛反应的催化性能,深入研究了铜负载量、催化剂制备方法、焙烧温度、还原温度、催化剂粒径、催化剂比表面积、助剂的选择以及助剂的加入量对反应的影响。评价结果表明,在反应温度为 275 ℃,反应空速为 3600h-1下,选用粒径为0.5~1.0mm的SiO2载体,采用等体积浸渍法制备的Cu-K2O/SiO2催化剂,在Cu负载量为 5wt.%,K负载量为 1wt.%时表现出最佳的催化反应活性。此时乙醇转化率为 31.9%,乙醛选择性为 93.8%,乙醛收率为 29.9%。在反应时间165小时内,催化剂催化活性基本没有下降。向催化剂体系引入 K、Na、Ca、Mg 等助剂以提高催化剂的活性,结果表明K、Na 助剂的加入使乙醛选择性明显提高。另外对 K、Na 助剂的负载量的影响做了进一步考察,确定 K、Na 助剂较佳的负载量均为 1wt.%。
4.2乙二醇的合成
乙二醇(EG)作为一种重要的有机化工原料,用途广泛,主要用于生产聚酷纤维、防冻剂、不饱和聚酷树脂、润滑剂、非离子表面活性剂等行业。由于大数乙二醇以石油制品环氧乙烷为基本原料制得,而石油资源日趋枯竭,因此有必要开发新的乙二醇生产工艺来对传统方法进行补充,其中草酸酯(如草酸二乙酯)加氢不但可以得到乙二醇,而且可以通过转化CO等有毒气体来改善环境,从经济和环保角度来看都具有很高的实用价值,尤其是对于石油资源缺乏的中国来说,此领域的研究显得更加重要和广阔的发展前景。
草酸二乙酯加氢合成乙二醇的工艺有以 Ru 等贵金属催化剂为主的液相均相加氢法和以负载型催化剂为主的非均相气相或液相加氢法。由于均相液相加氢需要在高压下进行,产品分离回收困难,所以更倾向于采用负载型催化剂进行气相或液相催化加氢,但早期的草酸酯加氢所用非均相催化剂中常含有铬元素,铬对人体和环境的危害极大,必须细致处理[7],这必然使成本大大提高。因此,新型非均相无铬催化剂的研发成为研究的热点之一,其中最具代表性的是以二氧化硅负载的铜基催化剂。
李竹霞、钱志刚[8]等人研究了草酸二甲酯的加氢反应,得出了在一定温度下,提高氢醋比和反应压力,乙二醇的平衡收率增加;而随温度升高和原料浓度降低,乙二醇的平衡收率下降。低氢醋比、低压和高溶剂比则有利于提高乙醇酸甲酷的平衡收率。
王保伟[19]、张旭[9]等在研究过程中得出用沉淀沉积法由铜氨溶液和硅溶胶制备Cu/SiO2催化剂时,并加法是最佳的滴加方法,可得到较均匀的活性位分布。350℃还原前驱体可获得最佳的Cu+/CuO。铜的最佳负载量为25%,温度240℃,压力1 MPa,氢/酯比200为反应的最优工艺条件。
与此同时,王 科,范鑫[10]等人在Cu/SiO2催化草酸酯加氢制乙二醇的探索过程中,用溶胶凝胶均匀沉淀法制备了负载型Cu/SiO2催化剂,在铜负载量 25%、活化温度 250℃~ 350 ℃、反应温度 180 ℃~190 ℃、反应压力 1.5MPa、氢酯比 100 以及液时空速 1.0h-1的条件下,可以获得最佳的催化加氢反应效果,使草酸二乙酯的转化率和乙二醇的收率分别达到 100%和 98%。
4.3甘油氢解制备1,2-丙二醇
甘油作为一种理想的可再生原料,以其为平台可以提供一条绿色且经济的生产大宗化学产品的途径。它作为生物柴油的副产物产量大,每生产 9 kg 生物柴油就有 1 kg粗甘油生成。甘油所富含的羟基易被官能化或降解,进而合成许多需要经过复杂的石油化工路线才能得到的化学品,其中选择性氢解可以得到各种二醇 ,包括乙二醇、1,2-丙二醇和 1,3-丙二醇等。近年来,有关甘油催化氢解合成 1,2-丙二醇的研究情况已有一定报道。报道的催化剂一般是含 Rh、Ru、Pt、PtRu、AuRu等贵金属以及 Ni基和 Cu基催化剂。研究表明在各种金属催化剂当中,对甘油催化氢解生成 1,2-丙二醇效果最好的是含Cu的催化剂。铜系催化剂对 C—C 键氢解的反应活性较低,而对C—O 键的氢解活性较高,具有较高的 1,2-丙二醇选择性。
顾 斌,王红[11]等研究了采用浸渍法制备的 Cu/SiO2催化剂,以甘油为原料采取两步法制备 1,2-丙二醇,其中较温和的反应条件有利于第一步的脱水反应,而第二步的加氢反应需要较高的温度和压力。其主要研究了第二步反应,即:以
甘油在催化剂上进行脱水反应生成的丙酮醇为原料加氢制备 1,2-丙二醇的工艺研究及催化剂设计。结果表明,负载量 10% Cu/SiO2催化剂表现出了较好的催化性能,在优化的反应条件下,1,2-丙二醇的收率达到 93.9%。
4.4其它方面的应用
除了以上的应用以外,Cu/SiO2催化剂还有其他方面的应用,鲁继青, 罗孟飞[12]等人研究了一系列用NaCl修饰的Cu/SiO2催化剂对丙烯在空气中直接环氧化反应的催化性能,结果表明在最佳反应条件下,丙烯转化率为0.16%,环氧丙烷选择性达到44%。石雷,孙军明[13]等人探索了Cu/SiO2催化剂用于一步法合成吲哚反应,其结果表明,当Cu/SiO2催化剂中铜负载量为0.68 mmol/g,焙烧温度为600℃,并且在150℃下经50%H2-50%N2混合气还原后,其催化性能最佳,吲哚收率可高达88%。董雪,苗治理,谭伟[14]等人以Cu/SiO2为催化剂研究了苯胺与正丙醇气相合成N-丙基苯胺,得出催化剂具有很好的活性和选择性,在铜担载量为0. 70 mmol/g SiO2、催化剂前体500℃焙烧4 h的最佳制备条件下,正丙醇转化率为100%,N-丙基苯胺的选择性高达92%,而且具有良好的稳定性。此外,Cu/SiO2催化剂还在甲醇脱氢制甲酸甲醋[15]、环己醇脱氢制备环己酮[16,18]、乙炔选择性加氢[17]等方面都有着广泛的研究与应用。
五 总结
Cu/SiO2催化剂作为一种工业化广泛的负载型催化剂,有着长久的研究历程,早期制备Cu/SiO2催化剂大多采用沉淀沉积法,浸渍法也应用广泛,近年来 溶胶凝胶法作为一种新型的制备方法,展现出来了反应温度低、纯度高、易于改性等优越性,其它制备方法也有一定的实例。而对Cu/SiO2催化剂的改性也有了相应的研究,如加入Al、Zn、Mg、K和Ca等助剂对催化剂催化性能的影响。对催化剂的改性主要是针对催化剂的应用进行的,通过加入助剂等研究对特定反应的反应速率、转化率和产率的影响。近年来,对Cu/SiO2催化草酸二乙酯加氢制乙二醇的研究较多,并取得了很好的效果,而对乙醇脱氢合成乙醛、乙炔选择性加氢、环氧丙烷的合成都有了相应的研究。但是,Cu/SiO2催化剂在更多反应和领域工业化的实现还有待更进一步的研究和改进,其制备方法和改性的探索还有很大的发展空间。
参考文献
[1] 孙琪,杨佳.溶胶凝胶法和浸渍法制备的Cu/SiO2催化剂的表征与性能[J].辽宁师范大学学报,2008,31(2):189-191.
[2] 杨佳.溶胶凝胶法制备的Cu/SiO2催化剂在NO+CO反应中的活性研究[D].辽宁:辽宁师范大学,2008.
[3]贺黎明,陈晓春.溶胶-凝胶法Cu/SiO2催化剂的表征与性能[J].石油化工,2010,39(12):1337-1343.
[4] 张悦.乙醇催化脱氢合成乙醛Cu/SiO2催化剂的研究[D].天津:津大学,2007.
[5] 刘会杰.草酸二甲酯加氢制乙二醇Cu/SiO2催化剂改性研究[D].上海:华东理工大学,2011.
[6] Weissermel K. , Arpe H. J. , 工业有机化学,北京:化学工业出版社,1998.
[7] Park D, Yun Y S, Park J M.Process Biochem, 2005,40(7): 2559.
[8] 李竹霞,钱志刚.Cu/SiO2催化剂上草酸二甲醋加氢反应的研究[J].化学反应工程与工艺,2004,20(2):121-128.
[9] 王保伟,张旭.Cu/SiO2催化剂的制备、表征及其对草酸二乙酯加氢制乙二醇的催化性能[J]. 催化学报,2008,29(3):275-280.
[10] 王科,范鑫.草酸酯加氢制乙二醇Cu/SiO2催化剂的制备及性能研究[J].天然气化工,2009,34(3):27-30.
[11] 顾斌,王红.Cu/SiO2两步法催化甘油氢解制备1,2-丙二醇[J].化工进展,2011,30(9):1961-1966.
[12] 鲁继青,罗孟飞.Cu/SiO2催化剂上丙烯在空气中的直接环氧化反应[J].催化学报,2004,25:5-9.
[13] Lei SHI, Jun Ming SUN. High Activity and Selectivity of Cu/SiO2 Catalyst for the Direct Synthesis of Indole [J].Chinese Chemical Letters,2002,13(3):211-212.
[14] 董雪,苗治理.Cu/SiO2催化剂上苯胺与正丙醇气相合成N-丙基苯胺[J].应用化工,2008,37(6):680-691.
[15] 李工,张红升.离子交换型Cu/SiO2催化剂用于甲醇脱氢制甲酸甲醋的研究[J].工业催化,1995,1:41-44.
[16] 吉定豪,王振旅. 碱金属掺杂对Cu/SiO2催化剂环己醇脱氢的影响[J].吉林大学学报,2007,45(2):293-296.
[17] 仲小慧.乙炔在Cu/SiO2催化剂上选择性加氢性能研究[D].大连:大连理工大学,2011.
[18] Chang H F,A bu SalequeM.Dependence of Selectivity on the PreparationMethod of Copper/α-Alumina Catalysts in the Dehydrogenation of Cyclohexanol [J]. ApplCatalA, 1993, 103: 233-242.
[19] ZHANG Xu,WANG Bao-wei.Deactivation behavior of SiO2 supported copper catalyst in hydrogenation of diethyl oxalate[J].Journal of Fuel Chemistry and Technology,2011,39(9):702-705.
-
二叉树的应用
二叉树的应用一实验目的1使学生熟练掌握二叉树的逻辑结构和存储结构2熟练掌握二叉树的各种遍历算法3熟悉二叉树的应用二实验内容本次实验…
-
二叉树的遍历和应用
内蒙古科技大学本科生课程设计说明书题目数据结构课程设计二叉树的遍历和应用学生姓名学号专业班级指导教师20xx年5月29日内蒙古科技…
-
二叉树的基本操作及其应用
广西工学院计算机学院数据结构课程实验报告书实验六二叉树的基本操作及其应用学生姓名学号班级指导老师专业计算机学院软件学院提交日期20…
-
树和二叉树的应用
数据结构实验报告实验题目树和二叉树的应用实验内容重言式判别实验目的掌握树和二叉树的概念及工作原理运用其原理及概念完成上述实验题中的…
-
二叉树的应用实验报告
实验报告课程名称数据结构上机实验实验项目二叉树的应用实验仪器PC机系别专业班级学号学生姓名实验日期成绩指导教师实验三二叉树的应用1…
-
信息化进程技术培训班工作总结
按照甘肃省计委甘计办[20xx]732号文的总体部署和要求,20xx年全省计划系统推进信息化进程技术培训班,历时一月,已于11月初…
-
机械设计基础课程改革总结
机械设计基础课程总结《机械设计基础》作为高职高专机电类专业的一门专业技术基础课。基于该课程在机电专业的核心地位,为了提高该课程的教…
-
20xx年理赔工作总结
理赔中心20xx年工作总结一、20xx年理赔重点工作20xx年对于理赔中心来说,是各项工作稳步提升的一年。理赔中心全年坚持“以客户…
-
会计工作年终总结
20xx年度,我校财务根据教育局年初工作计划及本校财务计划的要求,本着服务特殊教育发展的宗旨,以规范、合理、高效使用教育经费、为本…
-
户县电视台实习总结
20xx年x月x日,在学校的介绍下,我与本班数名同学前往户县电视台实习。在电视台领导的关心和调配下,我被分进了电视台新闻部,就这样…