食品中蛋白质的测定实验报告
1. 目的
掌握凯氏定氮法测蛋白质的原理、操作、条件、注意事项。
2. 原理
蛋白质是含氮有机化合物。食品与硫酸和催化剂一同加热消化,使蛋白质分解。分解的氨与硫酸结合生成硫酸铵。然后碱化蒸馏使氨游离,用硼酸吸收后在以硫酸或盐酸标准溶液滴定,根据酸的消耗量计算含氮量再乘以换算系数,即为蛋白质含量。
3. 试剂
3.1 浓硫酸、硫酸铜、硫酸钾,所有试剂均用不含氮的蒸馏水配制
3.2 混合指示液
1份(1g/L)甲基红乙醇溶液与5份1g/L溴甲酚氯乙醇溶液临用时混合。也可用2份甲基红乙醇溶液与1份1g/L次甲基蓝乙醇溶液临用时混合。
3.3 氢氧化钠溶液(400g/L)
3.4 标准滴定溶液
硫酸标准溶液[c(1/2H2SO4)=0.0500mol/L]或盐酸标准溶液[c(HCl)0.0500mol/L]
3.5 硼酸溶液(20g/L)
4. 仪器
定氮蒸馏装置
5. 样品
全蛋(2.47g)
6. 操作
6.1 样品处理
准确称取2—5g半固体样品,小心移入干燥洁净的500mL凯氏烧瓶中,
然后加入研细的硫酸铜0.5g,硫酸钾10g和浓硫酸20mL,轻轻摇匀后于瓶口放一小漏斗,将瓶以45°角斜放于加有石棉网的电炉上,小火加热,待内容物全部炭化后,泡沫完全消失后,加强火力,并保持瓶内液体微沸,至液体呈蓝绿色呈请透明后,再继续加热0.5h,取下放冷,慢慢加入20mL水。放冷后,移入100mL容量瓶中,并用少量水洗定氮瓶,洗液并入容量瓶中,再加水至刻度,混匀备用。取与处理样品相同的硫酸铜、硫酸钾、硫酸按同一方法做试剂空白试验。
6.2 连接装置
装好定氮装置,于水蒸气发生器内装水至2/3处,加甲基红指示剂数滴及少量硫酸,以保持水呈酸性,加入数滴玻璃珠以防暴沸,用调压器控制,
加热至水沸腾。
6.3 蒸馏、吸收及滴定
向接收瓶(锥形瓶)内加入10mL20g/L硼酸溶液及混合指示剂1-2滴,并使冷凝管的下端插入液面下。用移液管移取10.00mL样品消化稀释液有小漏斗室流入反应室,在将10mL 400g/L氢氧化钠溶液倒入碱液管中,提起玻璃塞使其缓缓流入反应室,并加水于小漏斗中以防止漏气。开始蒸馏。蒸气通入反应室使氨通过冷凝管而进入接收瓶内,蒸馏5min,移动接收瓶,是冷凝管下端离开液面,再蒸馏1min,然后用少量的水冲洗冷凝管下端外部。取下接收瓶,以0.05 mol/L盐酸标准溶液滴定至由蓝色变为微红为终点,记录盐酸溶液用量。
同时吸取10.00mL空白消化液按以上操作为空白实验,记录空白试验消耗盐酸标准溶液的体积。
7. 数据记录
7.1 原始数据
7.2 可疑值弃留
实验获得的数据均合理,无可疑值。
7.3 整理数据
粗滴/mL
5.90 精滴/mL 平行试验1 平行试验2 平行试验3 空白试验 5.30 5.50 5.60 0.45
8. 计算
(V标-V0)×Ca×0.014
X = ———————————— ×100×K
m样/V定×V测
式中:X—样品中蛋白质含量,%;
V标—主试验(测定用液)消耗硫酸或盐酸标准溶液的体积,mL;
V0—空白试验消耗硫酸或盐酸标准溶液的体积,mL;
Ca—硫酸或盐酸标准溶液的物质的量浓度,mol/L;
0.014—氮的物质的量质量×103,g/mol;
m样—样品的质量(体积),g(mL);
V定—消化液定容体积,mL;
V测—消化液参加测定(测定用液)的体积,mL;
K—氮换算为蛋白质的系数,蛋白质中的氮含量一般为15~17.6%,按16%
计算乘以6.25即为蛋白质,乳制品为6038,面粉为5.70,玉米、高粱为6.24,花生为5.46,米为5.95,大豆及其制品为5.71,肉或肉制品为6025,大麦、小米、燕麦、裸麦为5.83,芝麻、向日葵为5.30。
9. 结果
V标 =(V1+V2+V3)/ 3 =(5.30+5.50+5.60)/ 3 = 5.47
(V标-V0)×Ca×0.014 (5.47mL-0.45mL)×0.0500mol/L×0.014 X =——————————×100×K=—————————————————
m样/V定×V测 2.47g/100mL×10mL
×100×6.25=8.89%
10. 结果可靠性分析
10.1 精密度
平均偏差=(0.17+0.03+0.13)/3=0.11
相对平均偏差=(0.11/5.47) ×100%=0.02%
10.2 误差分析
10.2.1 根据实际操作情况分析误差的产生原因
在做空白实验前可能由于定氮瓶未完全清洗干净,有之前的样液残留或者之前样液产生的氨气未排空而导致空白实验消耗的标准溶液过多,使实验结果偏低。
10.2.2 误差的方向性
本实验产生误差为负误差。
11. 结论
三次平行试验均吸取10mL消化液,产生的氨气经吸收后以0.05 mol/L盐酸标准溶液滴定,消耗盐酸浓度依次为5.30mL、5.50mL、5.60mL(相对平均偏差为0.02%)。取三者平均值5.47mL计算得样品蛋白质含量为8.89%。由于空白实验前定氮瓶未完全清洗干净,有之前的样液残留或之前样液产生的氨气未排空导
致空白实验消耗的标准溶液过多,结果偏低,产生误差为负误差。
12. 思考题
12.1 为什么叫粗蛋白?
样品中常含有核酸、生物碱、含氮类脂、卟啉以及含氮色素等非蛋白质的含氮化合物,非纯蛋白质,故称粗蛋白。
12.2 试剂及用途?
浓硫酸:消化、氧化剂
硫酸铜:催化剂、指示消化终点
硫酸钾:使消化温度升高到400℃
混合指示剂:指示滴定终点
氢氧化钠溶液:用于蒸馏,使氨气溢出。
硼酸溶液:吸收液,将氨气固定于吸收液中,形成硼酸铵。
硫酸标准溶液或盐酸标准溶液:用于滴定,与硼酸铵反应
12.3 各步终点?
消化终点:溶液由黑色变为蓝绿色澄清透明。
蒸馏终点:凯氏瓶内溶液变为深蓝色或产生黑色沉淀,然后用表面皿接几滴馏出液,用奈氏试剂检查,如无红棕色物生成,表示蒸馏完毕。
滴定终点:用盐酸标准溶液直接滴定至溶液由蓝色变为微红色即为终点。
12.4 注意事项?
移液管不可交叉使用,防止酸碱试剂污染;蒸馏装置不能漏气;消化时,火力由弱到强,烧瓶倾斜呈45°;瓶口放一长颈漏斗;蒸馏与吸收,先进行吸收操作,冷凝管末端必须插入吸收液中,然后再进行蒸馏的操作;蒸馏结束时,将管离开液面,蒸馏1min,再用少量蒸馏水洗管外壁;滴定,先粗滴,后精滴。
12.5 叙述整个实验中有关颜色的变化,为什么?
消化终点:由黑色变为蓝绿色澄清透明。因为浓硫酸具有脱水性和氧化性,使有机物炭化呈黑色,待有机物全部被消化完后,不再有硫酸亚铜生成,溶液呈现清澈的蓝绿色。
蒸馏终点:凯氏瓶内溶液变为深蓝色或产生黑色沉淀。加入氢氧化钠后,与硫酸铜反应生成氢氧化铜沉淀,在高温下分解呈氧化铜,产生黑色沉淀。
滴定终点:用盐酸标准溶液直接滴定至溶液由蓝色变为微红色即为终点。硼酸铵是强碱弱酸盐,呈碱性,混合指示剂会显蓝色。用盐酸滴定后,溶液呈酸性,因此指示剂显微红色。
第二篇:食品中氨基酸及蛋白质的测定(实验报告)
 测定食品中的蛋白质 凯氏定氮
测定食品中的蛋白质 凯氏定氮
---2013.3.25
组员:***
实验目的:(1)会测定食品中粗蛋白的含量。
(2)明确常见的食品蛋白质含量,以及测定原理。
实验原理:将被检样品加入浓硫酸,以硫酸铜,硫酸钾为催化剂共同加热消化食品中蛋白质分解为氨,并与硫酸结合成硫酸铵,通过碱化蒸馏,使氨分离出来,用硼酸吸收形成硼酸按后,再用盐酸标准溶液滴定,根据消耗的标准盐酸的体积,通过换算系数,可测定食品中蛋白质的含量。
实验仪器:凯氏烧瓶、可调式电炉、定氮蒸馏装置
试剂:①硫酸铜CuSO4.5H2O ②硫酸钾 ③硫酸(密度为1.8149g/L) ④40g/L硼酸溶液 ⑤混合试剂;1g/L甲基红乙醇溶液与1g/L亚甲基蓝乙醇溶液,用时按2:1的比例混 合。
合。
实验步骤:

数据处理:标定0.1000mol/L盐酸标准溶液
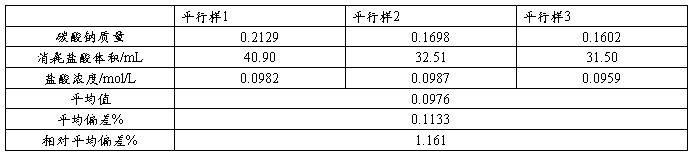

微量蒸馏按下式计算:
X=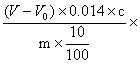 F
F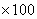
式中 X 食品中蛋白质质量分数,%;
V滴定试样时消耗盐酸标准滴定溶液的体积,mL;
V0 空白试验时消耗盐酸标准滴定溶液的体积mL;
C 盐酸标准滴定溶液的浓度;
0.014 氮的毫摩尔质量,g/mmol;
m 试样的质量,g;
F 氮换算蛋白质的系数。
注意事项:①本实验对蛋白质含量进行测定,因样品中常含有核酸、生物碱、含氮类脂以及含氮色素等非蛋白质的含氮化合物,故结果称为粗蛋白质含量。
②为减少实验误差,所有试剂溶液应用无氨蒸馏水配置。
③消化过程要不断转动凯氏烧瓶,以利于附着在烧瓶上的固体残渣被洗下,促进其消化;同时为防止造成氮损失,不要用强火,应保持缓和沸腾。
④样品中含脂肪或糖较多,消化过程中易产生大量泡沫,为防止泡沫外溢,在消化开始时用小火加热,并时时摇动,并可以加入少量辛醇、液体石蜡或硅油消泡剂,并控制热源强度。
⑤一般消化至呈透明后,继续消化30min即可,但对于含有特别难以氨化的氮化合物的样品,如含赖氨酸、组氨酸、色氨酸、酪氨酸或脯氨酸等时,呈较深绿色。
⑥当样品消化液不易呈透明时,可将凯氏烧瓶冷却,加入30%过氧化氢2-3mL后继续加热消化。
⑦蒸馏装置应密封,防止漏气;蒸馏过程中不得停火断气,防止放生倒吸,消化液呈蓝色不生成氢氧化铜沉淀,说明蒸馏前加碱量不足,要再增加氢氧化钠用量;蒸馏完毕后,应先将冷凝管下端提高液面,清洗管口,再蒸馏1min,而后关掉热源,否则可能造成吸收液倒吸。
⑧硼酸吸收液的温度不应超过40°C,否则对氨的吸收作用减弱而造成损失,此时可置于冷水浴中。
⑨混合指试剂在碱性溶液中呈绿色,在中溶液中呈灰色,在酸性溶液中呈红色。
实验体会:这次实验做得时间比较长,中间做消化的过程的时候第一天没有成功,当时感觉实验成功的希望不大,还好第二天有成功。
还有就是学会了凯式定氮仪的使用。
-
蛋白质的定量测定实验报告
显问题其次回顾全部过程的原理我们猜测可能存在的造成结果低的情况为在室温冷却后实验室没有空余的分光光度计排队时间应该是全部小组中最长…
-
蛋白质测定实验报告
蛋白质测定方法化学报告蛋白质的检测酚试剂法灵敏度较高20250mg费时蛋白质在碱性溶酚类柠檬液中其肽键与酸硫酸铵Cu2螯合形成tr…
-
蛋白质测定实验报告
生物化学实验报告姓名学号专业年级组别生物化学与分子生物学实验教学中心实验名称实验日期20xx1015合作者评分Folin酚试剂法测…
-
紫外分光光度法测定蛋白质含量实验报告
紫外分光光度法测定蛋白质含量一实验目的1学习紫外光度法测定蛋白质含量的原理2掌握紫外分光光度法测蛋白质含量的实验技术二实验原理1测…
-
分光法测蛋白质实验报告
紫外分光光度法测定蛋白质含量一实验目的1学习紫外分光光度法测定蛋白质含量的原理2掌握紫外分光光度法测定蛋白质含量的实验技术3掌握T…
-
蛋白质测定实验报告
蛋白质测定方法化学报告蛋白质的检测酚试剂法灵敏度较高20250mg费时蛋白质在碱性溶酚类柠檬液中其肽键与酸硫酸铵Cu2螯合形成tr…
-
蛋白质功能性质的检测实验报告
华南农业大学实验报告专业班次组别题目蛋白质功能性质的检测姓名黄俊怡日期20xx0711一实验目的通过本实验定性地了解蛋白质的主要功…
-
SCAU实验报告蛋白质功能性质的检测
蛋白质功能性质的检测一实验目的通过本实验定性地了解蛋白质的主要功能性质二实验原理蛋白质的功能性质一般是指能使蛋白质成为人们所需要的…
-
实验报告 蛋白质分子的测定
实验一蛋白质分子的测定凝胶层析法一实验原理凝胶层析法即凝胶过滤法gelfiltration是利用凝胶把分子大小不同的物质分离开的一…
-
蛋白质的定量测定实验报告
显问题其次回顾全部过程的原理我们猜测可能存在的造成结果低的情况为在室温冷却后实验室没有空余的分光光度计排队时间应该是全部小组中最长…