08�ﻯA��20xx������[1]
��������ѧ���γ��Ծ���A����
���Ծ������������뻯ѧ����ϵ20##����רҵ����ѧ��
������ʱ��120���ӣ��ܷ�100�֣�
ע�⣺1���𰸱�����д�ڴ���ֽ�ϣ���д���Ծ��ϵ���Ч��
2���������д����Ŀ��ţ��������˳����⡣
3���뱣���о࣬���־������ࡣ
һ��ѡ���⣨ÿ��ֻ��һ����ȷ�𰸣�ÿ��1.5�֣���30�֣�
1�� ������һ�����ǿ�����̵�������
A�� ����� B�����̽��е�ʱ������
C����ѹ����ѹ���һ������С D�����������ºۼ� [ ]
2�� Ħ�����������
A��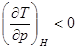 B��
B��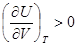
C��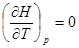 D��
D��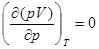 [ ]
[ ]
3�� ʵ�����廯ѧ��Ӧ�����¶��йص���
A��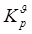 B��
B��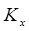
C��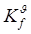 D��
D�� [ ]
[ ]
4�� ���A�����B���γ�������Һ�Ĺ�����
A��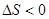 B��
B��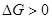
C�� D��
D��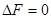 [ ]
[ ]
5��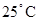 ��Ӧ
��Ӧ 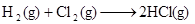 ��
��
A��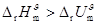 B��
B��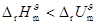
C��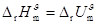 D��
D��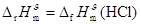 [ ]
[ ]
6�����¡���ѹ���������Ϊ������£��Է������Ļ�ѧ��Ӧ
A��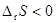 B��
B��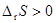
C�� D���������ֽ��п��� [ ]
D���������ֽ��п��� [ ]
7��ƽ�����������ʱ����ϵ�����ɶ�f�������C
A��f = 0 B��C = 0
C��f > 0 D��C < 0 [ ]
8��A��B���ɵ���ϵ����A��ƫĦ��������ʱ,B��ƫĦ����
A����֮���� B����֮��С
C�����ֲ��� D���������߽��п��� [ ]
9����Һƽ����ͼ��������Һ�������ϣ���ͼ��
A��������Һ��ͼ B���е㡪�����ͼ
C��ѹ���������ͼ D����������Һ��ͼ [ ]
10����Ӱ��缫���ƴ�С����������
A���¶� B��Ũ��
C���缫��Ӧʽ�е��ӵ����ʵ��� D�������ܶ� [ ]
11��A��B�γɵ���Һ�����ڶ������кܴ����ƫ��
A��A��B�γ���ߺ�л���� B��A��B���Ӽ��кܴ��������
C���ڽϵͷ�Χ��A��B���ֻ��� D������ʱA��B���������õ� [ ]
12��û��ƫĦ������״̬������
A��G B��p
C��V D��H [ ]
13���������Һ�������ӵ�Ǩ���ٶ��Ǹ�����Ǩ���ٶȵ�2���������ӵ�Ǩ������
A��2 B��3
C��2/3 D��1/3 [ ]
14�����ܽ��м������ʻᵼ��
A��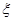 ���ƽ��� B������ѧ���ƽ���
���ƽ��� B������ѧ���ƽ���
C�����ܲ���� D�����Ŵ��������� [ ]
15������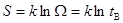 ����������˵���Ǵ����
����������˵���Ǵ����
A��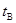 ��Boltzman�ֲ�������ѧ���� B��
��Boltzman�ֲ�������ѧ���� B��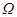 ��ϵͳ���е���״̬��֮��
��ϵͳ���е���״̬��֮��
C��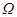 =
=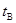 D��
D��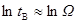 [ ]
[ ]
16���黯��ʹ��״Һ�ȶ�����Ҫԭ���ǣ�
A����������ճ�� B�����ͽ�������
C���γ�ǿ�Ƚϴ�Ľ���Ĥ D��ʹ������� [ ]
17��������Լ�C12H23O(C2H4O)20H����
A�������� B����������
C���������� D�����������Լ� [ ]
18����Ӧת���ʴ�50%��5min��ת���ʴ�75%��7.5min���÷�Ӧ�ļ�����
A��1�� B��2��
C��3�� D��4�� [ ]
19����Ӧ���¶�����ƽ�������ƶ����÷�Ӧ
A�����淴Ӧ�Ļ����� B������Ӧ�Ļ�ܴ�
C���淴Ӧ��ܴ� D����Ӧ��ϵ���ʹ��ڲ���ϵ���� [ ]
20�����ʵ��������ݺ�Һ������֮��
A�����¶����߶����� B�����¶����߶���С
C�����¶ȶ��� D���������߽��п��� [ ]
��������⣨ÿ��1�֣����ͼ2�֣���20�֣�
21�������̬Ϊ_____________________________________________________��
22��1mol ����������5pJ,300K��ʼ̬���������͵�2.5pJ,��״̬���ʵı仯��д����ֵ�͵�λ��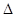 U=_________��
U=_________��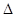 H=_________��
H=_________��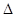 S=__________��
S=__________��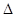 G=___________��
G=___________��
23��������ԭ���ɱ���Ϊ__________________________________________________,��������ʽ_________________________________����ġ�
24�����˹ά��ϵʽ֮һ��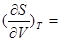 _________________________________________��
_________________________________________��
25������̬���ۻ����۵�ɸ���Ϊ___________________�� ��
��
26���ڹ⻯��Ӧ�ij��������У���Ӧ��ķ�Ӧ������_________________________��
27�����м����ܻ��õ����ɻ�������Ӧ����______________ ____�����н��ƴ�����
28��ͼ1��������ϵ��ͼ��
1������̬��____________________��2�������ɶ�����______________________��
3������̬��____________________��4������̬��__________________________��
a����ϵ����̬��_______________________����ͼ2�л���b����ϵ����ȴ���ߡ�
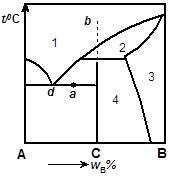

��������⣨ÿС��5�֣���15�֣�
29���γ�����Һ̬��������������Щ��
30�������������Ӧ�IJ��衣
31��д��0.1M AgNO3��Һ��0.2M KCl��Һ�������γɵĽ��ŵĽṹʽ��
�ġ������⣨ÿС��10�֣���30�֣�
32������101325Pa��105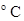 �£�1mol����ˮ����Ϊͬ��ͬѹ�µĹ���ˮ������W��Q��
�£�1mol����ˮ����Ϊͬ��ͬѹ�µĹ���ˮ������W��Q��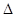 U��
U��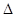 H��
H��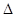 S��
S��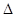 G,���жϹ����ܷ��Է�����֪100
G,���жϹ����ܷ��Է�����֪100 ��101325Pa��ˮ��������Ϊ40.6kJ×mol-1
��101325Pa��ˮ��������Ϊ40.6kJ×mol-1
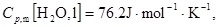
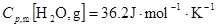 ��
��
33��д�����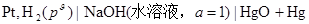 �ĵ缫��Ӧ�͵�ط�Ӧ����֪298K��������ص�
�ĵ缫��Ӧ�͵�ط�Ӧ����֪298K��������ص�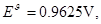

���㷴Ӧ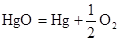 ƽ��ʱ
ƽ��ʱ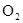 ��ѹ��
��ѹ�� ��������������
��������������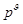 ��T=298K��
��T=298K��
34��340K�£������෴ӦB��2C�ĺ���ʵ�飬��ò�ͬʱ��B�ķ�ѹ ���ع�
���ع�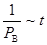 ���ݵúܺõ�ֱ�ߣ�ֱ��б��Ϊ
���ݵúܺõ�ֱ�ߣ�ֱ��б��Ϊ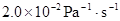 ��360K����������ʵ��õ���ֱ��б����
��360K����������ʵ��õ���ֱ��б����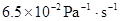 ������350K����Bѹ��Ϊ
������350K����Bѹ��Ϊ �¿�ʼ��Ӧ��100��ʱ��ϵ��ѹ������ߣ�
�¿�ʼ��Ӧ��100��ʱ��ϵ��ѹ������ߣ�
�塢�ۺ��⣨5�֣�
35.֤����
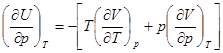
���
һ����ѡ��
1. D 2. D 3. C 4. C 5. C
6. D 7. A 8. B 9. B 10.C
11. C 12. B 13.C 14.A 15.C
16. C 17. A 18.D 19.B 20.B
���������
21��TK��pJ�´���������״̬��
22��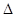 U=0,
U=0, 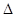 H=0 ,
H=0 , 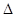 S=5.76 J·K
S=5.76 J·K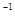
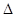 G=-1.729kJ×mol
G=-1.729kJ×mol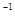
23��������ϵ����ȹ�������ϵ�����������١�
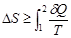 ��
�� 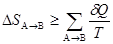
24��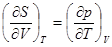
25����Ӧ�������γɻ���������ɲ����Ӧ��ͻ�����佨������ƽ�⣬�����ת��Ϊ�����ǿ��ٲ���
26���㼶
27����̬���Ʒ�
28��1����Һ̬ �� 2����f =1 �� 3���������嵥�ࣻ
4����������Ͳ��ȶ�������C��
a�㣺��A��s��+��C(s)+Һ�ࣨ�����d�㶨����
b����ϵ�������ߣ�

���������
29 ��V=0; ��H=0; ��S<0; ��G<0
30����1����Ӧ��������������������������ɢ������ɢ����
��2����Ӧ������������ڱ�����ɢ��
��3����Ӧ�������ڱ����ϣ�
��4����Ӧ���ڱ����Ͻ��л�ѧ��Ӧ�����ɲ��
��5������ӱ����Ͻ�����
��6�����������ɢ��
��7�����������ɢ��
31��
{[AgCl]m nCl����n��x��K+ }x+ x K+
�ġ�������
32���⣺
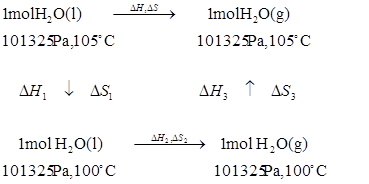
�����ͼʾ������̣��� 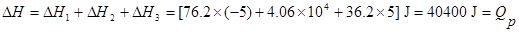
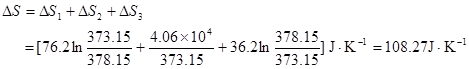
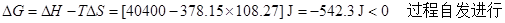

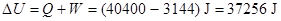
33���⣺��� 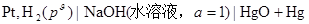
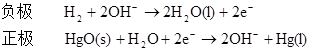
��ط�Ӧ�� 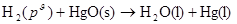
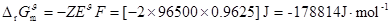
��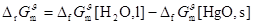
��
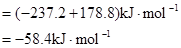
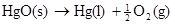

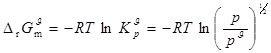
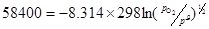
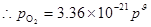
34���⣺��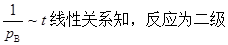
��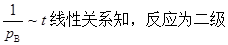
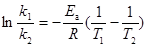
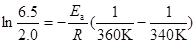
��֮ 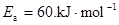
��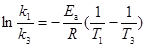
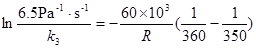
��֮ 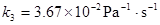
��Ӧ 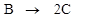
t = 0 pB0 0
ijt pB 2(pB0 �� pB) 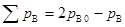
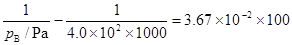
��֮  = 0.272 Pa
= 0.272 Pa
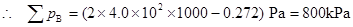
�塢�ۺ���
35��֤����
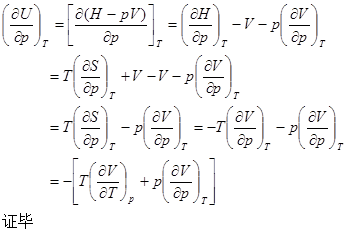
�ڶ�ƪ��08-09ѧ���1ѧ��������ѧ�Ծ�-����-A-��[1].
���ڷܡ����ǡ����¡����ף�
2008�� 2009 ѧ��� 1 ѧ�ڿ����Ծ�
������ʦ�� ��ݼ��
ѧԺ ��ѧ����ѧԺ �༶ __________ ���� __________ѧ�� ___________
��������ѧ���������γ��Ծ�A
����������ʱ�� 120���ӣ�
һ��ѡ���⣨���10С�⣬ÿС��2�֣���20�֣�
1. (2392)������ NH4HCO3(s) ������������У����µ� 400 K��NH4HCO3 ����ʽ�ֽⲢ�ﵽƽ��: NH4HCO3(s) = NH3(g) + H2O(g) + CO2(g)
��ϵ������� C �����ɶ��� f Ϊ�� ( ) (A) C= 2�� f= 1 (B) C= 2�� f= 2 (C) C= 1�� f= 0 (D) C= 3�� f= 2
(C) S = 4 C= S - R - R' = 4 - 1 - 2 = 1 f*= C+ 1 -��= 1 + 1 - 2 = 0
2. (2398)
�� N2,H2,NH3���������� 773 K,32 424 kPa �ĺϳ����У����д������ڵ����
�£�ָ�������������ʱ����ϵ�Ķ�������� C(1),C(2),C(3)��Ϊ����? ( )
(1) ������֮ǰ (2) �����ڷ�Ӧ��ƽ��ʱ (3) ��ֻ���� NH3��������ƽ��� (A) 3��2��1 (B) 3��2��2 (C) 2��2��1 (D) 3��3��2
(A) (1) ����ǰ�������� S = 3 ������������ C= 3 (2) �Ѵ�ƽ�� C= S - R - R' = 3 - 1 - 0 = 2
�����Ծ��� 1 ҳ �� 6 ҳ

(3) ֻ�� NH3����������ƽ�� C= S - R - R' = 3 - 1 - 1 = 1
�� 2NH3 ? N2+ 3H2 R = 1
�� [H2] = 3[N2] R' = 1
3. (4931) ��ͭ�缫��� CuCl2��ˮ��Һ���������ϻᷢ���� ( D )
(A) ��������
(B) ��������
(C) ����ͭ
(D) ͭ�缫�ܽ�
4. (3625) ��0.1 A�ĵ�������200 ml Ũ��Ϊ0.1 mol��dm-3��AgNO3��Һ�з���Ag������Һ�з����һ��������ʱ��Ϊ��
(A) 10 min
5. (4855) ��������������ʱ�����缫�ĵ缫���ƽ��������±仯�� ( B )
(A) ?ƽ������ ?�� �� ?ƽ������ ?��
(B) ?ƽ������ ?�� �� ?ƽ������ ?��
(C) ?ƽ������ ?�� �� ?ƽ������ ?��
(D) ?ƽ������ ?�� �� ?ƽ������ ?��
6. (5301) ij������ͬλ�صİ�˥��Ϊ 5 d ���� 15 d����ʣ��ͬλ�ص�����ԭ���ģ� ( C )
(A) 1/3
(B) 1/4
(C) 1/8
(D) 1/16
7. (5266) һ����Ӧ�Ļ����33 kJ��mol-1, �� T = 300 K ʱ���¶�ÿ���� 1K����Ӧ���ʳ������ӵİٷ���Լ�ǣ� ( A )
(A) 4.5%
(B) 90%
(C) 11%
(D) 50%
8. (5288) ij��Ӧ�ﷴӦ�� 7/8 �����ʱ��ǡ��������Ӧ�� 1/2 ����ʱ��� 3 ������÷� Ӧ�ļ����ǣ� ( B )
(A) �㼶
(B) һ����Ӧ
(C) ������Ӧ
(D) ������Ӧ
�����Ծ��� 2 ҳ �� 6 ҳ
�� B �� (B) 16 min (D) 160 min (C) 100 min
9. (7235)
ˮ�� ��K2Sn(OH)6 SnCl4��������SnO2(���ʳ���)����������������SnO2(�ܽ�), �����Ʊ��ܽ��� �����ǣ� ( B )
(A) ��ĥ��
10. (6654)���������ϸ���ѹ���ļ��㹫ʽ�� ?p = p' - p0= 2? /R' �У�R' �ķ��ţ� ( A ) (B) ���ܷ� (D) �绡�� (C) ��������ɢ��
(A) Һ��Ϊ��ʱΪ��������Ϊ��
(B) Һ��Ϊ��ʱΪ��������Ϊ��
(C) ����
(D) ����
��������⣨���10С�⣬ÿ��2�֣���20�֣�
1. (2312) �о�������ϵ��״̬����桢����ͼ������ʾ��ϵ��״̬�ı仯������ͼ��Ϊ״̬ͼ���Ϊ��ͼ��
��Ũ�� �¶� ѹ�� ��2�֣� ��ע��ÿ��һ����1�֣�
2. (2573) ��ȫ���ܵĶ������Һ���� xB= 0.6 ��ƽ������ѹ�����ֵ����ô���xB=0.4����Һ����-Һƽ��ʱ,xB(g)��xB(l)��xB(��)�Ĵ�С˳��Ϊ________________ ���� xB=0.4 ����Һ���о��֣��������õ� ___________ ��
xB(g) > xB(��) > xB(l) (1��)
xB= 0.6 ����� (1��)
3. (2324)��һ����������У�Ͷ��CaCO3(s)���ȷֽ��ƽ�⣬����������Ϊ����Ͷ��NH4HS(s)���ȷֽ��ƽ�⣬������������Ϊ��2��1
4. (5662) N2��H2�ϳ�NH3, ��400����, ����ѧʵ��ⶨ�������û�д���ʱ, ����Ϊ334.9 kJ��mol-1 ����Fe��ʱ, ��ܽ���167.4 kJ��mol-1��
�ٶ����ͷǴ���Ӧ��ָǰ�������, ����������£���Ӧ���ʳ���֮��ֵ
kc a t / k0) =_____ k(cat)/k0 =exp{[-E(cat)-E]/RT}=1013 _________________________��
5. (4070) Ũ��Ϊ0.1 mol��kg-1 ��MgCl2ˮ��Һ��������ǿ��Ϊ___________________ mol��kg-1 ��
[��] 0.3
6. (3906) 298Kʱ����H2SO4��Һ��Ũ�ȴ�0.01 mol��kg-1���ӵ�0.1 mol��kg-1ʱ����絼��?��Ħ���絼��?m����?__________________��?m____________________��(�������ӡ����ٻ�)
�����Ծ��� 3 ҳ �� 6 ҳ
2�֣� ��
3906
[��] ���ӣ�����
7. (5211) 2A��B��2C ��֪��Ӧijһ˲��, rA��12.72 mol��dm-3��h-1, �� ��2�֣�
rB�� , rC��___________________�� rB��6.36 mol��dm-3��h-1, rC��12.72 mol��dm-3��h-1
8. (6975) 25��ʱ��ˮ�ı�������Ϊ0.071 97 N��m-1����һ�����ܲ���ˮ�У�ˮ������5 cm��
��ëϸ�ܰ뾶Ϊ____________________��
r=(2��/��gh)=0.03cm
9. (6961) Һ���ڹ���������ʪ�̶���__________��������_________ʱ��Ϊ����ʪ�� �Ӵ���? ��? > 90��
10. (7492) ��pH��7��Al(OH)3�ܽ��У�ʹ��(1) Na2SO4 ��(2) NaCl ��(3) K3[Fe(CN)6]��
(4) KNO3���ֵ��������ͬʱ�䡢��ͬ�¶���ʹ��۳����۳������ɴ�С��˳��Ϊ�� _____________________________________________________________��
K3[Fe(CN)6]��Na2SO4��NaCl��KNO3
[��д�ɣ�(3)��(1)��(2)��(4)]
����10 �� (9410)
���ȷ�������öԶ��ױ��ͼ���ױ��IJ�������ת�۵����±���ʾ��
��1�����ƶԶ��ױ��ͼ���ױ����۵�-���ͼ��
��2��ָ������������������̬�����ɶȡ�
�𣺣�1��������ͼ���£�
�����Ծ��� 4 ҳ �� 6 ҳ
��2�֣�
����ױ� x(�Զ��ױ�) �Զ��ױ� ��6�֣�
��2������������������̬�����ɶ������±��� ��4�֣�
���� 1 2 3 4
���� 1 2 2 2
��̬ �ۻ���(l) l+����ױ�(s) l+�Զ��ױ�(s) ����ױ�(s)+�Զ��ױ�(s) ���ɶ� 2 1 1 1
�ġ�4639 10��
Ǧ���� Pb��PbSO4��H2SO4(1 mol��kg-1)��PbSO4��PbO2��Pb ,
�� 0��60�� ��Χ�� E/V = 1.91737 + 56.1��10-6(t/��) + 1.08��10-8 (t/��)2����֪ 25��, ������ص� E?= 2.041V����ˮ�Ļ��Ϊ 1���� m(H2SO4) = 1 mol��kg-1 ��ƽ�����ϵ����
[��] ��ط�Ӧ�� PbO2 + Pb + 4H+ + 2SO4���� 2PbSO4 + 2H2O (2��) E = E?- RT/2F �� ln[1/(aH+)4(aSO2-)2] (2��)
E = E?+ RT/F �� ln (a?)3 (1��) E = E?+ 3RT/F �� ln(??��m?/m?) (1��) m?/m?= 41/3 (1��) 25�� E = 1.919 V (1��) ??= 0.129 (2��)
�塢 15 �� (4323)
��� Pt,H2(p?)��NaOH(ϡˮ��Һ)��HgO(s)��Hg,Pt 298 Kʱ E��0.9261V
(A) д���缫��Ӧ����ط�Ӧ
(B) ��298 Kʱ��ط�Ӧ��ƽ�ⳣ��
(C) ��֪��?fHm(HgO)��-90.71 kJ��mol-1,��?fHm(H2O,l)= -285.84 kJ��mol-1,
�����Ծ��� 5 ҳ �� 6 ҳ
$$41 3 2 4 2?
�� E(308 K) ��
��: (A) H2��2OH-����2H2O��2e-
HgO��H2O��2e-����Hg��2OH-
������������������������������
��ط�Ӧ: H2(g)��HgO(s)����Hg(l)��H2O(l) (5��)
? (B) �˵�ط�Ӧ ?rGm��?rG$, ��E��E m
? ?rG$����RTlnK����zFE am
lnKa��(zFE?/(RT))��72.142 Ka��2.115��1031 (5��)
$$-1 (C) ?rH$(298 K)��?H(HO)��?H(HgO)����195.13 kJ��mol f2fmmm
$$-1-1 ?rS$��(?H��?G)/T����55.0 J��K��mol rrmmm
-4 -1 ��(?E/?T)p��?rS$/(zF)����2.85��10V��K m
E(308 K)��E(298 K)��(?E/?T)p(308��298)��0.923 V (5��)
����15 ��(5361) ��һ��յĸ��������У�����һ���������� A ���������·�Ӧ�� A(g) �� B(g) + 2C(g)
�跴Ӧ�ܽ�����ȫ����һ��ʱ����º�ʼ��ʱ�ⶨ��ϵ��ѹ��ʱ��ı仯���£�
(323 K)
t / min 0 30 50 ��
p��/ Pa 53329 73327 79993 106658
��Ӧ���������ʳ�����
[��] A(g)����B(g) + 2C(g)
t=0 p0 p' 2p' p0 = p0+ 3p'= 53 329 Pa (2��)
t=t p (p0-p)+ p' 2(p0- p) + 2p' pt = 3(p0+p') - 2p (2��)
t=�� 0 p0 + p' 2(p0+ p') p�� = 3(p0+p')=106 658 Pa (2��)
��� p'= 8 888 Pa p0 = 26 665 Pa (2��)
���� pt ʽ����� pt (30 min) = 16 666 Pa (2��) pt (50 min) = 13 333 Pa (2��)
Ӧ�ó��Է�����Ϊ������Ӧ���� p0 ��pt �������ʻ��ֹ�ʽ���� k�����ʳ�����Ϊ
������k=7.5��10-7(Pa)-1��min-1�� (3��)
�ߡ�10 �� (5686)
673 Kʱ����NO2(g)ͨ�뷴Ӧ����ѹ��Ϊ26.66 kPa��������ӦNO2(g) == NO(g) +
����㷴Ӧ����45.7 sʱ����Ӧ��ѹ����÷�Ӧ��ܶ��٣�
[��] k=3.07 dm3��mol-1��s-1 ������Ӧ ��2�֣�
NO2(g) == NO(g) + 1/2O2
t=0 p0=26.66 kPa 0 0
t=t p0-p p (1/2)p pt=p0+(1/2)p
(1/p0)-[1/(p0-p)]= -kt �� p=10.68 kPa �� pt=32.00 kPa ��6�֣�
k=Aexp(-Ea/RT) ����ʽ�Ƚ�
Ea/R=12.8867��103 K �� Ea=107.1 kJ��mol-1 ��2�֣�
�����Ծ��� 6 ҳ �� 6 ҳ
��ʵ��õ������ʳ������¶�T��ϵΪln(k/dm3��mol-1��s-1) = -12.8867��103 K/T+20.27��1O2��2
- ���꼶��ѧ������
- ���꼶��ѧ��ѧ����ĩ����
- ���꼶��ѧ�������ȫ
-
���꼶�ϲ���ĩѧ������
���꼶�ϲ���ĩѧ��������꼶�ϲ���ĩѧ������1��һѧ�����״̬�����ɽ���㲻���굽��Ҫ�߳���������������ڸDz��˵�һ������͡�
- ���꼶�ϲ�ѧ����ĩ����
-
����ƻ��ܽ�
ʤɽͷ�塰����ƻ��������ܽ�����ϼ����Ż��龫��Ϊ��ʵ����ѧУ��������ͥ����������������ϻ��ƣ�ȫ���ǿδ������˼����½��蹤��
- ����ʵϰ�±��ܽ� ���þ���ʵϰ�ܽ�
-
���������ܽ�
���꣬��˾�������ڹ�˾������ز��ҵ��쵼�£��������ȡ���˽Ϻõijɼ�����������ȫ�������棬���β������������ڷ��𣬷���ʤ�ھ��֡�
-
������ίԱ��20xx�����չ����ܽ�
�ݰ���ҽ�ƾ����������ίԱ���0һһ�깤���ܽ�һ�������ſ�20xx�������غ�ȫ��ҽ�ƾ����������ίԱ����������ĵڶ��ꡣ��ҽ��ί�ڡ�
-
���꼶�ط��γ̽�ѧ�ܽ�
20xx----20xxѧ�����꼶�ط��γ̽�ѧ�����ܽ᱾ѧ�ڣ����ǿ��贫ͳ�Ļ��γ̡���ȫ�γ̡������γ̡���ͳ�Ļ��γ��Ƕ������ͯ����