ҽ����е˵����
ҽ����е˵���顢��ǩ�Ͱ�װ��ʶ��дҪ��ʾ���ı�
ҽ����е������ҵӦ���ա�ҽ����е˵���顢��ǩ�Ͱ�װ��ʶ�����涨����Ҫ����ȷ��д˵���飬���е��������Ρ�����ʳƷ��ҩƷ�ල��������ע������ҽ����е˵��������ݲ������ԸĶ���
ҽ����е������ҵ�밴�������ݺ�Ҫ����˳����б�д��������������
���ݵ�10����Ļ���Ҫ�����˸�ʽ�����ο���
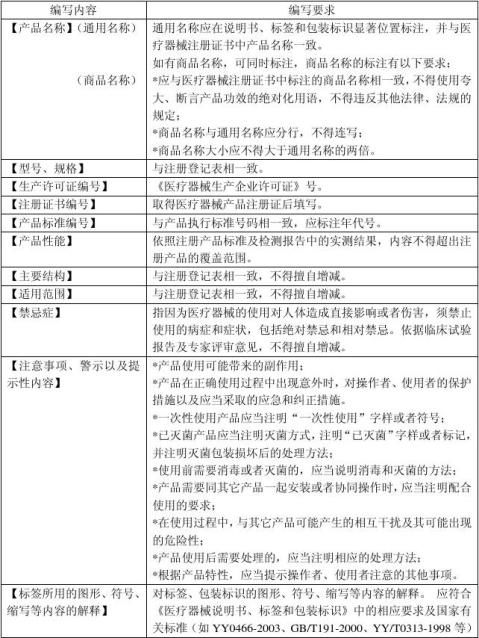
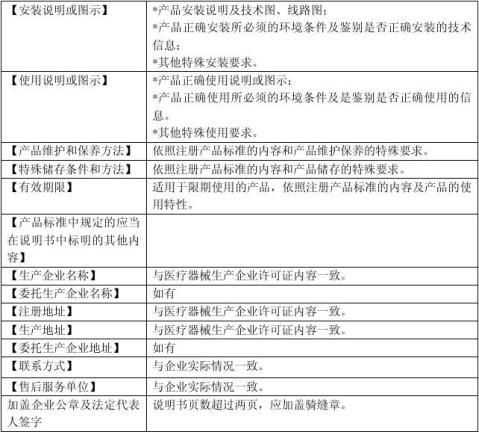
����ҽ����е��ǩ�Ͱ�װ��ʶ����

ע�����
1�� �����л������������ۡ�ʹ�õ�ҽ����еӦ�����ձ��涨Ҫ����˵���顢��ǩ
�Ͱ�װ��ʶ�������õIJ�Ʒ�����չ���ʳƷҩƷ�ල�����ֵĹ涨������ʡ��˵���顢��ǩ�Ͱ�װ��ʶ�����е�ijһ�����ij���
2�� ҽ����е˵������ָ��������ҵ���������Ʒ�ṩ���û��ģ��ܹ����Ǹò�Ʒ��ȫ��Ч
������Ϣ������ָ����ȷ��װ�����ԡ�������ʹ�á�ά���������ļ����ļ���������Ӧ����ʵ��������ȷ����ѧ�������Ʒ������һ�¡�ҽ����е��ҵӦ����˵�������ݵ���ʵ�ԡ������Ը��𣬲������κ���ʽ��ƭ���������ߡ�
3�� ҽ����е˵���顢��ǩ�Ͱ�װ��ʶ����Ӧʹ���������ֹ���ίԱ�ṫ���Ĺ淶�����֣�
���Ը����������֡�
4�� ˵���鲻�ú����������ݣ�
�� ��ʾ��Ч�Ķ��Ի��߱�֤���硰��Ч��ѡ�������֤�������������Ρ��������Ρ��������̼�Ч��
����ȫ�������á��ȣ�
�� ���Ի����Ժͱ�ʾ���硰��������������ѧ���������Ƚ���������ѡ��ȡ�
�� ˵���������ʻ�����Ч�ʵġ���
�� ��������ҵ��Ʒ�Ĺ�Ч�Ͱ�ȫ����Ƚϵģ�
�� ���С����չ�˾���ա�������Ч�˿�ȳ�ŵ�����Եģ�
�� �����κε�λ���߸��˵����塢������֤�������Ƽ��ģ�
�� ����ʹ�˸е��Ѿ�����ij�ּ���������ʹ����ⲻʹ�ø�ҽ����е�Ỽij�ּ�������
�ز���ı����ģ�
�� ���ɡ�����涨��ֹ���������ݡ�
����ҽ����е˵������Ҫ��
ҽ����еע��֤�����ͺš����������ַ����Ʒ������Ʒ���ܽṹ����ɡ���Ʒ���÷�Χ��������ģ�Ӧ���ա�ҽ����еע������취���Ĺ涨��������ע���������ҽ����е˵�����������ݡ�
������ҵ�����ҵ���ơ���Ʒ���ơ���Ʒ���������Ըı䡢��Ʒ�ͺš���������Ըı��Լ���Ʒ�������ƻ��ߴ��������Ըı䡢������ҵע���ַ�����������ַ�����Ըı�ģ�Ӧ���ա�ҽ����еע������취���Ĺ涨���б��ע���������ҽ����е˵�����������ݡ�
������ҵ�����ע������ҽ����е˵��������ݣ����漰��Ʒ�����Ա仯�ģ�������ҵӦ���ύ����ļ���������Ӧ�����֪�������ҽ����е˵�����������ݡ�
�ڶ�ƪ��ҽ����е˵��������涨

������ҵ֮�� ҽ����е˵��������涨
��20xx��1��4�չ���ҩƷ�ල���������30�ŷ�����,20xx��5��1����ʩ�У�20xx��7��8�շ�ֹ��
��һ�� Ϊ�淶ҽ����е˵��������ݣ�ȷ����ʹ�����ṩ��ȷ�IJ��������Ͳ�Ʒ�������Ϣ�����ݡ�ҽ����е�ල�������������ƶ����涨��
�ڶ��� �����л������������������ۡ�ʹ�õ�ҽ����е��Ӧ����˵����,ҽ����е˵����Ӧ�����ϱ��涨��Ҫ��
������ ҽ����е˵����Ӧ��������Ʒ����ȷʹ�õ�ȫ����Ϣ��������Ӧ����ʵ��ȷ����ѧ������,�����Ʒʵ������һ�¡��������κ���ʽ��ƭ���������ߡ�
������ ������ҵ�걨��ҽ����е˵����Ӧ�Ӹǹ��²��з���������ǩ��,���������ݵ���ʵ�ԡ������Ը���
������ �������м�ҩƷ�ල�������Ÿ������������������ĵ�һ��ҽ����е˵�����������ʡ����������ֱϽ��ҩƷ�ල�������Ÿ������������������ĵڶ���ҽ����е˵���������������ҩƷ�ල�����ָ����������ĵ�����ҽ����е������ҽ����е˵�����������
ҽ����е˵��������Ӧ��ҽ����еע�����һ�����У�˵���������Ӧ��ע�������й�������һ�¡�
������ ҩƷ�ල�������Ŷ�ҽ����е˵�������������Dz�Ʒ������Ʒ��ʽ���������ٴ����鱨�漰ר�����������������ҽ����е˵���鼰˵���������������ԸĶ���
������ ҽ����е˵����Ӧʹ�ù����������ֹ���ίԱ�ṫ���Ĺ淶����̩��ҽ�ƿƼ�����˾ tel:187xxxxxxxx
TEL��0731-8274 2552 Http:// ADD������ʡ��ɳ����´��´��·8������5�� 1


������ҵ֮��
������,���Ը����������֡�
�ڰ��� ҽ����е˵����Ӧ��ѭ����ҵ��Ʒʹ��˵���飭�����ұ�������ҽ����е�������ԣ�Ӧ�����������й����ݣ�
��һ����Ʒ���ơ����������ơ���ַ�������������ϵ�绰��
��������Ʒע��ţ�
������ִ�еIJ�Ʒ����
���ģ���Ʒ����Ҫ�ṹ�����ܡ����Ʒ��;�����÷�Χ������֢��ע�������ʾ����ʾ��˵����
���壩��ǩ����ʶ��ͼ�Ρ����š���д�����ݵĽ��ͣ�
��������װ��ʹ��˵����ͼʾ��
���ߣ���Ʒά���ͱ�������,���ⴢ�淽����ʹ�����ޣ�
���ˣ���Ʒ���й涨Ӧ�����е��������ݡ�
�ھ��� ������ҵ�����Ʒ��;�����÷�Χ������֢����Ʒ���������Ʒ���ơ����������ơ���ַ�ģ�Ӧ����ҽ����еע������취���Ĺ涨���б���������ҽ����е˵�����������ݡ�
��ʮ�� ҽ����е˵���鲻�ú����������ݣ�
��һ����ʾ��Ч�Ķ��Ի�֤���硰��Ч��ѡ�������֤�������������Ρ��������Ρ��������̼�Ч��������ȫ�������á��ȣ�
����������������������ѧ���������Ƚ��������ƾ��Ե����Ժͱ�ʾ��
������˵���������ʡ�������Ч�ʡ�����������ҵ��Ʒ��ȽϵĴ��P��������������ݣ�
���ģ������չ�˾���ա�������Ч�˿�ȳ�ŵ�����ԣ�
����̩��ҽ�ƿƼ�����˾ tel:187xxxxxxxx
TEL��0731-8274 2552 Http:// ADD������ʡ��ɳ����´��´��·8������5�� 2


������ҵ֮��
���壩�����κε�λ����������֯������������Ƽ���
������ʹ�˸е��ѻ�ij�ּ�����ʹ����ⲻʹ�ø�ҽ����е�Ỽij�ּ�������ز���ı�����
���ߣ����ࡢ���š��ĵ����ֲ������֣�
���ˣ����ɡ�����涨��ֹ���������ݡ�
��ʮһ�� ҽ����е��Ʒ����Ӧ���Ϲ���ҩƷ�ල�������ƶ���ҽ����е��������
��ʮ���� ҽ����е��ͨ������Ӧ�ڲ�Ʒ˵�����б���,����Ʒ���Ƶģ�Ӧͬʱ��ע��Ʒ���ơ�
��ʮ���� ҽ����е˵�������й�ע�������ʾ����ʾ��˵����Ҫ������
��һ����ƷԤ�����ܼ����ܴ����ĸ����ã�
��������Ʒ��ʹ�ù����г�������ʱ���Բ����ߺ�ʹ���ߵı�����ʩ��Ӧ��ȡ��Ӧ���;�����ʩ��
������һ����ʹ�ò�ƷӦע����һ����ʹ�á�������
���ģ��������ƷӦע���������������������IJ�Ʒ��Ӧע�������װ��Ĵ���������ʹ��ǰ��������Ӧ˵������������
���壩��Ʒ����ͬ������Ʒһ��װ��Эͬ����ʱ������ע������ʹ�ò�Ʒ�����ԣ�
��������ʹ�ù����У���������Ʒ��������ż�����ܳ��ֵ�Σ���ԣ�
���ߣ����ݲ�Ʒ�ص㣬Ӧ��ʾʹ���ߡ���Ӫ��Ӧע���������� ����̩��ҽ�ƿƼ�����˾ tel:187xxxxxxxx
TEL��0731-8274 2552 Http:// ADD������ʡ��ɳ����´��´��·8������5�� 3


������ҵ֮��
��ʮ���� ��װ��ָ�����ļ�������Ӧ�ܱ�֤�û���ȷ��װʹ�á�Ӧ������
��һ����Ʒ��װ˵��������ͼ����·ͼ��
��������Ʒ��ȷ��װ������Ļ��������������Ƿ���ȷ��װ�ļ�����Ϣ��
�������������ⰲװҪ��
��ʮ���� ҽ����е��ǩ�Ͱ�װ��ʶӦ�����Ϲ����йر���涨�����涨��������ݡ�
��ʮ���� ���涨�ɹ���ҩƷ�ල�����ָ�����͡�
��ʮ���� ���涨��20xx��5��1����ʩ�С���
����̩��ҽ�ƿƼ�����˾ tel:187xxxxxxxx
TEL��0731-8274 2552 Http:// ADD������ʡ��ɳ����´��´��·8������5�� 4

-
ҽ����е��Ʒʹ��˵����ģ��
����2XXXʹ��˵����Ʒ������Ʒ���ܽṹ��������÷�Χʹ��˵������֢ע��������Ч��������������֤��Ʒע��Ų�Ʒ��YZBǭ��������
-
ҽ����е˵����
ҽ����е˵�����ǩ�Ͱ�װ��ʶ��дҪ��ʾ���ı�ҽ����е������ҵӦ����ҽ����е˵�����ǩ�Ͱ�װ��ʶ�����涨��Ҫ����ȷ��д˵���鲢�е�����
- ҽ����е˵����ָ��ԭ��
-
ҽ����еʵ���Ե�ͬ�Ա�˵������
ҽ����еʵ���Ե�ͬ�Ա�˵��һ�����ò�Ʒ��һ������ҽ����е����Ŀ¼����6866ҽ�ø߷��Ӳ��ϼ���Ʒ����ע���Ʒ��YY032520x��
-
ҽ����е˵������ѵ
ҽ����е˵�����ǩ�Ͱ�װ��ʶ�����涨���Ҿ����10����ҵ���ƴ���˳ɼ�һ�����1ҽ����е˵������ָ��������ҵ���������Ʒ�ṩ���û���
-
ҽ����е��ͬ����
��ͬ��Ŀ������Ŀ��ż���ҽԺ�ҷ�������˾����˫��������Ŀ������Ŀ��ŵĽ��ǩ�𱾺�ͬһ��������1��������2�ͺŹ��3������λ����
- ҽ����е��Ӫ�������뷶��
-
ҽ����е��Ʒʹ��˵����ģ��
����2XXXʹ��˵����Ʒ������Ʒ���ܽṹ��������÷�Χʹ��˵������֢ע��������Ч��������������֤��Ʒע��Ų�Ʒ��YZBǭ��������
- ҽ����е˵����ָ��ԭ��
- ҽ����е�������Ϣ����ϵͳ����������ܺ���˵��