篇一 :药品不良反应报告表
药 品 不 良 反 应 / 事 件 报 告 表
报告类型:新的□ 严重□ 一般□ 首次报告□ 跟踪报告□ 报告来源:医疗机构□ 药品经营企业□ 药品生产企业□ 其他□
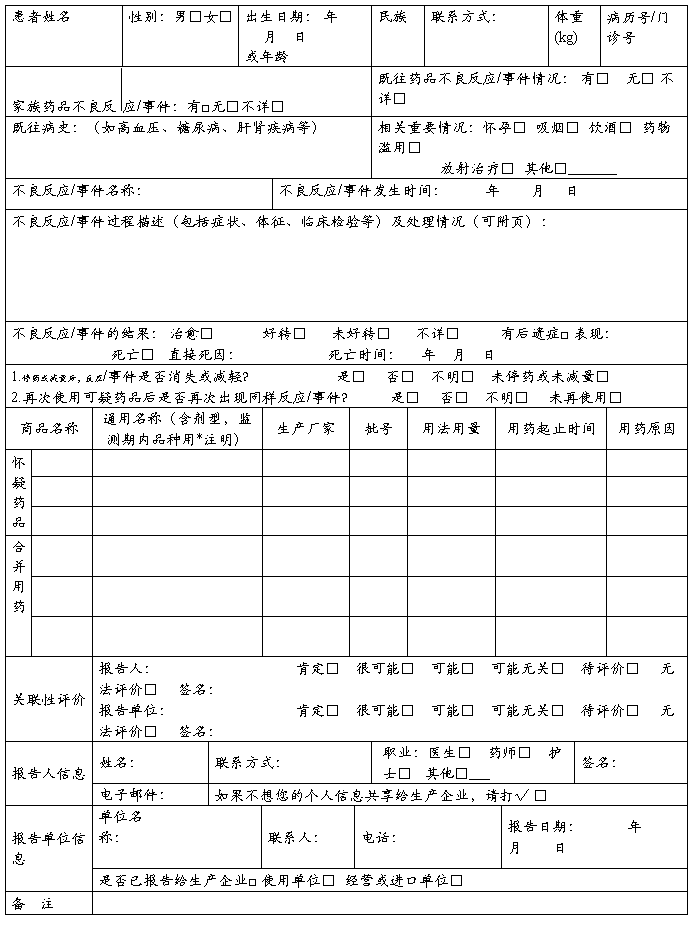
除非得到允许,报告表中的个人信息将予以保密。
严重药品不良反应/事件是指因使用药品引起以下损害情形之一的反应/事件:
1) 导致死亡;
2)危及生命;
3)致癌、致畸、致出生缺陷;
4)导致显著的或永久的人体伤残或器官功能的损伤;
…… …… 余下全文
篇三 :药品不良反应报告表模板
药品不良反应报告表
部分项目填报注意事项
一、药品不良反应事件名称及描述
1.如果患者出现皮疹伴瘙痒,不要把二者同时列为一个不良反应,应当分类描述为“皮疹;瘙痒”,
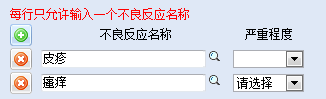
对于皮疹的发生部位、大约形态进行描述;
2.如果患者发生多种过敏反应,就不用分类描述,直接描述为“过敏反应”或是“过敏样反应”;不属于过敏反应的其他症状,应当分类描述;
3.如果患者出现过敏性休克,就必须描述患者的临床表现(包含呼吸道阻塞、微循环障碍、中枢神经系统症状及皮肤过敏症状)及体征;
例如头晕、面色苍白、呼吸困难、胸闷、腹痛、出汗、脉搏增快及血压下降等;此时相应的体征进行描述,如体温、心率、血压、呼吸频率等;还包含不良反应发生前后的症状和体征的动态变化。
4.如果患者出现血象异常,要将不良反应发生前后相应指标、实验室检查进行描述;
例如患者白细胞降低,此时就需要提供患者入院时(或服药前)白细胞指数,服药后发生不良反应是监测的白细胞指数以及采取措施停药后患者白细胞有所恢复的指数。
5.如果患者出现消化道反应,例如腹泻、呕吐等,请具体描述一哈相关的症状;
…… …… 余下全文
篇四 :药品不良反应报告表样本
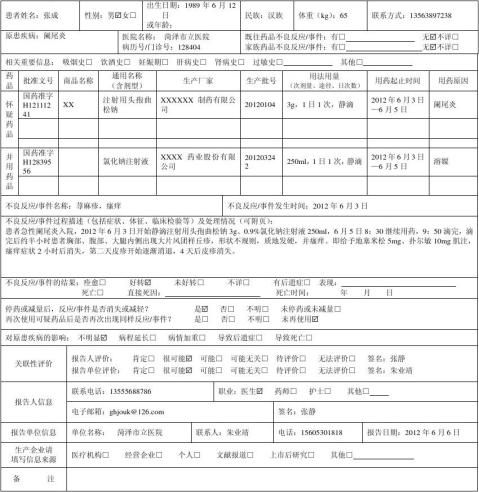
附:2.《药品不良反应报告表》填写范例
制表单位:国家药品监督管理局
紧急□ 一般√ 编号:□□□□□□□□□□□□□□□
药 品 不 良 反 应 报 告 表(医疗单位使用)
医院名称:解放军第251医院 科别:呼吸科 电话:8785120 报告日期: 20##年1月18日
…… …… 余下全文
篇五 :药品不良反应报告表
附表1 制表单位:国家食品药品监督管理局
药品不良反应 / 事件报告表
新的□严重□一般□ 医疗卫生机构□ 生产企业经营企业□ 个人□ 编码□□□□□□□□□□□□□□□□□□□
单位名称: 部门: 电话: 报告日期: 年 月 日
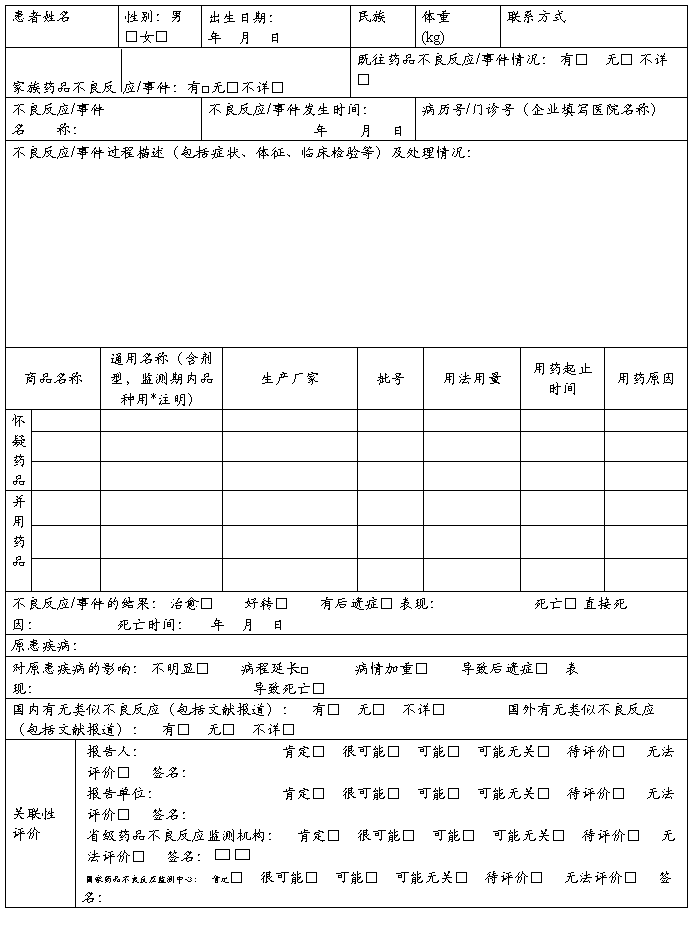
报告人职业(医疗机构):医生□ 药师□ 护士□ 其他□ 报告人职务职称(企业): 报告人签名
◇不良反应/事件分析

◇严重药品不良反应/事件是指有下列情形之一者:
① 引起死亡 □
② 致畸、致癌或出生缺陷 □
③ 对生命有危险并能够导致人体永久的或显著的伤残 □
④ 对器官功能产生永久损伤 □
⑤ 导致住院或住院时间延长 □
…… …… 余下全文
篇七 :药品不良反应-事件报告表
例表1
药 品 不 良 反 应 / 事 件 报 告 表
首次报告□ 跟踪报告□ 编码: 报告类型:新的□ 严重□ 一般□ 报告单位类别:医疗机构□ 经营企业□ 生产企业□ 个人□ 其他□
附表2
药 品 不 良 反 应 / 事 件 报 告 表
首次报告□ 跟踪报告□ 编码: 报告类型:新的□ 严重□ 一般□ 报告单位类别:医疗机构□ 经营企业□ 生产企业□ 个人□ 其他
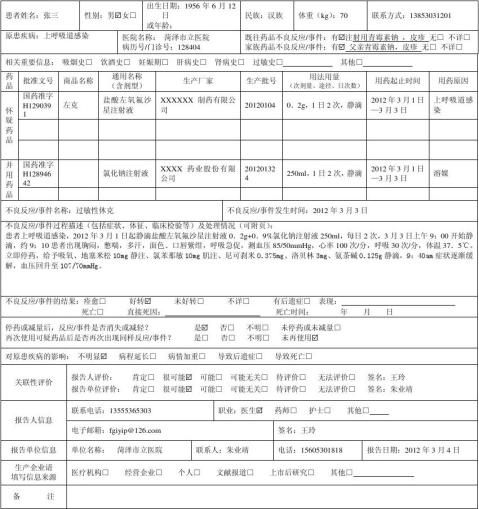
不良反应过程描述:
3个时间3个项目和2个尽可能
3个时间:
• 不良反应发生的时间;
• 采取措施干预不良反应的时间;
• 不良反应终结的时间(好转、缓解、消失)。
3个项目:
• 第一次药品不良反应出现时的相关症状、体征和相关 检查;
• 药品不良反应动态变化的相关症状、体征和相关检查;
• 发生药品不良反应后采取的干预措施结果。
2个尽可能:
…… …… 余下全文
篇八 :药品不良反应报告表填写要求
药品不良反应报告表填写要求
《药品不良反应报告和监测管理办法》(以下简称《办法》)中针对不同报告类型提供了三份表格,分别是《药品不良反应/事件报告表》、《药品群体不良反应/事件报告表》和《药品不良反应/事件定期汇总表》;为全面贯彻落实《办法》,国家食品药品监督管理局药品安全监管司在20xx年2月印发的《关于定期汇总报告和进口药品境外发生的不良反应报告有关问题解释的通知》(国食药监安[2005]89号)文件中对有关问题进行了说明,同时在文件中公布了两份表格,分别是《定期安全更新报告提交表》和《进口药品在境外发生的不良反应/事件报告表》。下面将分别对五份表格填写要求进行详细的说明。
(一)《药品不良反应/事件报告表》
《办法》第十三条明确规定:药品生产、经营企业和医疗卫生机构必须指定专(兼)职人员负责本单位生产、经营、使用药品的不良反应报告和监测工作,发现可能与用药有关的不良反应应详细记录、调查、分析、评价、处理,并填写《药品不良反应/事件报告表》,每季度集中向所在地的省、自治区、直辖市药品不良反应监测中心报告,其中新的或严重的药品不良反应应于发现之日起15日内报告,死亡病例须及时报告。
…… …… 余下全文